专题训练一:基本理论――物质结构与周期律
(每题只有一个最佳选项)
1、同温同压下,等容积的两个密闭集气瓶中分别充满12C18O和14N2两种气体。关于这两个容器中气体的说法正确的是
A、质子数相等,质量不等 B、分子数和质量都不相等
C、分子数和质量都相等 D、原子数、中子数和质子数都相等
2、下列说法错误的是
A、原子及其离子的核外电子层数等于该元素所在的周期数
B、元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
C、除氦外的稀有气体原子的最外层电子数都是8
D、同一元素的各种同位素的物理性质不同、化学性质基本相同
3、关于晶体的说法正确的是
A、在晶体中只要有阴离子就一定有阳离子
B、在晶体中只要有阳离子就一定有阴离子
C、原子晶体的熔点一定比金属晶体的高
D、分子晶体的熔点一定比金属晶体的低
4、国际无机化学命名委员会在1989年做出决定,把长式周期表原先的主、副族及族号取消,由左至右改为第1~18列,碱金属族为第1列,稀有气体为第18列,按这个规定,下列说法不正确的是
A、第2列元素中肯定没有非金属元素
B、第15列元素的最高价氧化物为R2O5
C、第17列元素的第一种元素的单质具有强氧化性
D、第16、17列元素都是非金属元素
5、从实验中测得不同物质中O―O之间的键长和键能的数据为:
| O22- | O2- | O2 | O2+ | |
| 键长(10-12m) | 149 | 128 | 121 | 112 |
| 键能(kJ/mol) | x | y | z=494 | w=628 |
其中x、y的键能数据尚未测定,但可以根据规律性推导键能的大小顺序为w>z>y>x,该规律性是
A、成键时电子数越多,键能越大 B、键长越长,键能越小
C、成键所用的电子数越少,键能越大 D、成键时电子对越偏移,键能越大
6、下列各分子中所有原子都满足最外层8电子结构的是
A、光气(Cl―C―Cl) B、五氯化磷 C、三氟化硼 D、溴乙烷
O
7、下列各物质熔化或气化时,所克服的微粒间相互作用属同种类型的是
A、干冰和萘的升华 B、二氧化硅和生石灰的熔化
C、苯和汞的蒸发 D、氯化钠和钠的熔化
8、下列化学式及结构式中,从成键情况来看不合理的是
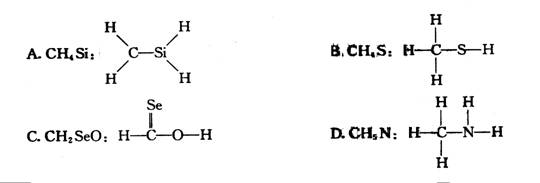
9、有M、R两种主族元素,已知M2- 和R+离子核外电子数之和为20,则下列说法不正确的是
A、M与R的质子数之和一定等于19
B、M、R可能分别处于第二周期和第三周期
C、M、R可能分别处于第三周期和第二周期
D、M与R的质子数之差可能等于7
10、下列各组物质各自形成的晶体,均属于分子晶体的化合物是
A、NH3、HD、C10H8 B、PCl3、CO2、H2SO4
C、SO2、SiO2、P2O5 D、CCl4、Na2S、H2O2
11、下列有关共价化合物的叙述正确的是:①都有较低的熔、沸点;②都是电解质;③固态时都是分子晶体;④都有以分子形式存在;⑤液态时都不导电
A、①③④⑤ B、②④⑤ C、只有⑤ D、全部错误
12、下列数据是各物质的熔点(℃)
| NaCl | Na2O | AlF3 | AlCl3 | BCl3 | Al2O3 | CO2 | SiO2 |
| 801 | 920 | 1291 | 190 | -109 | 2073 | -57 | 1723 |
据此做出下列判断,其中错误的是
A、Al的化合物的晶体中有离子晶体
B、只有BCl3和干冰是分子晶体
C、同族元素的氧化物可形成不同类型的晶体
D、不同族元素的氧化物可形成相同类型的晶体
13、下列叙述中,正确的是
A、两种粒子,若核外电子排布完全相同,则其化学性质一定相同
B、凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
C、两种原子,如果核外电子排布相同,则一定属于同种元素
D、可能存在两种质子数和电子数均相同的阳离子和阴离子
14、关于晶体的下列说法中,正确的是
A、氢化物一定属于分子晶体 B、离子晶体都有是离子化合物
C、分子晶体都是共价化合物 D、原子晶体都是固态单质
15、主族元素X、Y、Z的离子为aX+、bY2-、cZ-,其离子半径大小关系是:X+< Z-< Y2-。下列说法不正确的是
A、Y2-的还原性大Z- B、单质的还原性X>Z
C、b一定小于c D、X、Y可处于同周期或X在Y的下一周期
16、下列关于只含非金属元素的化合物的说法中,正确的是
A、一定是共价化合物 B、其晶体不可能是离子晶体
C、其晶体不可能是原子晶体 D、有可能是离子化合物
17、短周期的三种元素分别为X、Y、Z,已知X元素的原子最外层只有一个电子,Y元素原子的M电子层上的电子数是它K层和L层电子总数的一半,Z元素原子的L电子层上的电子数比Y元素原子的L电子层上的电子数少2个,则三种元素所组成的化合物的化学式不可能是
A、X2YZ4 B、XYZ3 C、X3YZ4 D、X4Y2Z7
18、下列说法中不正确的是:①质子数相同的粒子一定属于同种元素;②同位素的性质几乎完全相同;③质子数相同,电子数也相同的粒子不可能是一种分子和一种离子;④电子数相同的粒子不一定是同一种元素;⑤一种元素只能有一种质量数;⑥某种元素的相对原子质量取整数,就是其质量数。
A、①②④⑤ B、③④⑤⑥ C、②③⑤⑥ D、①②⑤⑥
19、已知A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A的顺序依次减小,B和E同为ⅥA族,则下列推断中,不正确的是
A、 D位于第2周期 B、 A、D可能属同一主族
C、 A、B、E一定位于不同周期 D、 C和D的单质有可能化合形成离子化合物20、按核电荷数依次递增的短周期元素A、B、C,它们的原子序数之和为15,原子最外层电子数之和为11,周期数之和为5,则A、B、C不可能形成的化合物是
A、A2BC3 B、A2BC2 C、A2BC D、ABC3
21、能够用键能的大小作为主要依据来解释的是
A、常温常压下氯单质和溴单质的状态不同 B、氯化钠的熔点比溴化钠高
C、稀有气体一般难于发生化学反应 D、铝的化学性质比铁活泼
22、已知短周期元素的离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是
A、原子半径:A>B>D>C B、原子序数: d>c>b>a
C、离子半径:C>D>B>A D、单质的还原性:A>B>D>C
23、甲、乙两种非金属: ①甲比乙容易与氢气化合;②甲原子能与乙阴离子发生氧化还原反应;③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;④与某金属反应时,甲原子得电子数目比乙多;⑤甲的单质熔、沸点比乙低。能说明甲比乙的非金属性强的是
A、只有④⑤ B、只有⑤ C、①②③ D、①②③④⑤
24、右图是元素周期表的一部分。X、Y、Z、W均为短周期元素,若W原子最外层电子数是其内层电子数的7 / 10,则下列说法中不正确的是
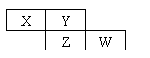 A、X元素的氢化物分子间可以形成氢键
A、X元素的氢化物分子间可以形成氢键
B、Y元素的两种同素异形体常温下都是气体
C、最高价氧化物对应水化物的酸性:W>Z
D、阴离子半径从大到小排列顺序为:X>Y>Z>W
25、由钠和氧元素组成的某种离子晶体中阴离子只有O2- 和O22-(过氧根离子)。在此晶体中氧元素和钠元素质量之比为48∶92,其中O2- 和O22-的物质的量之比为
A、1∶1 B、2∶1 C、1∶2 D、1∶3
专题训练一:基本理论――物质结构与周期律
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| A | A | A | D | B | A | A | A | D | B | C | B | C |
| 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| B | C | D | A | D | A | D | B | C | C | D | A |
专题训练一:基本理论――物质结构与周期律
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| A | A | A | D | B | A | A | A | D | B | C | B | C |
| 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| B | C | D | A | D | A | D | B | C | C | D | A |
专题训练一:基本理论――物质结构与周期律
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| A | A | A | D | B | A | A | A | D | B | C | B | C |
| 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| B | C | D | A | D | A | D | B | C | C | D | A |
专题训练一:基本理论――物质结构与周期律
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| A | A | A | D | B | A | A | A | D | B | C | B | C |
| 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| B | C | D | A | D | A | D | B | C | C | D | A |
专题训练一:基本理论――物质结构与周期律
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| A | A | A | D | B | A | A | A | D | B | C | B | C |
| 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| B | C | D | A | D | A | D | B | C | C | D | A |