����߿�����Ԫ�ز���ѡ����
1�� p��ij�ᾧˮ����A��nH2O,����ʧȥȫ���ᾧˮ��,������Ϊq��,�ɴ˿��Ե�֪�ýᾧˮ����ķ�����Ϊ

2���ֱ���������������ʸ�100��:��KMnO4����KClO3(��������MnO2����HgO.��ȫ��Ӧ��,���ų����������ɶൽ�ٵ�˳����
(A)��>��>�ۡ�����(B)��>��>��
(C)��>��>�ڡ�����(D)��>��>��
3�����д�����Ⱦ����,����������Ѫ�쵰��϶������ж���������
(A)SO2������(B)CO2 ����(C)NO2 ����(D)CO
4������һ����Һ��������Na2S��Na2S2O3��Na2CO3��NaAlO2��Na2SO4������Һ.Ӧѡ��
(A)�ռ���Һ�� (B)���ᡡ��(C)��ˮ����(D)�Ȼ�����Һ
5�� X(��)��Y(��)��Ӧ,�ɷų�����ζ������Z;Z��NaOH��Ӧ�ֵõ�X(��);Z���������ղ���ΪW��,W������ˮ�ֵõ�Y(��).��X(��)��Y(��)��
(A)Na2S��ϡ���ᡡ ��(B)Na2SO3������
(C)Na2S������ ��(D)Na2SO3��ϡ����
6����ȥ������̼�л��е�����������������,��ѡ�õ��Լ���
(A)���������Һ������(B)����������
(C)����С�մ���Һ����(D)ʯ��ˮ
7����������������������Ⱦ���Ǣ�ú��ȼ��;�ڹ�ҵ�����������ŷ�;��ȼ�ű���;�ܷɻ�������β�����ŷ�
(A)ֻ�Т٢ڡ� (B)ֻ�Тڢܡ� (C)ֻ�Т٢ڢ� ��(D)�٢ڢۢ�
8������������Ʊ�����ķ���:�ټ���ϡ������Ҵ��Ʊ���ϩ;�ڼ���ϡ����Ͷ��������Ʊ�����;����ϡ����ʹ���ʯ�Ʊ�������̼;����ϡ������������Ʊ�����.���˲��õķ�������Щ?
(A)ֻ�Тٺ͢� ��(B)ֻ�Тں͢�
(C)ֻ�Тۺ͢� ��(D)�٢ڢۢ�
9���������������������ˮ��Ⱦ����:�ٳ���������ˮ�������ŷ�;��ũҵ������ũҩ������ʹ�ò���;�ۺ�������ʯ��й©;�ܹ�ҵ�����з�Һ���������������ŷ�
(A)ֻ�Т٢ۡ� (B)ֻ�Т٢ܡ� (C)ֻ�Тڢܡ� (D)�٢ڢۢ�
10�����й����������������ȷ����
(A)������������ɸ�����Ӧ
(B)�����������ڳ��³�ѹ�¾�Ϊ��̬
(C)���������ﶼ�Ǽ���������
(D)���ܸ��ᷴӦ��������һ���ܸ��Ӧ
11�����б仯���������仯����
(A) �����ڷŵ������±�ɳ����� (B) ���ȵ����ɰ�ɫ��ˮ����ͭ
(C) Ư�IJ�ñ����������б�� (D)�������������������þ��������
12�����и��������У��ȿ�����Ũ�����ֿ��ü�ʯ�Ҹ������
(A) CO��H2��CH4�� (B) H2��O2��Cl2��(C) CO��O2��H2S��(D)��SO2��NH3��CH4
13����������ķе��ˮ�ߣ����������ֽ⡣ij�Լ������Ƶ�7��8���ù���������Һ����Ũ����30������Һʱ���ɲ������˵ķ�����
�� (A) ��ѹ���� (B) ��ѹ���� (C) ����ʯ�ҳ�ѹ����(D)��ѹ����
14����������ԭ��Ӧ3S��6KOH��K2SO3��2K2S��3H2O�У��������ͱ���ԭ����ԭ����֮��Ϊ
(A)��1��2������(B)�� 2��1���� (C)����1��1������(D)����3��2
15�����и��������У��� Cl2O7 HClO�� �� SO2��H2SO4�� �� NO2��HNO3���� SiO2 H2SiO3���� Mn2O7 HMnO4 ��ǰ���Ǻ��ߵ���������ȷ����
(A)���ڢۡ���(B)���ۢܡ���(C)���ܢݡ� (D)���٢ۢ�
16������������Һ�м�������������Һ���� O2���� Cl2 �� SO2 ��CuSO4����ʹ��ҺPHֵ��С����
(A)���٢ۡ���(B)���ڢܡ���(C) �ڢۢܡ���(D) ��
17���������ǿ�������·ֽ�,���ɰ���������������ˮ.��Ӧ�����ɵ���������ͻ�ԭ��������ʵ���֮����
(A)1:3 ����(B)2:3 ����(C)1:1 ����(D)4:3
18����94ȫ�����������岻����ɴ�����Ⱦ����
(A)�������� (B)��������(C)һ����̼�� (D)һ������
19��п������һ�ְ�ɫ����,����Ҫ�ɷ���������ˮ��п�κͱ���,�����ǡ�
(A)ZnCO3��BaCl2�� (B)ZnCl2��BaCO3
(C)ZnS��BaSO4����(D)ZnCO3��Ba(NO3)2
20�� 24����Ũ��Ϊ0.05Ħ/����Na2SO3��Һ,ǡ����20����Ũ��Ϊ0.02Ħ/����K2Cr2O7��Һ��ȫ��Ӧ,��Ԫ��Cr�ڱ���ԭ�IJ����еĻ��ϼ���
(A)+6�� (B)+3 �� (C)+2�� ��(D)0
21.������,��20�����������ͨ��aĦ�����bĦ��������(a��b����������,��a��5,b��5).��Ӧ��ȫ��,������������ܴﵽ������ܶ�Լ��
(A)24.5��/������B��14.4��/���� (C)8��/�� (D)5.1��/��
������������,�ش�22��23С��.
1995��ŵ������ѧ�������������о������㱻�ƻ��������λ������ѧ��.�����еij�������˳������������,���������ϵ�����.������(��CCl2F2���ڹ�������·ֽ�,����Clԭ��,Clԭ�ӻ�Գ�����������õ��ƻ�����(�����ķ���ʽΪO3).�йط�ӦΪ:
22.������������������ķ�Ӧ������,Cl��
(A)��Ӧ�� (B)������ ��(C)�м���� (D)����
23. O3��O2��
(A)ͬ���칹�� ������ (B)ͬϵ��
(C)����ͬ�������塡��(D)����ͬλ��
24����0��10������0.1Ħ/��BaCl2��Һǡ�ÿ�ʹ��ͬ�����������������п�������������Һ�е������������ȫת��Ϊ���ᱵ����,��������������Һ��Ħ��Ũ��֮����
(A)3:2:2�� (B)1:2:3�� (C)1:3:3�� (D)3:1:1
25������������,�����ᾧˮ����
(A)â������(B)����ʯ�� (C)������ (D)��ʯ��
26����60�������ͭ������Һ100��,��ȴ��20��,����˵����ȷ����
(A)��Һ�������䡡���������� (B)�ܼ����������仯
(C)��ҺΪ������Һ,Ũ�Ȳ��䡡 (D)�о�������,�ܼ���������
27��ij��Һ���н϶��Na2SO4��������Fe2(SO4)3.���ø���Һ��ȡâ��,�ɹ�ѡ��IJ�����:
�ټ�����H2SO4��Һ,�ڼӽ���Na,�۽ᾧ,�ܼӹ���NaOH��Һ,
�ݼ�ǿ���ѽᾧˮ,����.��ȷ�IJ���������
(A)�ڢޢۡ� (B)�ܢޢ٢ۡ� (C)�ܢޢۢݡ�( D)�ڢޢ٢ۢ�
28����50mL 18 mol��L-1H2SO4��Һ�м���������ͭƬ������.��ַ�Ӧ��,����ԭ��H2SO4�����ʵ���
(A)��0.45 mol�������������� (B)����0.45 mol
(C)��0.45 mol��0.90 mol֮�䡡(D)����0.90 mol
29����������Һ�μ�ϡ���ᣬ���ɰ�ɫ�����������μ�ϡ���ᣬ�������ܽ����
(A)Na2SiO3���� (B)BaCl2������ (C)FeCl3������ (D)NaAlO2
30�� 0.05molij������0.8g����һ����������ȫ��Ӧ���õ��ʿ�����
(A) H2�� ��B����O2��(C) K��(D)��Zn
31����100gŨ��Ϊ18mol/L���ܶ�Ϊ��(g/cm3)��Ũ�����м���һ������ˮϡ�ͳ�9mol/L�����ᣬ������ˮ�����Ϊ
(A) ��100mL��(B) ����100mL��(C) ����100mL��(D) ����100/��mL
32��������ء����������������������λ�����������ữ��ˮ�У����![]() ��
��![]()
![]() ����Һ��pH=2.0��������Һ��H2SO4��ȫ����ΪH+��SO
����Һ��pH=2.0��������Һ��H2SO4��ȫ����ΪH+��SO![]() ������K+Ϊ��
������K+��
(A)0.045mol/L�� (B)0.035mol/L��(C)0.055mol/L�� (D)0.040mol/L
33�����������������Ҫԭ�����ŷ�SO2�йص���
(A)���ꡡ�� (B)�⻯ѧ���� ������(C)�����ն� ����(D)����ЧӦ
34����������ƿ���Ϊ���ȼ�����֪25.0mL 0.100 mol��L-1 Na2S2O3��Һǡ�ð�224mL����״���£�Cl2��ȫת��ΪCl�����ӣ���S2O32����ת����
(A)S2�� ��������(B)S ����������(C)SO32����������(D)SO42��
35��Ϊ�˱��������㣬�ɲ�ȡ����Ч��ʩ��
(A)���ٶ���������ŷ�����������(B)���ٺ�Ǧ�������ŷ���
(C)���ٷ��ȴ������ŷ�����������(D)���ٶ�����̼���ŷ���
36���������ʲ����ڡ����п��������ձ�����������
(A) ��������(B)�����������(C) ������̼����(D) ��������
37����״����H2S��O2�������100mL������ȼ��Ӧ����ȫ���������徭����ָ���ԭ��״��ʱ���Ϊ10mL����10mL���������
(A) H2S��SO2����(B)��O2 ���� (C) H2S�� (D) SO3
38�����и������ʵ�ϡ��Һ���Ӧ��������ǰ�ߵ�����ߣ����Ǻ��ߵ���ǰ�ߣ���Ӧ������ͬ����
(A) NaHSO4��Ba(OH)2������ ����(B)��AlCl3��NaOH
(C) NaAlO2��H2SO4��������(D)��Ba(HCO3)2��Ba(OH)2
39����֪��Ȼ������ͬλ����16O��17O��18O�����ͬλ���� H��D����ˮ���ӵ�ԭ�������������Ȼ���ˮһ����
(A) 3�֡���(B)��6�֡���(C)��9�֡� (D)��12��
40�����������ȵ������£�ֻ��һ���Լ��Ϳ��Լ�������李��Ȼ��ء��Ȼ�þ������������������Һ�������Լ���
(A) NaOH����(B)��NH3��H2O����(C)��AgNO3����(D)��BaCl2
41�������������������п����������Һ�ֱ����������Ȼ�����Һ��Ӧ�������ɵ����ᱵ������������Ϊ1�U2�U3����������������Һ�����ʵ���Ũ�ȱ�Ϊ
(A) 1�U2�U3����(B)��1�U6�U9����(C) 1�U3�U3�� (D)��1�U3�U6
42�� 15����NH3��HNO3��H2SO4�Ĺ�ҵ�����У����еĹ�ͬ����
(A) ʹ���������豸�� (B)��ʹ��β������װ��
(C) ʹ��H2��ԭ�ϡ��� (D)��ʹ�ô���
43����NaBr��NaI��Na2SO3���Һ�У�ͨ�롪������������Һ���ɲ�������գ��õ�����ʣ�����ʵ���ɿ�����
(A) NaCl�� Na2SO4������ (B)��NaCl�� NaBr�� Na2SO4
(C)��NaCl�� Na2SO4�� I2�� (D)��NaCl�� NaI�� Na2SO4
44������ʵ������в������������Ӧ��ͼ������ϵ���
(A) NaHSO3��ĩ����HNO3��Һ�С��� (B)��H2S����ͨ����ˮ��
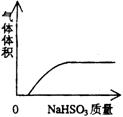 ��������
��������
��������
��������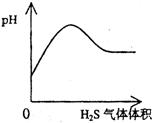
(C)��NaOH��Һ����Ba(HCO3)2��Һ�С�(D)��CO2����ͨ�����ʯ��ˮ��
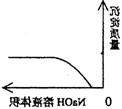 ������������������
������������������
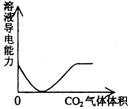
45�����й���Ũ�����������ȷ���ǡ�����������������������������
(A)Ũ���������ˮ�ԣ������ʹ����̿��
(B)Ũ�����ڳ����¿�Ѹ����ͭƬ��Ӧ�ų�������������
(C)Ũ������һ�ָ�������ܹ����ﰱ�������������塡
(D)Ũ�����ڳ������ܹ�ʹ�������Ƚ����ۻ�
46����Ba(OH)2��Һ����������Һ�У�ʹSO![]() ȫ��ת����BaSO4��������ʱ��Ԫ�ص���Ҫ������ʽ�ǡ���������������������������������
ȫ��ת����BaSO4��������ʱ��Ԫ�ص���Ҫ������ʽ�ǡ���������������������������������
(A)Al3+��(B)Al(OH)3 (C)AlO![]() �� (D)Al3+��Al(OH)3
�� (D)Al3+��Al(OH)3
47��ǿ��������������ɷ������·�Ӧ2FeSO4 ����Fe2O3
+SO2��+SO3�������˷�Ӧ���ɵ�����ͨ��BaCl2��Һ�У���������������������������������������
(A)����BaSO3��������(B)����BaSO4����
(C)�ݳ�SO3���塡 ����(D)�ݳ�SO2����
48�� CuS��Cu2S�����������ᣬ���Ǹ������յIJ�����ͬ�����¼���CuS��Cu2S���ֺ�ɫ��ĩ�ķ�����������
(A)��������Ʒ�ֱ��������ᣬ����������������
(B)��������Ʒ�ֱ��������ᣬ������Һ����ɫ
(C)ȡ����ͬ��������Ʒ�ֱ��ڸ������գ�����������������
(D)ȡ����ͬ��������Ʒ�ֱ��ڸ������գ���������������ɫ
49�����и����������Һ���������Լ����Լ������в���������
(A)������̼����������һ����̼��Ʒ����Һ��
(B)�Ȼ��ơ���������̼���ƣ�ϡ���ᣩ
(C)�ƾ������ᡢ�����ƣ�ʯ����Һ��
(D)���ᡢ���ᱵ���Ȼ��أ�̼������Һ��
50������ʱ����pH =2�������м���������������Һ���������Һ�����ֺ�ɫ������Һ������
(A)pH =12 ��Ba(OH)2������������ (B)pH =12�İ�ˮ
(C)0.005mol/L NaOH�������������� (D)0.05mol/LBaCl2
��
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| �� | A | B | D | B | AD | AC | D | D | D | A |
| ��� | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| �� | A | B | C | B | ||||||
| ��� | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 |
| �� | B | D | C | C | B | B | B | A | D | C |
| ��� | 31 | 32 | 33 | 34 | 35 | 36 | 37 | 38 | 39 | 40 |
| �� | A | B | A | D | C | C | C | AD | C | A |
| ��� | 41 | 42 | 43 | 44 | 45 | 46 | 47 | 48 | 49 | 50 |
| �� | B | D | AB | D | D | C | BD | C | A | CD |