�л���ѧ������ߣ��ߣ� ��Ϣ������
1.HCN����������HX��ֻ��ˮ����ﲻͬ����CNˮ��Ϊ��COOH������Xˮ��Ϊ��OH��
������ HCN������ˮ�⡡����CH3OH�������ۺ�
![]()
![]()
![]()
![]() CH3C��CH������ A��������
B��������
C����������
D����
CH3C��CH������ A��������
B��������
C����������
D����
������������������������������ ����
д���йػ�ѧ����ʽ��_______________________________________________________
2.ϩ����ǿ�����������£��ɷ������·�Ӧ��
������ǿ������
![]() ��>C=C<����������
>C=O + O=C<��
��ijϩ��AΪԭ�ϣ���ȡ����������Ĺ������£�
��>C=C<����������
>C=O + O=C<��
��ijϩ��AΪԭ�ϣ���ȡ����������Ĺ������£�
������������������������ ��������
![]()
![]()
![]()
![]()
![]() ��������ǿ�������� B������������
D���� ������������
��������ǿ�������� B������������
D���� ������������
![]()
![]() ����A������������������
��ԭ������������������
HCOOCH(CH3)CH3
����A������������������
��ԭ������������������
HCOOCH(CH3)CH3
![]()
![]()
![]() ���� ��������������C������������
E
���� ��������������C������������
E
��д��A��B��C��D��E�Ľṹ��ʽ��
���������������� NaCN�������������� HCl
![]()
![]()
![]() 3.��֪Br (CH2) Br������ NC(CH2)CN������ HOOC (CH2)COOH
3.��֪Br (CH2) Br������ NC(CH2)CN������ HOOC (CH2)COOH
���������������������������������� ˮ��
����ϩ����������Ϊԭ�Ϻϳɻ�״�л���E ��C6H8O4�����������£�
�������������� ����ˮ������NaCN������ HCl
![]()
![]()
![]() ��������CH2=CH2������
A��������
B��������
C
��������CH2=CH2������
A��������
B��������
C
![]()
![]() ����������������������
NaOHˮ�⡡�� ˮ��
����������������������
NaOHˮ�⡡�� ˮ��
����������������������
![]() ����������������������
D����������������
��������������E����״����
����������������������
D����������������
��������������E����״����
��д��A��B��C��D��E�Ľṹ��ʽ�������������������������� KMnO4
![]() 4.��֪>C=C<�ɱ����Ը��������Һ�����ɶ�Ԫ�����磺CH2=CH2������ HOCH2CH2OH
4.��֪>C=C<�ɱ����Ը��������Һ�����ɶ�Ԫ�����磺CH2=CH2������ HOCH2CH2OH
�������������������������������������������������������� ��[H+]
���Լ���ϩΪԭ�Ϻϳ��л�����D�ͻ�״������E��C8H12O4��
��������CH3�� KMnO4���� ��������������
![]()
![]()
![]()
![]() ����CH2=C-CH3������
A��������
B����������
E
����CH2=C-CH3������
A��������
B����������
E
![]() ������������
��[H+]������������
ŨH2SO4
������������
��[H+]������������
ŨH2SO4
������������������������������ ��ȥ
������������������������������������������ �Ӿ�
![]()
![]() ����������������������������
C��������
D��������
�����
����������������������������
C��������
D��������
�����
������������������������������ CH3OH����
��д��A��B��C��D��E�Ľṹ��ʽ��
5����ά�ڵijɷ�����ϩ������ȩ����������ʯ�͵IJ�ƷΪ��ʼԭ�Ͻ��кϳɡ�������ϩ�������ʹ���ϳɴ�����ϩ��������������
![]() ������CH2=CH2 + 1/2O2
+ CH3COOH��������
CH3COOCH=CH2 + H2O Ȼ���Ӿۡ�ˮ�⡢�����Ƶá���д��������Ӧ��ָ���л���Ľṹ��ʽ��
������CH2=CH2 + 1/2O2
+ CH3COOH��������
CH3COOCH=CH2 + H2O Ȼ���Ӿۡ�ˮ�⡢�����Ƶá���д��������Ӧ��ָ���л���Ľṹ��ʽ��
���������� O2�ʹ��ᡡ �Ӿۡ��� NaOH������ HCHO
![]()
![]()
![]()
![]() ���� CH2=CH2������
A��������
B��������
C����������
D
���� CH2=CH2������
A��������
B��������
C����������
D
������������ ���������������� ˮ�⡡������ ����
(B��C ��D��Ϊ�߷��Ӿۺ���)��
6����ij��״�л������ʽΪC6H12O��������ŵ�������������������Ĺ������������ƣ���֪A�����������ʣ���1������HX���ã�
![]() ����������������������
��2��A��Cu����B������ʽΪC6H10O��
����������������������
��2��A��Cu����B������ʽΪC6H10O��
������������������������������ O2
���������������������� (3) ����ʹBrˮ��ɫ��
���������������������������� ŨH2SO4���� H2��Ni��
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ����������
���������� ��4��A��������
C����������������
����������
���������� ��4��A��������
C����������������
![]()
![]()
![]()
![]() ����������������������������������
OH��H2(Ni)
����������������������������������
OH��H2(Ni)
![]()
![]()
![]()
![]() ����������������������
(5)��������������������
A
����������������������
(5)��������������������
A
![]() ������������������������������
������������������������������
�� ��д��A��B��C���Ľṹ��ʽ��
7.���л���C5H10O3������������ͼ��ʾ��һϵ�з�Ӧ��
���������� ŨH2SO4������ŨH2SO4�� NaOH��Һ
![]()
![]()
![]()
![]()
![]() ���� C5H10O3��������
A��������
B��������
C
���� C5H10O3��������
A��������
B��������
C
![]()
![]()
![]()
![]() ����������
CH3OH��������
����������
CH3OH��������
������ H2SO4������������������������������ ŨH2SO4
������
������E���������������������������������� D
��֪E�ķ���ʽΪC5H8O2����ṹ��������֧����������D��E��Ϊͬ���칹�壬B��ʹBr2ˮ��ɫ����д��A��B��C��D��E��C5H10O3�Ľṹ��ʽ��
8����![]()
![]()
![]()
![]() ͨ������£�����ǻ���ͬһ��̼ԭ���ϵķ��ӽṹ�Dz��ȶ��ģ������Զ�ʧˮ����̼��˫���ṹ���磺��������
��C��OH��������
��C=O + H2O
ͨ������£�����ǻ���ͬһ��̼ԭ���ϵķ��ӽṹ�Dz��ȶ��ģ������Զ�ʧˮ����̼��˫���ṹ���磺��������
��C��OH��������
��C=O + H2O
![]()
![]() ����������������������
������ OH
����������������������
������ OH
�� ������ֻ������ת����ϵ��ͼ��
������������������������ ˮ�⡡���������������� ��
![]()
![]()
![]()
![]()
![]()
![]()
![]() ��������������������
�ڡ�����������
�C�� CH2OH ������
��������������������
�ڡ�����������
�C�� CH2OH ������
![]() ����������
Cl2��������������
ˮ�⡡�� �ݡ����� H+
����������
Cl2��������������
ˮ�⡡�� �ݡ����� H+
![]()
![]()
![]()
![]()
![]()
![]() ������
�١�����������
-CHCl2��������
-CHO��������
��
������
�١�����������
-CHCl2��������
-CHO��������
��
![]() ��������
����A��������
�ۡ�����������
��
��������
����A��������
�ۡ�����������
��
�������������������������� ˮ�⡡������ Na2CO3
![]()
![]()
![]() ��������������������
�ܡ�����������
�ߡ���������
��
��������������������
�ܡ�����������
�ߡ���������
��
��1����������ǡ����������� ��������������Ӧ������A��
![]()
![]() ����2��������ݺ͢�����Ĵ�����ˮ���ɻ�����ᣬ��Ľṹ��ʽ
����2��������ݺ͢�����Ĵ�����ˮ���ɻ�����ᣬ��Ľṹ��ʽ
![]() ����3�������������Ҫ�Ķ���������Ϲ�ҵ�ϳ��û�����ں͢�ֱ�Ӻϳɣ��˷�Ӧ�Ļ�ѧ����ʽΪ
����3�������������Ҫ�Ķ���������Ϲ�ҵ�ϳ��û�����ں͢�ֱ�Ӻϳɣ��˷�Ӧ�Ļ�ѧ����ʽΪ
![]()
![]()
![]() 9.��֪���з�Ӧ���Է�����RCHO + R��COOH������ R��COOCHR������֪���Ͱ�������ˮ�ԣ��롡��������������������������������������������
OH
9.��֪���з�Ӧ���Է�����RCHO + R��COOH������ R��COOCHR������֪���Ͱ�������ˮ�ԣ��롡��������������������������������������������
OH
ˮ���������ƣ���������ˮ���ֿ��Դ�����߰��⡣������ϩΪԭ�Ϻϳ�ά�ڣ�����Ҫ�������£�
![]()
![]() ��������������������������������������������������
D
��������������������������������������������������
D
������������������������������������������ CH3OH
![]()
![]() ��������
O2����
CH3COOH������ �Ӿۡ�������������������
HCHO
��������
O2����
CH3COOH������ �Ӿۡ�������������������
HCHO
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() CH2=CH2������A��������
B����������
C����������
E������
�� ��
CH2=CH2������A��������
B����������
C����������
E������
�� ��
![]()
![]() ������ ����������H2O��������������������������������������
��C5H8O2��n
������ ����������H2O��������������������������������������
��C5H8O2��n
![]() ������������������������������������������
NH3
������������������������������������������
NH3
![]() ��������������������������������������������������
F
��������������������������������������������������
F
��1��![]() ����A�Ļ�ѧ����ʽΪ
����A�Ļ�ѧ����ʽΪ
��2��![]() ��C����D��E�Ļ�ѧ����ʽΪ
��C����D��E�Ļ�ѧ����ʽΪ
��3��E������Ϊ������������������ ά�ڵĽṹ��ʽΪ���������� ����������������
![]()
![]() ��������������������������
��H2
��������������������������
��H2
![]() 10����֪������CH3CHCOOR��������
CH2=CCOOR
10����֪������CH3CHCOOR��������
CH2=CCOOR
![]()
![]()
![]() ����������������
CH3����
������������CH3
����������������
CH3����
������������CH3
������������������������ H2�� CO
![]() ������������
RCH=CH2������������
RCHCHO
������������
RCH=CH2������������
RCHCHO
![]() ��������������������������
��ѹ������ CH3
��������������������������
��ѹ������ CH3
���������� ��MR+27�������������� ��MR+57��
����ֻ��C��H��O�Ļ�����A���� F���й����ǵ�ijЩ��Ϣ���£�
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ��������������
A������H2�� CO��������
B��������
Cu��OH��2������C
��������������
A������H2�� CO��������
B��������
Cu��OH��2������C
![]()
![]()
![]() ������ ������Ϊ82�ġ�����������
�ɷ���������Ӧ������������
�ɱ����к�
������ ������Ϊ82�ġ�����������
�ɷ���������Ӧ������������
�ɱ����к�
����������֧���������� ��ѹ
![]()
![]()
![]()
![]() ��������������������������
����������������������������������
��������������������������
����������������������������������
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ������������
F��������������������
E����������
��H2����������
D
������������
F��������������������
E����������
��H2����������
D
![]()
![]() ������ �߷��ӻ��������������������������������������������
������Ϊ202
������ �߷��ӻ��������������������������������������������
������Ϊ202
![]()
![]()
![]() ��������C10H14O4��n����һ������������������������
������������������
��������C10H14O4��n����һ������������������������
������������������
![]()
![]() ��1��д��������A��E��F�Ľṹ��ʽ��A��������������
E��������������
F
��1��д��������A��E��F�Ľṹ��ʽ��A��������������
E��������������
F
![]() (2)д��B������������Cu��OH��2����Һ��Ӧ�Ļ�ѧ����ʽ
(2)д��B������������Cu��OH��2����Һ��Ӧ�Ļ�ѧ����ʽ
![]() 11���ɱ���������������Ϣ�������ѧ֪ʶ���ش��������⣺
11���ɱ���������������Ϣ�������ѧ֪ʶ���ش��������⣺
�� ����֪�л������е�ϩ���ɷ��������ֽⷴӦ�����磺
���������������������� ��O3
![]() ���� R�DCH=CH�DCH2OH��������
R�DCH=O + O=CH�DCH2OH
���� R�DCH=CH�DCH2OH��������
R�DCH=O + O=CH�DCH2OH
�������������������� ��Zn+H2O
�������������� ���� �ڼ������
![]() ��������
RCO�DCl + R��OH����������
RCOOR��+ HCl
��������
RCO�DCl + R��OH����������
RCOOR��+ HCl
�������з���õ����ɰش��������ʽΪC10H12O3�����Ȳ�����ˮ��Ҳ������̼��������Һ����ͼΪ�ɰش��IJ������ʡ�
![]()
![]()
![]()
![]()
![]()
![]() ��������������������������������
D��������������������
HO�D������
�DCHO
��������������������������������
D��������������������
HO�D������
�DCHO
![]() ����������������������������
C10H11O2Br����������
������������������OCH3
����������������������������
C10H11O2Br����������
������������������OCH3
![]()
![]() ����������������������������������
��Ӧ��
����������������������������������
��Ӧ��
![]()
![]()
![]() ��������������������������������������
O3/Zn+H2O��������������
B (C2H4O2)
��������������������������������������
O3/Zn+H2O��������������
B (C2H4O2)
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ������A����������
Br2/CCl4�������ɰش�
������A����������
Br2/CCl4�������ɰش�
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ����C10H12O3Br2������Ӧ���� C10H12O3������������
COCl���
C (C24H20O5)
����C10H12O3Br2������Ӧ���� C10H12O3������������
COCl���
C (C24H20O5)
�Իش𣺣�1��д��������Ľṹ��ʽ���ɰش������������� B����������C�������� D��
![]()
![]()
![]()
![]() ��2��д����Ӧ���ͣ���Ӧ��������������
��Ӧ��
��2��д����Ӧ���ͣ���Ӧ��������������
��Ӧ��
��3��![]()
![]() д����Ӧ��Ļ�ѧ����ʽ���л���Ҫд�ṹ��ʽ����
д����Ӧ��Ļ�ѧ����ʽ���л���Ҫд�ṹ��ʽ����
![]()
![]() ������������������������������������������
OH�� ˮ�⡡������
OH
������������������������������������������
OH�� ˮ�⡡������
OH
![]()
![]() 12����֪��R�DCO�DR��+ HCN������������
R�DC�DCN����������
R�DC�DCOOH
12����֪��R�DCO�DR��+ HCN������������
R�DC�DCN����������
R�DC�DCOOH
![]()
![]() ������������������������������������������
R�䡡��������������
R��
������������������������������������������
R�䡡��������������
R��
������ͼ�仯���Իش��������⣺
������ HCN������ ˮ�⡡���� ŨH2SO4��������CH3OH����������
![]()
![]()
![]()
![]()
![]() �� A��������
B��������
C����������
D ������������E
���������� F
�� A��������
B��������
C����������
D ������������E
���������� F
![]()
![]() ��C3H6O����������������������������
����������������C5H8O2������C5H8O2��n
��C3H6O����������������������������
����������������C5H8O2������C5H8O2��n
��1��д���л���Ľṹ��ʽA������ B������ C��������D������ E��������F
![]()
![]()
![]()
![]()
![]()
![]() ��2��д�������йط�Ӧ�Ļ�ѧ����ʽ��
��2��д�������йط�Ӧ�Ļ�ѧ����ʽ��
![]() ���� C������D
���� C������D
![]() ���� D������E
���� D������E
13���Ҵ���ŨH2SO4���ڲ����ȵ������¿ɷ�����ˮ��Ӧ��A�����������ڼ��ȡ���ѹ����H2SO4���ڵ������¿ɷ���ˮ����Ӧ��B������Ӧ���ܾ����������м��壨����һ����
�������������������� ���� A
![]() ����������
CH3CH2OH������������
CH2=CH2 + H2O
����������
CH3CH2OH������������
CH2=CH2 + H2O
![]()
![]()
![]()
![]()
![]() ������������������
C������B������E
������������������
C������B������E
�������������� D�������������������� F��������
������������������ CH3�DCH2�DOSO2�DOH
�������������������������� ����
��1���������Ӧ��ȡ�����ӳɡ�����ȥ���࣬��A����F������Ӧ������ĸ�����������¿հף�������ȡ����Ӧ����______ ���ڼӳɷ�Ӧ����_______ ������ȥ��Ӧ����_____
��2����ϵͳ���������м��壨��������
![]() ��3�������ԭ��C2H5OH�е��ǻ��е�H��D��dz�C2H5OD����Ӧ���ŨH2SO4���Ƿ���ܺ���D��Ϊʲô��������֮һ��ˮ���Ƿ���ܺ���D��Ϊʲô��
��3�������ԭ��C2H5OH�е��ǻ��е�H��D��dz�C2H5OD����Ӧ���ŨH2SO4���Ƿ���ܺ���D��Ϊʲô��������֮һ��ˮ���Ƿ���ܺ���D��Ϊʲô��
��4�������� �����ŨH2SO4��D��dz�D2SO4����������֮һ��ˮ���Ƿ���ܺ���D��Ϊʲô��
��5�������� ģ�����ⷴӦԭ����������з�Ӧ�������Ƿ�Ӧ������������ƽ��
![]() ��������3CH3CH2OH
+��HO��3P=O����������
�������� ����������+
��������3CH3CH2OH
+��HO��3P=O����������
�������� ����������+
![]()
![]()
![]()
![]()
![]() ��������2CH3OH
+ HOCH=CCl2 +��HO��3P=O������������������������
���е�η��+
��������2CH3OH
+ HOCH=CCl2 +��HO��3P=O������������������������
���е�η��+
![]()
![]()
![]()
![]() �������ۡ���������
+ ��HO��3P=O����������
��ClCH2CH2O��3P=O����ȼ����+����������������
�������ۡ���������
+ ��HO��3P=O����������
��ClCH2CH2O��3P=O����ȼ����+����������������
NaOH
������������������������������������
![]() 14����֪±������ˮ�ⷴӦ��R�DX + H2O������ R�DOH + HX��X����±ԭ�ӣ���ij��A�Ļ�ѧʽΪC6H8O4Cl2���л���B��C��D��E��ת����ϵ��ͼ��ʾ��
14����֪±������ˮ�ⷴӦ��R�DX + H2O������ R�DOH + HX��X����±ԭ�ӣ���ij��A�Ļ�ѧʽΪC6H8O4Cl2���л���B��C��D��E��ת����ϵ��ͼ��ʾ��
�������������������������������� Cu��OH��2����Cu O2
![]()
![]()
![]()
![]()
![]()
![]()
![]() ����������������������������
B����������
E
����������������������������
B����������
E
���������������� ˮ�⡡C2H3O2Cl
![]() ��������������
A����������������������������������
D��������
��������������
A����������������������������������
D��������
![]() ����������
������ H+������������������������
NaOH
����������
������ H+������������������������
NaOH
![]()
![]() ������������������������������������������
C
������������������������������������������
C
���������������������������������������������� ˮ��
��1��д��A��B��C��D�Ľṹ��ʽ��A�������� B���������� C���������� D
![]()
![]()
![]()
![]() ��2��д��E��B�Ļ�ѧ����ʽ��
��2��д��E��B�Ļ�ѧ����ʽ��
![]() ��3��B������������Һ��ˮ������ữ���Եõ�F��д��F�������۷�Ӧ�Ļ�ѧ����ʽ��
��3��B������������Һ��ˮ������ữ���Եõ�F��д��F�������۷�Ӧ�Ļ�ѧ����ʽ��
15����ҵ���üױ������ԨD�ǻ�������������HO�DC6H4�DCOOC2H5 (һ�ֳ��õĻ�ױƷ������)���������������£���Ӧ����δע������ͼ��ʾ��
![]()
![]()
![]()
![]()
![]()
![]() ����������
Cl2����������
һ�������� CH3�D������CH3I���� CH3�D������HOOC�D
����������
Cl2����������
һ�������� CH3�D������CH3I���� CH3�D������HOOC�D
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() C6H5�DCH3���� ������ A����������������������������������������������
C6H5�DCH3���� ������ A����������������������������������������������
![]()
![]()
![]()
![]()
![]()
![]() ��������
�����١��� �ڡ��������������������ۡ���������������
��
��������
�����١��� �ڡ��������������������ۡ���������������
��
![]()
![]()
![]()
![]() ������������������������������������
�DOH��������������
�DOCH3�� �����DOCH3���� ��
������������������������������������
�DOH��������������
�DOCH3�� �����DOCH3���� ��
![]()
![]()
![]() C2H5OH����������
HI�� HO������
C2H5OH����������
HI�� HO������
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ������������
B��������������������
COOC2H5 ��
������������
B��������������������
COOC2H5 ��
�����ݡ��������� ��
����ͼ��� ��
��1�� �л���A�� �ṹ��ʽΪ������������ ��
![]()
![]() ��2��д ����Ӧ�ݵĻ�ѧ����ʽ���л���д�ṹ��ʽ��ע����Ӧ����������������������
��
��2��д ����Ӧ�ݵĻ�ѧ����ʽ���л���д�ṹ��ʽ��ע����Ӧ����������������������
��
��3��![]()
![]() ��Ӧ�ںܵ͢ķ�Ӧ���ͷֱ���
��Ӧ�ںܵ͢ķ�Ӧ���ͷֱ���
��4��д����Ӧ�۵Ļ�ѧ����ʽ
![]()
![]() ��5���ںϳ���·�У���Ƣۺ͢�������Ŀ����
��5���ںϳ���·�У���Ƣۺ͢�������Ŀ����
16����֪��1��ȩR�DCH2CHO��ȩR��DCH2CHO��һ�������£����ȣ�ȥˮ��õ�ȩ
![]() RCH2CH=C�DCHO����2��±��������������ˮ��Һ��ˮ��������Ӧ�Ĵ��������������ƴ���Һ
RCH2CH=C�DCHO����2��±��������������ˮ��Һ��ˮ��������Ӧ�Ĵ��������������ƴ���Һ
������ R��
�У����ȷ�����ȥ��Ӧ��ȥ±���⣩�����ɲ����͵Ļ����
![]() C6H5�DCHO����������������
D������������������
E�DC9H6O2
C6H5�DCHO����������������
D������������������
E�DC9H6O2
![]()
![]()
![]() ������CH3CHO��������������������
NaOH��Һ
������CH3CHO��������������������
NaOH��Һ
������NaOH��Һ�������� Br2��CCl4��Һ��������H2�� ����
����������ȥˮ
![]()
![]() �� ������������������������
C��������������������
F
�� ������������������������
C��������������������
F
![]() ��������g��NH3��2 +��Һ����������H2������
��������g��NH3��2 +��Һ����������H2������
H2������
B
��֪A��һ�ֿ�����Ϊҩ����л�����������Ӧʽ�и��л�������Ĺ�ϵ���Ʋ��л���A��B��C��D��E��F�Ľṹ��ʽ��A�������� B�������� ��C����������D��������
E�������� F_________
17����������²���֪ʶ����17�⣺
![]() ������������������������������������������
OH
������������������������������������������
OH
![]() �� R1�DC��C�DH + R2�DCHO��������
R1�DC��C�DCH�DR2��R������������ͬ����
�� R1�DC��C�DH + R2�DCHO��������
R1�DC��C�DCH�DR2��R������������ͬ����
�������������������������������� Pd.BaSO4
![]() �� R�DC��C�D��CH2��n�DCH=CH2 + H2��������
R�DCH=CH�D��CH2��n�DCH=CH2
�� R�DC��C�D��CH2��n�DCH=CH2 + H2��������
R�DCH=CH�D��CH2��n�DCH=CH2
�������������������� NaOHˮ��Һ
![]()
![]() ��������������������������������
R�DCH2�DCH�DCH3
��������������������������������
R�DCH2�DCH�DCH3
![]()
![]() �� R�DCH2�DCH�DCH3��������������������
OH
�� R�DCH2�DCH�DCH3��������������������
OH
![]()
![]() ����������
Cl������������������
R�DCH=CH�DCH3
����������
Cl������������������
R�DCH=CH�DCH3
�������������������� NaOH ����Һ
1����4�D��������������������PBT���۶Ա������ᶡ����������Ҫԭ�ϣ�������ͨ����ͼ���ֲ�ͬ�ĺϳ�·���Ʊ�����д����Ӧ���ʵĽṹ��ʽ��
������������������������������ Pd�� BaSO4
![]() ������������������������
�ڡ���������������
��
������������������������
�ڡ���������������
��
![]()
![]() ������������
�����Ӿۺϡ������������� ����H2����������������������������������������������
������������
�����Ӿۺϡ������������� ����H2����������������������������������������������
���������������� H2O
![]() �� �������� ��ʯ��������
�١���������������
��
�� �������� ��ʯ��������
�١���������������
��
![]()
![]() ������������������
HCHO
������������������
HCHO
������������������������ �ޡ��������������� ��
![]()
![]() ������������������
HCHO����������������������
ϡNaOHˮ��Һ
������������������
HCHO����������������������
ϡNaOHˮ��Һ
�ߡ�������������������������������������������
![]()
![]()
![]()
![]() HOCH2��CH2��2CH2OH
HOCH2��CH2��2CH2OH
![]()
![]() ����������������������������������������������
�Ա�������
����������������������������������������������
�Ա�������
�������������������������������������������� �� (PBT)
![]()
![]()
![]() ��д���١�������Ľṹ��ʽ��
��д���١�������Ľṹ��ʽ��
18��±����R�DCL��һ�������¿ɷ������·�Ӧ��
���������������� OH -
![]()
![]() �� R�DCl + KCN��������R�DCN
+ KCl�� R�DCN + 2H2O
+ H+������
R�DCOOH +NH4+
�� R�DCl + KCN��������R�DCN
+ KCl�� R�DCN + 2H2O
+ H+������
R�DCOOH +NH4+
������������������ ��
![]() ������R�DCl + NaOH������R�DOH + NaCl
������R�DCl + NaOH������R�DOH + NaCl
��������������������H2O
����ϩΪԭ�Ͼ�����ͼ��ʾ��Ӧ����ȡ�л���W��A��B��C��D��E��Ϊ���������
�������������������� �ס����� KCN������ H2O
![]()
![]()
![]()
![]()
![]()
![]() ������������������������
A��������
B��������
C
������������������������
A��������
B��������
C
���������������������������� OH-��������H+���������� ŨH2SO4
![]()
![]() ��������CH2=CH2 ���������������������������������������������������� W
��������CH2=CH2 ���������������������������������������������������� W
�������������������� �ҡ�������NaOH , H2O���������������� ��
![]()
![]()
![]() ������������������������
D����������������
E
������������������������
D����������������
E
�������������������������������� ��
(1)������ΪCl2����ΪHCl�����ɵ�W�ķ���ʽΪC8H14O4����W�Ľṹ��ʽΪ��
(2)����W�ķ���ʽΪC5H10O3�����Ϊ����������, ��Ϊ___________
�л���ѧ������ߣ��ˣ���һ����߿Ƽ���ص��л��߷��Ӳ�����
1���������Զ�����Ϊ�����ĵ��Ӽ��������Ҫ����֮һ��Ҫ�ڷ���ˮƽ�����Ʒ��Ӽ���������ӿ���ʮ�ֹؼ���һ�����û�ѧ��Ӧ�ĵ�ؿ��أ���Ӧ���£�
![]()
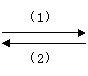
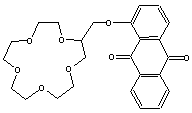
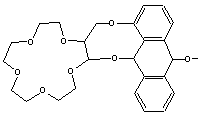
![]() ��Ӧ��1��ʹ�л���A���첲����ͨ��������Ӧ��2��ʹ��Ͽ����Ӷ������л���Ӧ����ʹ��������ڡ������͡��ء�����״̬���Իش��������⣺
��Ӧ��1��ʹ�л���A���첲����ͨ��������Ӧ��2��ʹ��Ͽ����Ӷ������л���Ӧ����ʹ��������ڡ������͡��ء�����״̬���Իش��������⣺
��1���л���A��������״�������������������������������A�ɳ�֮Ϊ�� ��
A����������������B�������ѡ��� C������������������D������ͪ
��2���л���A�ķ���ʽΪ�������������� ��
��3����������Ӧ��ԭ��Ӧ�ĽǶ������������Ӽ��������ʱ�������������� ��Ӧ�������Ӽ�����ػ�ʱ�������������� ��Ӧ��
��4����Ӧ��1���ͣ�2���Ƿ����ڿ��淴Ӧ�������� ����������������������������
������������������������������ ��
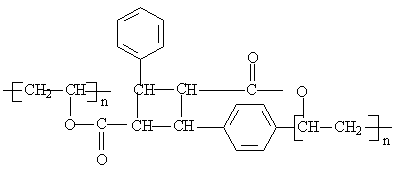 2���й�߷���ʵʩ�������ģ���ɵ�·����ȱ�ٵIJ��ϣ��й�߷������ع��ǻᷢ�����۷�Ӧ�����ɲ����ԵĽ����߷���Ӳ��ģ����δ�йⲿ�����ܼ�������ҩƷϴȥ����������켯�ɵ�·�ȡ����õĸй�߷����о���ϩ��������������й��Ķ��۽����߷��ӽṹ��ʽΪ������ͼ����
2���й�߷���ʵʩ�������ģ���ɵ�·����ȱ�ٵIJ��ϣ��й�߷������ع��ǻᷢ�����۷�Ӧ�����ɲ����ԵĽ����߷���Ӳ��ģ����δ�йⲿ�����ܼ�������ҩƷϴȥ����������켯�ɵ�·�ȡ����õĸй�߷����о���ϩ��������������й��Ķ��۽����߷��ӽṹ��ʽΪ������ͼ����
��1���ڸй�ǰ���ָй�߷��ӣ������ӣ��Ľṹ��ʽΪ���������������������������� ��
��2�������ӵ����ָй�߷��Ӳ��Ͽ�������ᣨC6H5•C3H3O2����һ������Ӧ�����䵥�塣���ƶ�������������������������ϩ������Ļ�ѧ����ʽ������������������������ ��
3�� ��ϩ�DZ���һ��ͬ���칹�壬��ṹ����ͼ��
��ϩ�DZ���һ��ͬ���칹�壬��ṹ����ͼ��
�� ��1�����ƶ���ϩ��һ��ȡ������칹����Ŀ�������� ������ȡ
������칹����Ŀ���������� ��
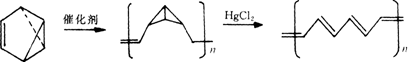 �� ��2�����ִ���ѧ��չ�Ĺ����У���������ϩ�ϳɶ����Ȳ������һ�־����Ӵ����Խṹ�Ĺ�����ϵ����Ϊ���ӵ���ʹ�ã�
�� ��2�����ִ���ѧ��չ�Ĺ����У���������ϩ�ϳɶ����Ȳ������һ�־����Ӵ����Խṹ�Ĺ�����ϵ����Ϊ���ӵ���ʹ�ã�
������
Ϊ�������������Ϊ���ӵ��ߵķ��ӿ��أ����ӿ��ع㷺�������·�չ�ķ��Ӽ�����У������й�˼��Ϊ�����Ī����Six1��Higelin����Ʋ��ϳɵ�Nһ�������л�������ط��ӿ��ء�
 |
�������� ��I���������������������� ����������������������������II��
��ͨ�������жϣ�����������״̬�У���I��ʽ��ʹ��·�����������Ͽ����պϣ�״̬��ԭ������������������������������������ ��
�� ��3�����������������ӵ��ߣ��ֱ������������ṹ���������ϣ�����·���ڱպ�״̬ʱ�����������������ӷ�ʽ��α�ʾ��
4�� 2000��10��10�գ����ʼҿ�ѧԺ��������λ��ѧ����Ϊ�Ե���ۺ���ķ��ֺͷ�չ����ñ����ŵ������ѧ���������ǣ��������������Ǵ�ѧ�İ���-J-�ڸ�������Ϧ�����Ǵ�ѧ�İ���-G-���˵϶��º��ձ�������ѧ�İ״�������1977�꣬�״����ڵ��˷��֣������Ͼ���Ȳ�����ӵ���һ���ʺ���Ȳ��������������е����ԡ�
��1����д������Ȳ�Ľṹ��ʽ������������������ ��
![]() ��2������֪�״�Ӣ��������ɫ�ľ���Ȳ��Ĥ�Ǵ����ķ�ʽ����Ȳ����ṹƬ������ͼ��ʾ��
��2������֪�״�Ӣ��������ɫ�ľ���Ȳ��Ĥ�Ǵ����ķ�ʽ����Ȳ����ṹƬ������ͼ��ʾ��
��д��ͭɫ�ľ���Ȳ��Ĥ˳ʽ����Ȳ�ĽṹƬ�Σ�
�������������������������������������������� ��
![]() ��3������ۺ�����о��ɹ������Է��ӵ���ѧ��Ѹ�ٷ�չ���ƶ����á��ձ��ij�ľ���ڳɹ��ϳ��˾�������״��ʽ�ṹ�ľ���Ȳ������������״��ʽ�ṹ�ľ���Ȳ�Ƿ���������Ƴɵ�������в���ȱ�ٵ���Ȧ�͵������ ������ ��
��3������ۺ�����о��ɹ������Է��ӵ���ѧ��Ѹ�ٷ�չ���ƶ����á��ձ��ij�ľ���ڳɹ��ϳ��˾�������״��ʽ�ṹ�ľ���Ȳ������������״��ʽ�ṹ�ľ���Ȳ�Ƿ���������Ƴɵ�������в���ȱ�ٵ���Ȧ�͵������ ������ ��
��4��������ɫ�ľ���Ȳ��Ĥ��ͭɫ�ľ���Ȳ��Ĥ�Լ��۱���ϩ�Ļ���ﹲ13g������ȫȼ�գ������ĵ����������ɵĶ�����̼�����ܷ�ȷ����Ϊʲô��
����������������������������������������������������������������������������
������������������������������������������������ ��
��5��һ�������Ȳ������ͬ���ʽ���л������Է���������52���÷������ɵ�ʯΪԭ�Ϻϳɵģ����Ǻϳ�ij�����м��壬���ж���ͬ���칹�塣
A������һ����ʽ�ṹ��ͬ���칹��Ľṹ��ʽ������������������������ ����ͬ���칹��ķ����У����е�ԭ���Ƿ����������� �����е�̼ԭ���Ƿ��������� ��
B��������һ��ͬ���칹���ÿ��̼ԭ�Ӿ��ﵽ���ͣ��ҿռ乹����̼��̼֮��ļнǶ���ͬ����ͬ���칹��ķ�����ֱ�Ӽ��ϵ�����̼ԭ�Ӽ�ļн������������� ���뻭
�����Ŀռ乹������������������ ��
��6����һ�������Ȳ������ͬ���ʽ���л������Է���������104��
A�������ʽΪ������������ ��
B�����û�������ӵ�һ�ȴ���ֻ��һ��ͬ���칹�壻����л���Ľṹ��ʽΪ������������ �����Ķ��ȴ�����____��ͬ���칹�壻���ȴ�����_______��ͬ���칹�塣
 C�������л���Ϊ������������ṹ��ʽΪ������������������
���÷����У��Ƿ�����ԭ��һ����ͬһƽ��������������
��
C�������л���Ϊ������������ṹ��ʽΪ������������������
���÷����У��Ƿ�����ԭ��һ����ͬһƽ��������������
��
D��������ҹ�һ������ѧ�Ҳ���ϳ���һ������ըҩ����������������һ������������𣬵�һ�������ͷ������ұ�ը����Ϥ�����������ԵķǺ˱�ըƷ����ըҩ�Ļ�ѧʽ���Կ���B�з��ӵ�����ȡ���ͬ��Ԫ�ص�ԭ���ڷ������Ǻ�������ġ�������ͼ�����л�����ṹ��ʽ�����û��������ըʱֻ����CO2��N2����д���йصĻ�ѧ����ʽ��������������������������
��
�л���ѧ������ߣ��ţ� �л��ۺϲ���
һ��ѡ���⣨����1-10��ֻ��1��ѡ��������⡣11-15����1-2��ѡ��������⡣ÿС��4��,��60�֡���
�ҹ���ѧ����1965��9���������˹������ϳ�ţ�ȵ��ء� Ϊ��֤ʵ�˹��ϳɵ��ȵ�������Ȼ���Ƿ���ͬһ���ʣ����˹��ϳ�ţ�ȵ��ع����в����˷�����14C��Ȼ���˹��ϳɵ�ţ�ȵ�������Ȼ�Ļ�ϵõ��˷�����14C�ֲ����ȵĽᾧ��Ӷ�֤�������߶���ͬһ�����ʣ�Ϊ�ҹ��ڹ��������Ⱥϳɾ����������ţ�ȵ����ṩ������֤�ݡ�
1�����˹��ϳɹ����в��������14C����;��
A. ������������B. ý���ʡ����� C. ���Ԫ�ء�������D. ʾ��ԭ��
2�� ���������˹��ϳɵ�ţ�ȵ�������Ȼ�ᾧ����ͬһ���ʵ�������
A. ��ɢ���á��� B. �����á��� C. ��������ԭ������D. ���ʽṹ��ͬ
3���˹��ϳ�ţ�ȵ��أ�֤���������ĸ������ǿ��ܵ�
A. ����С����ת��Ϊ�л�С���ӡ���B. ���л�С����ת��Ϊ�л��߷���
C. ���л��߷���ת��Ϊ�������ϵ����D. �Ӷ������ϵ�ݱ�Ϊԭʼ����
![]() 4��������������Ҫ�ɷֵĽṹ��ʽ�� -[CH2-O-]n-����ͨ���Ӿ۷�Ӧ�������ĵ�����
4��������������Ҫ�ɷֵĽṹ��ʽ�� -[CH2-O-]n-����ͨ���Ӿ۷�Ӧ�������ĵ�����
����A��(CH3)2O ����������B��CH3CHO ��������C��CH3OH ������D��HCHO
5���ڹ��ʻ��������У�һ����ʹ�õľ۱���ϩ���ϴ����ġ���ɫ��Ⱦ����Ϊͻ�������ֲ������Էֽ⣬�����鷳������о��Ƴ�һ�����͵IJ���������۱���ϩ���������������۶����ɵģ����ֲ��Ͽ�������������·������⣬���й��ھ������˵����ȷ����
A����������һ�ִ������������������ B����ۺϷ�ʽ��۱���ϩ����
C���䵥��Ϊ![]() ������ D����������һ�����߷��Ӳ���
������ D����������һ�����߷��Ӳ���
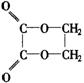 6�����Ҵ�Ϊԭ�ϣ�������6�����͵ķ�Ӧ:������������ȥ���ۼӳɣ�����������ˮ�⣻�Ӿۣ����ϳ��Ҷ����Ҷ���(�ṹ��ʽ����ͼ��ʾ)����ȷ˳����
6�����Ҵ�Ϊԭ�ϣ�������6�����͵ķ�Ӧ:������������ȥ���ۼӳɣ�����������ˮ�⣻�Ӿۣ����ϳ��Ҷ����Ҷ���(�ṹ��ʽ����ͼ��ʾ)����ȷ˳����
A.�٢ݢڢۢܡ�����������B.�٢ڢۢܢ�
C.�ڢۢݢ٢ܡ�����������D.�ڢۢݢ٢ޡ���
7���ۺ���������ɫ��Ⱦ���ĸ��ִ�ʩ�У�����ǰ�����ǡ�
A������������㵹�������������������� B���ȷֽ��������������
C������Ѱ��ֽ����ά����Ʒ������ϡ����� D�� �������ƽ�������
8��1993�������ʮ��Ƽ����ųƣ��й�ѧ����־����������ѧ���¶���ͬ�ϳ�������������̼����ӣ�����1��������1134��̼ԭ�Ӻ�1146����ԭ�ӹ��ɡ����ڴ����ʣ�����˵���������
A�����������B�������³ʹ�̬ C���������ƽ��ʯ��Ӳ�� D���ױ�����
9����������ֻ��һ����ʹ�ã�������������
A�� ������ϩ��B����ȩ��֬��C���ۼ���ϩ�������D���۱���ϩ
10�����в��������ڹ��ܸ߷��Ӳ��ϵ���
�ٸ߷���Ĥ�� ������߷��Ӳ��ϡ� ���������ϡ� ��Һ���߷��Ӳ��ϡ� �ݹ����߷��Ӳ��ϡ������ܸ߷��Ӳ���
A���٢ڢݡ����� B���ڢܢݢޡ���C���ۢܢݡ��� D��ȫ��
11����������ά����K����ֹѪ���ã�����ͨ�����������������Ƶã���Ӧ�г����������������÷�Ӧ���ȣ��ɱ�ʾΪ��
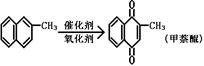
��ij�κϳɷ�Ӧ�У���1.4g(0.01mol)�Ħ������������Ƶ�0.17g(0.001mol)����������֪�÷�Ӧ�������ǿ�ġ����жϵ�������ʵ͵�ԭ����
A��ʹ���˹����Ĵ����������� B��û�������ᣬ����ʹ����������
C���ѷ�Ӧ�������ȡ��������� D�������ɵļ����dz�����
12�������йظ߷��ӻ��������ʵ���������ȷ����
A��һ��������õľ�Ե�ԡ������������� B����������ˮ���������л��ܼ�
C���������ȣ����Ⱥ���ۻ��ı�ԭ����״��D��һ���ͬ��������ǿ�ȴ�
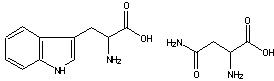 13����ͼΪ���ְ�����Ľṹʾ��ͼ��������ͨ���ļ��γɶ��ģ����γɵĶ��Ĺ��м��ֽṹ
13����ͼΪ���ְ�����Ľṹʾ��ͼ��������ͨ���ļ��γɶ��ģ����γɵĶ��Ĺ��м��ֽṹ
A��2�� B������C������D������
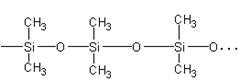 14��������Ҫ�ɷ�����ͼ��ʾ�����ɶ��ȶ������龭
14��������Ҫ�ɷ�����ͼ��ʾ�����ɶ��ȶ������龭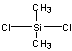 ���ַ�Ӧ�Ƴɵģ������ַ�Ӧ��
���ַ�Ӧ�Ƴɵģ������ַ�Ӧ��
A����ȥ���Ӿۡ� B��ˮ�⡢���ۡ� C�����������ۡ� D��ˮ�⡢�Ӿ�
15���ص����飨CH2N2�������������ʷ�Ӧ��R-COOH+CH2N2��R-COOCH3+N2�����������������ص����鷴Ӧ�����ﲻ��������
A��H-CHO�� B��C6H5OH�� C��C6H5CH2OH�� D��C6H5COOH
������ռ����(��29��)
16����6�֣��л���ķ���ʽΪC6H12N4��������ÿ��Nԭ�ӷֱ�������Cԭ�Ӽ��ϣ���ÿ��Cԭ�ӷֱ�������Nԭ�Ӽ��ϡ�������û��C��C˫����C��C��������д�����л���Ľṹ
��ʽ�ߣߣߣߣߣߣߣ��÷������Уߣߣߣ߸���Ԫ����ÿ����Ԫ��ռ�Уߣߣߣ߸���ԭ�ӡ�
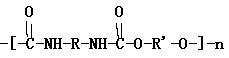 17. ��4�֣��۰�������������-NHCOO-�ظ���Ԫ��һ�����߷��ӻ�����䵥��������������O=C=N-R-N=C=O���Ͷ�Ԫ������HO-R��-OH������߾���ṹʽ����ͼ��ʾ��
17. ��4�֣��۰�������������-NHCOO-�ظ���Ԫ��һ�����߷��ӻ�����䵥��������������O=C=N-R-N=C=O���Ͷ�Ԫ������HO-R��-OH������߾���ṹʽ����ͼ��ʾ��
��1�����������������Ͷ�Ԫ���ϳɸ߾���ķ�Ӧ������ ������ ��Ӧ����Ӿۡ��������ۡ�����
��2��д����2��6-��������������������ͼ��ʾ����1��3-������Ϊ�������ɸ߾���Ļ�ѧ����ʽ��
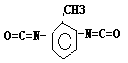
������������������������������������������������ ��
18��(8��)�л�����Խ��п����ۺϡ�����![]() �ɽ��п����ۺ�����-��-CH2-CH2-O-��-n
�ɽ��п����ۺ�����-��-CH2-CH2-O-��-n
��д�����л�״�����↑���ۺ��γɵĸ߷��ӻ�����Ľṹ��ʽ:
(1) 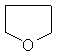 ����������������������������������
����������������������������������
(2) 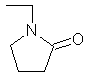 ������������������������������ ��
������������������������������ ��
19����11�֣�������±��X2�뱽��ͬϵ��ķ�Ӧ��±������ɽ������Ʒ�Ӧ����1��3��5�����ױ��������ķ�Ӧ�����ǵķ�Ӧ�������м��壨����һ�����м��壨��Ϊ��ɫ���壬�۵㣭15�棬�����ɸ�����BF4����һ����Ԫ������������ɵģ��������������ƽ�������ڳ���*��̼ԭ�������������ɻ���̼ԭ���ϣ�����ͼ�������ߡ�
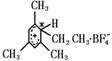
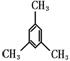
+ CH3CH2F + BF3![]() ����
����![]()
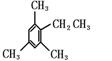
(��)
+ HF +BF3
(��)
��1�� �ӷ�Ӧ���Ϳ�����ӦA�������������� ����ӦB�������������� ��ȫ������������������ ��
��2���м��壨���л�*�ŵ�̼ԭ�ӵ����幹�������л������л�*��̼ԭ�ӽӽ����ǣ�������
A��*CH��CH�� B��CH3*CH2CH3����C����![]() �� D
�� D ![]()
��3��ģ�����⣬������з�Ӧ������д�м��壬�����Ƿ�Ӧ��������Ҫ����ƽ����
�١�![]() +
+ ![]() ������
������
�� ![]() ��������+��CHCl3�� ������
��������+��CHCl3�� ������
�ۡ�![]() + ���������� ������
+ ���������� ������![]() ��+
HBr
��+
HBr
���������ƶϣ���11�֣�
20�� CH3COCH3![]() (CH3)3COMgBr
(CH3)3COMgBr![]() (CH3)3COH
(CH3)3COH
![]() (CH3)3CMgBr
(CH3)3CMgBr![]() A
A![]() B
B![]() C + D
C + D
�� D![]() E����
D
E����
D![]() F + G
F + G
�Ա�ͪ�ȳ����л���Ϊԭ�ϣ���������Ӧ�ܺϳɴ�B��B����ȥ1����ˮ�õ�����ϩ��C��D��H������ռC80%��Dռ20%��H�������Ͷ�δ�г���C�ij�������E���ܷ���������D�ij�������F�ܷ�������������1gF���ɵý�����14.4g��G��Cl2�ڹ����·�Ӧʱ���ɵ�����ͪ��һ��ȡ���
(1).��8�֣�д���������ʵĽṹ��ʽ��
A�������������� ��B���������������� E�������������� ��G_______________
(2).��3�֣���һ������ʽ��ʾBת��ΪC��D�ķ�Ӧ��
______________________________________________________