普通高等学校招生全国统一化学考试5
理科综合能力测试(全国卷Ⅲ)
(化学部分)
6.下列分子中含有的电子数目与HF相同,且只有两个极性共价键的是
A.CO2 B.N2O C.H2O D.CH4
7.久置空气中会发生颜色变化,但颜色变化不是由于跟氧气反应引起的物质是
A.过氧化钠固体 B.亚硫酸钠固体 C.硫酸亚铁晶体 D.苯酚晶体
8.若1.8 g某金属跟足量盐酸充分反应,放出2.24L(标准状况)氯气,则该金属是
A.Al B.Mg C.Fe D.Zn
9、有一种白色粉末由等质量的两种物质混合而成,分别取适量该白色粉末置于三支试管中进行实验。
(1)逐滴加入6 mol・L-1盐酸,同时不断振荡试管,有气泡产生,反应结束后得到无色透明溶液
(2)加热试管中的白色粉末,试管口有水滴凝结
(3)逐滴加入6 mol・L1硫酸,同时不断振荡试管,有气泡产生,反应结束后试管中还有白色不溶物
下列混合物中符合以上实验现象的是
A.NaHCO3、AgNO3 B.BaCl2、MgCO3
C.NH4HCO3、MgCl2 D.CaCl2・6H2O、Na2CO3
10.心酮胺是治疗冠心病的药物,它具有如下结构简式:
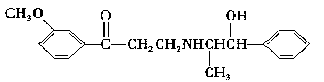
下列关于心酮胺的描述,错误的是
A.可以在催化剂作用下和溴反应 B.可以和银氨溶液发生银镜反应
C.可以和氢溴酸反应 D.可以与浓硫酸和浓硝酸的混合液反应
11.1体积pH=2.5的盐酸与10体积某一元酸强碱溶液恰好完全反应,则该碱溶液的pH等于
A.9.0 B.9.5 C.10.5 D.11.0
12.反应2SO2+O2![]() 2SO3经一段时间后,SO3的浓度增加了0.4 mol・L-1,在这段时间内用O2表示的反应速率为0.04 mol・L-1・s‑1,则这段时间为
2SO3经一段时间后,SO3的浓度增加了0.4 mol・L-1,在这段时间内用O2表示的反应速率为0.04 mol・L-1・s‑1,则这段时间为
A.0.1 s B.2.5 s C.5 s D.10 s
13.某温度下在密闭容器中发生如下反应:2M(g)+N(g)![]() 2E(g)
2E(g)
若开始时只充入2 mol E(g),达到平衡时,混合气体的压强比起始时增大了20%;若开始时只充入了2 mol M和 1 mol N的混合气体,达到平衡时M的转化率为
A.20% B.40% C.60% D.80%
14.下列分子中,所有原子的最外层均为8电子结构的是
A.BeCl2 B.H2S C.NCl3 D.SF6
15.以mD 、mp 、mn分别表示氘核、质子、中子的质量,则
A.mD=mp+mn B.mD=mp+2mn C.mD>mp+mn D.mD<mp+mn
26.下图表示制备无水盐E的主要步骤:
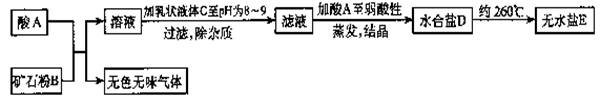 已知B是石灰石,D盐含有约49%的结晶水,无水盐E可用作干燥剂。取少量E溶于水向其中滴加硫酸后,再滴加硝酸银溶液,有白色沉淀F生成。
已知B是石灰石,D盐含有约49%的结晶水,无水盐E可用作干燥剂。取少量E溶于水向其中滴加硫酸后,再滴加硝酸银溶液,有白色沉淀F生成。
填写以下空白(写出化学式或名称):
A ,C ,D ,E ,F 。
27.芳香化合物A、B互为同分异构体,B的结构简式是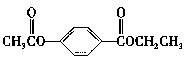 。A经①、②两步反应得C、D和E。B经①、②两步反应得E、F和H。上述反应过程、产物性质及相互关系如图所示。
。A经①、②两步反应得C、D和E。B经①、②两步反应得E、F和H。上述反应过程、产物性质及相互关系如图所示。
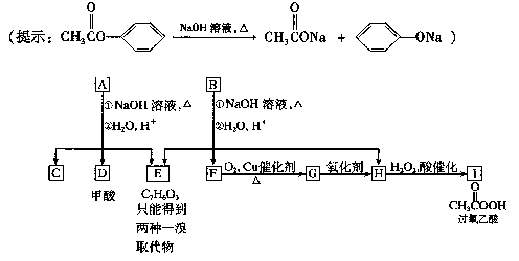
(1)写出E的结构简式 。
(2)A有2种可能的结构,写出相应的结构简式:
。
(3)F和小粒金属钠反应的化学方程式是 ,实验现象是
,反应类型是 。
(4)写出F在浓H2SO4作用下在170℃发生反应的化学方程式:
,实验现象是
,反应类型是 。
(5)写出F与H在加热和浓H2SO4催化作用下发生反应的化学方程式:
,实验现象是 ,反应类型是 。
 (6)在B、C、D、F、G、I化合物中,互为同系物的是
。
(6)在B、C、D、F、G、I化合物中,互为同系物的是
。
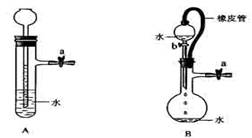
28.根据下图及描述,回答下列问题:
(1)关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示。试判断:A装置是否漏气?(填“漏气”、“不漏气”或“无法确定”) ,判断理由: 。
(2)关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直到全部流入烧瓶。试判断:B装置是否漏气?(填“漏气”、“不漏气”或“无法确定”) ,判断理由: 。
29.A、B、C、D、E分别代表五种微粒,每种微粒中都含有18个电子。其中A和C都是由单原子形成的阴离子,B、D和E都有是分子;又知在水溶液中A跟B反应可生成C和D;E具有强氧化性。请回答:
(1)用化学符号表示上述5种微粒:
A ,B ,C ,D ,E 。
(2)在水溶液中A跟B反应的离子方程式是: 。