几何在化学中的应用
数学科《考试说明》中指出:“数学科考试的宗旨是:测试中学数学逻辑基础知识、基本技能、基本思想和方法,考查逻辑思维能力、运算能力、空间想象能力以及分析问题解决问题的能力。”空间想象能力作为四大考查能力之一,可见其重要性,每年的高考试题立体几何知识占35分左右。同时《考试说明》中又指出“知识的综合性,则是从学科的整体高度考虑问题,在知识网络交汇点设计试题。”尤其是高考科目设置和改革,“3+X”的综合科目的设置,为这一目标的实现提供了大量的机会。本文拟就几何知识在化学中的应用谈几点建议。
一、 重视正多边形在化学中的应用
平面几何中的正多边形都有很好的性质,一些规则的晶体结构就是正多边形。
【例一】
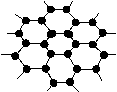 石墨晶体中的每一层
石墨晶体中的每一层
为正六边形的平面网状结构(如图),
则每个正六边形平均分占多少个碳原子?
平均分占多少个化学键?
【解析】每个碳原子为三个六边形所共有,
故每个碳原子对每个六边形的贡献只有1/3,则每个正六边形所占的碳原子数为6![]() =2,又因为每条边(即一个C-C单键)为两个环所共有,则每一条边对每个环的贡献也只能算1/2,于是就有6
=2,又因为每条边(即一个C-C单键)为两个环所共有,则每一条边对每个环的贡献也只能算1/2,于是就有6![]() =3。即每个环分占三个化学键。
=3。即每个环分占三个化学键。
在平面图形的化学晶体中,要注意的是一种网络结构。
二、 重视正多面体在化学中的应用
立体几何中共有五种正多面体:正四面体、正方形、正八面体、正十二面体、正二十面体,它们都有很好的性质。化学中的很多晶体结构都是正多面体的网络结构,要很好的解决空间构型题,就必须有很好的空间想象能力。
【例二】 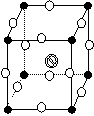 如右图为超导领域里一种
如右图为超导领域里一种
化合物:钙钛矿晶体结构,该结构是具
有代表性的最小重复单元,该晶体结构中,
元素氧、钛、钙的个数比为多少?(其中
![]() 代表氧原子, 代表钙原子, 代表钛原子。)
代表氧原子, 代表钙原子, 代表钛原子。)
 【解析】将晶胞放入整个晶体中考虑,一个氧原子为四个晶胞所共有,所以一个晶胞上有氧原子为12
【解析】将晶胞放入整个晶体中考虑,一个氧原子为四个晶胞所共有,所以一个晶胞上有氧原子为12![]() =3个,每个钛原子为八个晶胞所共有,所以一个晶胞占有钛原子为8
=3个,每个钛原子为八个晶胞所共有,所以一个晶胞占有钛原子为8![]() =1个,一个钙原子为一个晶胞所有,所以一个晶胞占有钙原子一个,因此O:Ti:Ca=3:1:1。
=1个,一个钙原子为一个晶胞所有,所以一个晶胞占有钙原子一个,因此O:Ti:Ca=3:1:1。
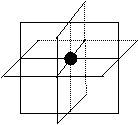
此题的关键在于空间想象能力,
要知道所给图形仅为一个单元而已,
在考虑一个钛原子为八个晶胞所共有
时,可用右图说明其空间结构,发挥好空间想象,就能较好地解决问题。
【例三】 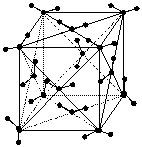 结合下左图分析,干冰晶体中,每个CO2分子周围距离相等且最近的CO2分子数目为( )
结合下左图分析,干冰晶体中,每个CO2分子周围距离相等且最近的CO2分子数目为( )
(A)6, (B)8, (C)10, (D)12。
![]() (图中 代表CO2分子)
(图中 代表CO2分子)
【解析】展开你的空间想象的翅膀吧,
我们仍用一个右下图来说明问题。
就一个面的对角线上的CO2分子而言,
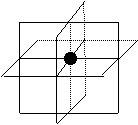 三个互相垂直的且过CO2分子的切面,每
三个互相垂直的且过CO2分子的切面,每
个面的是距离最近的CO2分子数有4个;
故共有4![]() 3=12个。故选(D)
3=12个。故选(D)
若用一个角上的CO2分子来考虑,
则比较麻烦,因为一个角上的CO2分
子为八个晶胞所共有,需考虑八种情况
这时有3+2+2+5![]() 1=12个。
1=12个。