高三月考理科综合化学部分卷
(化学部分)
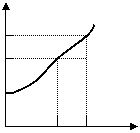
6.有一种盐A,它的溶解度曲线如图一。现有盐A的溶液,其组成处于图中的 P 点,试根据图中的信息分析判断,下列说法中错误的是(已知盐A的晶体不含结晶水) ( )
|
A.把该溶液温度降低 20 ℃,该溶液可变为 50
饱和溶液 40 ・P
B.50℃时,向溶液组成为 P 的A盐溶液加
![]() 入 10gA盐,溶液可变为饱和溶液
入 10gA盐,溶液可变为饱和溶液
C.从图判断: 50 ℃时,若配成盐A的饱和
溶液,则其质量分数约为33.3%
D.50℃时,若组成为 P 的A盐溶液含 Bg A盐, 则加入 B/4 g A盐,溶液即变为饱和溶液
7.地处重庆市开县高桥镇的川东北气矿一矿井12月23日22时左右发生天然气“井喷”,事故发生后,当地医疗机构立即投入到紧张的抢救治疗工作中。目前的治疗方案主要是保证治疗室通风,为病人提供充足的氧气,必要时采用呼吸机。对于肺部感染的病人,对症采用美兰、细胞色素C、阿脱莫兰或某化学物质等药物进行静脉滴注。某化学物质可能是( )
A.NH4Cl B.KCl C.Na2S2O3 D.NaOH
8.最近,科学家用一种称为“超酸”的化合物H(CB11H6Cl6)和C60反应,使C60获得一个质子,得到一种新型离子化合物[HC60]+[CB11H6Cl6]-。该反应看起来很陌生,其实在反应类型上可以跟中学化学里某个熟悉的化学反应相类似。该化学反应是
![]() A.H2O+CH3COOH H3O++CH3COO-
A.H2O+CH3COOH H3O++CH3COO-
B.Zn+2HCl ZnCl2+H2↑
C.CO2+2NH3 CO(NH2)2+H2O
D.NH3+HCl NH4Cl
9.已知NH3和HCl都是能用来作喷泉实验的气体,若在同温同压下用体积不等的烧瓶各收集满NH3和HCl气体,喷泉实验后(假设溶液充满整个烧瓶)二个烧瓶中溶液的关系是
A.溶质的物质的量浓度相同,溶质的质量分数不同
B.溶质的质量分数相同,溶质的物质的量浓度不同
C.溶质的物质的量浓度和溶质的质量分数都不同
D.溶质的物质的量浓度和溶质的质量分数都相同
10.下列离子方程式的书写正确的是:( )
A.漂白粉溶液中通入SO2气体 Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
B.苯酚钠溶液与FeCl3溶液混合 3C6H5O-+Fe3++3H2O=3C6H5OH+Fe(OH)3↓
![]() C.NaHS水解
HS-+H2O
S2-+H+
C.NaHS水解
HS-+H2O
S2-+H+
D.过量的NH4HSO4溶液与Ba(OH)2溶液反应 2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
11.在下图的甲、乙两个装置的烧瓶中盛有同一种红棕色气体M,用弹簧夹夹住橡皮管,烧杯中盛有水.向甲烧杯中加入X,甲烧瓶中气体颜色变浅;向乙烧杯中加入Y,乙烧瓶中气体颜色变深;下列关于气体M与X、Y的组合正确的是( )
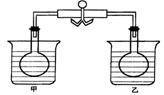
| A | B | C | D | |
| M |
|
|
|
|
| X | NaOH固体 | 硝铵固体 | 冰块 | 碱石灰 |
| Y | 无水乙醇 | 生石灰 | 浓硫酸 | 醋酸铵 |
12.在1 L 0.2 mol・![]() NaOH溶液中通入标准状况下的
NaOH溶液中通入标准状况下的![]() 4.48 L,完全反应后,则下列关系式中正确的是( ).
4.48 L,完全反应后,则下列关系式中正确的是( ).
A.![]()
B.![]()
C.![]()
D.![]()
![]() 13.摄影胶卷上涂布的感光物质主要是AgBr。照相时,在快门按动的一瞬间,进入相机的光使AgBr发生了分解反应:2AgBr
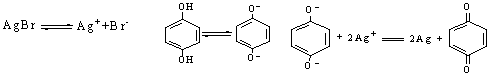
2Ag+Br2。由于进光量极少,分解出的Ag极少,所以必须通过化学反应进行显影才能看到底片上的影像。对苯二酚是一种常用的显影剂,在显影时发生了如下变化:下列关于显影过程的叙述正确的是:( )
13.摄影胶卷上涂布的感光物质主要是AgBr。照相时,在快门按动的一瞬间,进入相机的光使AgBr发生了分解反应:2AgBr
2Ag+Br2。由于进光量极少,分解出的Ag极少,所以必须通过化学反应进行显影才能看到底片上的影像。对苯二酚是一种常用的显影剂,在显影时发生了如下变化:下列关于显影过程的叙述正确的是:( )
 |
![]()
A.在显影过程中 是还原剂
B.在显影液中加入一定量Na2CO3,可加快显影速度
C.溶于显影液的O2能加快显影速度
D.曝光时产生的微量Ag在显影时起了催化作用
26. (16分) (1)下面A~F是中学化学实验中常见的几种仪器:
A量筒 B容量瓶 C滴定管 D托盘天平 E玻璃棒 F坩埚
①其中仪器上标示出仪器的使用温度的是___________________(填写编号);
②能够用于精确量取液体体积的是_____________(填写编号);
③称取 10.5 g固体样品(1 g以下使用游码)时,将样品放在了天平的右盘,则所称样品的实际质量为_____g.
(2)①实验室要用98%(ρ =1.84g・cm-3)的硫酸配制3.68mol・L-1的硫酸溶液500mL需准确量取98%的硫酸________________mL;
②准确量取一定体积的98%的硫酸之后,要配制成3.68mol・ L-1的硫酸溶液500mL,还必须用到的实验仪器是(填写序号)__________________.
A 500mL量筒 B 烧杯 C 1000mL容量瓶 D 500mL容量瓶
E 托盘天平 F 胶头滴管 G 锥形瓶 H 玻璃棒
J酸式滴定管
③若配制3.68mol・L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,将使 所配制的硫酸溶液浓度偏低的是____________________________.
A.在烧杯中稀释浓硫酸后,立刻转移入容量瓶定容
B.将烧杯内的稀硫酸向容量瓶中转移时,因操作不当使部分稀硫酸溅出瓶外.
C.用胶头滴管向容量瓶中加水时溶液凹液面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切
D.用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切.
27.(15分)合金A由4种单质组成,经过一系列反应分别进入了沉淀或气体中.
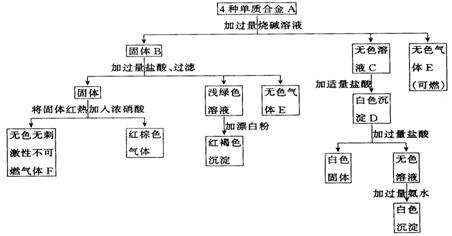 |
试回答:
(1)合金A由哪4种元素的单质组成?_________、________、________、_________.
(2)写出固体B、溶液C、沉淀D和气体E、F有关组成的化学式:
B_________、C_________、D_________、E_________、F_________.
(3)写出合金A中的有关组成与过量烧碱溶液反应生成无色气体E的化学反应方程式: ______________________________________.
(4)写出向无色溶液C加适量盐酸生成白色沉淀D有关反应的离子方程式:
__________________________________________________________________________.
28.(15分)已知两个羟基同时连在同一碳原子上的结构是不稳定的,它要发生脱水反应:
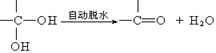
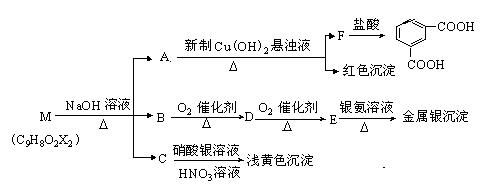 |
现有分子式为C9H8O2X2(X为一未知元素)的物质M,可在一定条件下发生上述一系列反应试回答下列问题:
⑴ X为 (填元素 符号);
⑵A中所含的官能团为 ,上述转化中其中属于氧化反应的共有 步(填数字);M与NaOH溶液共热反应的所属类型是 反应。
⑶ M的结构简式为 。
⑷写出下列反应的化学方程:
①B→D ;
②D在一定条件下发生加聚反应: ;
③E和银氨溶液反应的化学方程式: 。
29.(14分)某复盐的组成可表示为:![]() ,R为-2价含氧酸根.为了确定该盐的组成,进行如下实验:
,R为-2价含氧酸根.为了确定该盐的组成,进行如下实验:
(1)准确称取4.02 g样品加热到失去全部结晶水,冷却后称量,质量为2.94 g.
(2)将剩余固体溶于适量水,滴加盐酸,无现象,再滴加足量![]() 溶液,产生白色沉淀.过滤,将沉淀烘干,称质量为4.66 g.
溶液,产生白色沉淀.过滤,将沉淀烘干,称质量为4.66 g.
(3)向上述溶液中加入过量NaOH溶液,产生白色沉淀,过滤,将沉淀烘干,称质量为0.58g,再将固体高温灼烧后冷却,称得剩余固体质量是0.40 g.
请通过计算回答下列问题:
(1)确定R的化学式. R的化学式______________.
(2)求x、y、z的值. x=________,y=________,z=_________.
(3)确定A是什么元素. A元素的名称是_____________.
(4)该复盐的化学式为______________.
(5)要确定某化合物是否含A元素,最简单方法是______________.
化学部分参考答案
| 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | ||
| C | C | D | A | D | B | B | A |
26.(1)①A B C ②C ③9.5g
(2)①100ml ②BDFH ③BC
27.(1)Mg ![]() C
C ![]() MgO CO
MgO CO
|
28.(1)Br ② (醛基),4,取代(水解)
 |
(3)
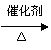 |
(4)①2CH3OH +O2 HCHO +2H2O
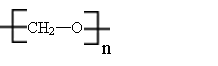
![]() ②nHCHO
②nHCHO
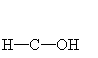 | |||
③ +2Ag(NH3)2OH (NH4)2CO3 + 2Ag +2NH3 +H2O
29.(1)由于向溶液中滴加盐酸,无现象,再滴加![]() 溶液,产生白色沉淀.所以,R必定是硫酸根;R的化学式为
溶液,产生白色沉淀.所以,R必定是硫酸根;R的化学式为![]()
(2)4.02 g样品中含结晶水的物质的量为![]()
4.02 g样品中含硫酸根的物质的量为![]()
![]()
![]()
b+34 18 18
0.58 g (0.58-0.40)g
解得 b=24,∴ B是镁元素
4.02 g样品中含硫酸镁的物质的量为![]()
4.02 g样品中含另一种硫酸盐的物质的量为0.02 mol-0.01 mol=0.01 mol
x∶y∶z=0.01∶0.01∶0.06=l∶1∶6
∴ x=1;y=1;z=6
(3)A的原子量为![]() ,∴ A是钾元素
,∴ A是钾元素
A元素的名称是钾
(4)复盐的化学式为![]()
(5)焰色反应