《生活和生产中常见有机物》专题复习及其强化训练
朱敬华 湖北公安教研室434300(供新教材用)
1.《考试大纲》的要求
(1)了解有机物的主要来源。了解石油化工、农副产品化工、资源综合利用及污染和环保的概念。
(2)了解在生活和生产中常见有机物的性质和用途。
(3)以葡萄糖为例,了解糖类的基本组成和结构,主要性质和用途。
(4)了解蛋白质的基本组成和结构,主要性质和用途。
(5)初步了解重要合成材料的主要品种的主要性质和用途。理解由单体进行加聚和缩聚合成树脂的简单原理。
2.题型与考查方式
最近几年理综综合能力测试利用新材料、医药、农药、环境、社会、生活方面的内容或研究成果作背景材料作为载体,考查有机化学基础知识的题型逐渐丰富起来。生活中的有机物涉及的内容主要有:石油、煤、天然气、油脂、糖类、氨基酸、蛋白质及合成高分子化合物等,这些内容既是学生从理论上学习的内容,又与学生的生活联系紧密。由于高考命题注重理论联系实际,靠近学生生活。因此,在近几年的高考试题中这一部分成为高考命题的新热点。在学科内综合中,由于糖类是多官能团化合物,在题目设计中能体现所有有机物官能团的性质,在连续四年的高考试题中都将该部分内容作为命题素材;又由于这部分内容与生物联系密切,在高考试题这一部内容连续四年出现了学科间综合试题(生物与化学两个学科间)。这一部分在命题时往往与烃和烃的衍生物相联系,主要考查这些有机物中官能团的性质和转化。
主要为框图推断题,是这几年的重点题型。常以新情境题形式出现,它能把有机部分所有重点及主干知识,如结构、性质包容在题中,达到既考查基础知识,又使学生了解有机化学与现代社会发展和科学进步的贡献的目的。
3.复习重难点
重点:1、《烃》《烃的衍生物》《糖类油脂蛋白质》《合成材料》章节中与能源、交通、医疗、环境等方面的结合点;2、适当关注有机方面的前沿科技成果,特别是近些年诺贝尔化学、医学奖方面的内容
难点:与生活生产紧密联系的相关综合应用各类化合物的不同性质的信息题思路和解题方法的训练,着力点放在有机合成和有机推断上。应该特别注意定性和定量结合即带计算因素的推断题,也要注意无机与有机结合的一些试题
4.注意事项
从调研考试及近几年高考评卷场反馈的信息来看,本专题学生在试卷上易出现的主要问题有:①结构简式、结构式、分子式、最简式混写;②专用名词出现错字:如,苯写“笨”、“酯”和“脂”混用等;③有机化学反应方程式中常忘记写无机小分子:如酯化反应的H2O、醛催化氧化成酸多加上H2O等;④有机化学反应中的重要的条件不对或不全(如卤代烃消去写成浓H2SO4、△)、不准确(如水浴加热用“△”代替;“→”写成“=”,“↑”、“↓”不写)、不配平(如醇、醛的催化氧化、银镜反应);⑤不会写麦芽糖、淀粉、纤维素、尿素的分子式。除此而外,其余地方有机物一般都是用结构简式却写成分子式。经常发现的有的同学把物质推断出来了,但由于平时习惯未养成,将结构简式、化学反应方程式书写不正确而丢分,非常可惜。
在解题时要注意:生活中常见几个较复杂有机物分子式、结构简式的书写(如葡萄糖、麦芽糖、淀粉、纤维素等);几个典型代表物在化学反应过程中的相互转化(由多糖转化成低聚糖、单糖、简单有机物和二氧化碳,纤维素的几个主要性质反应等)。
5.经典题型
(1)常识性知识
例题1 2000年理科综合高考试题(全国卷)5题:
尿素是第一个人工合成的有机物,下列关于尿素的叙述不正确的是
A.尿素是一种氮肥 B.尿素是人体新陈代谢的一种产物
C.尿素能发生水解反应 D.尿素是一种酸性物质
例题1是一道学科间综合试题,考查生物、化学和生活常识性知识,尿素的化学式为CO(NH2)2,它是一种肥效高的氮肥,人体新陈代谢过程中排出的尿液中含有尿素,根据其化学式可知它是一种酰胺类有机物,所以能水解生成氨和二氧化碳,它不是酸性物质。所以该题的答案为D。
(2)与工业生产相联系
例题2 2001年理科综合高考试题(全国卷)26题(4):
在啤酒生产过程中,发酵是重要环节。生产过程大致如下:将经过灭菌的麦芽汁充氧,接入啤酒酵母菌菌种后输入发酵罐。初期,酵母菌迅速繁殖,糖度下降,产生白色泡沫,溶解氧渐渐耗尽。随后,酵母菌繁殖迅速下降,糖度加速降低,酒精浓度渐渐上升,泡沫不断增多。当糖浓度下降一定程度后,结束发酵。最后分别输出有形物质和啤酒。
根据上述过程,回答下列问题:
请写出由麦芽糖→葡萄糖→酒精的反应方程式 。
例题2是学科间综合试题的其中一小题,主要考查麦芽糖、葡萄糖化学式的书写和由二糖转化为单糖,再由单糖转化为酒精化学方程式的书写,由二糖转化为单糖是水解反应,由单糖转化为酒精和二氧化碳是分解反应。高考中考生出现的错误主要原因是麦芽糖的化学式或结构简式书写错误。
(3)与日常生活相联系
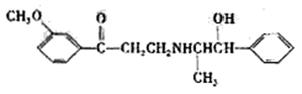
例题3 (04年理综吉林四川卷)科学家发现某药物M能治疗心血管疾病是因为它在人体内能释放出一种“信使分子”D,并阐明了D在人体内的作用原理。为此他们荣获了1998年诺贝尔生理学或医学奖。
请回答下列问题:
(1)已知M的分子量为227,由C、H、O、N周四种元素组成,C、H、N的质量分数依次为15.86%、2.20%和18.50%。则M的分子式是_____________________。D是双原子分子,分子量为30,则D的分子式为________________。
(2)油脂A经下列途径可得到M。
![]() 图中②的提示
图中②的提示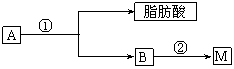 :
:
C2H5OH+HO-NO2 C2H5O-NO2+H2O
硝酸 硝酸乙酯
反应①的化学方程式是__________。
反应②的化学方程式是___________________。
(3)C是B和乙酸在一定条件下反应生成的化合物,分子量为134,写出C所有可能的结构简式_______________________________。
(4)若将0.1mol B与足量的金属钠反应,则需消耗_________g金属钠。
本题赋分14分,是典型的信息迁移题,与诺贝尔奖扯在一起,起点很高,落点却很低,考查的都是有机最基础的写化学方程式、写分子式、结构简式,第(1)(4)涉及的化学方程式也很简单。本题难在学生平时对油脂的一些反应和性质没有引起重视,这个知识点好些年没有考过,平时练习想都没有想过,失分相当严重。这题告诉我们:综合能力测试没有所谓的热点,也没有冷点,只有认真对照考试大纲,熟悉教材,才能融会贯通,丢掉教材,增天围绕一本教辅资料转是休想得高分的。
6.对应训练
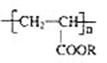 1.(04年上海理综)聚丙烯酸酯类涂料是目前市场上流行的墙面涂料之一,它具有弹性好,不易老化、耐擦洗、色泽亮丽等优点。右边是聚丙烯酸酯的结构简式,它属于
1.(04年上海理综)聚丙烯酸酯类涂料是目前市场上流行的墙面涂料之一,它具有弹性好,不易老化、耐擦洗、色泽亮丽等优点。右边是聚丙烯酸酯的结构简式,它属于
(C )。
①无机化合物 ②有机化合物 ③高分子化人合物 ④离子化合物 ⑤共价化合物
A.①③④ B.①③⑤ C.②③⑤ D.②③④
2.(04年上海理综)室内装潢和家具挥发出来的甲醛是室内空气的主要污染物,甲醛易溶于水,常温下有强烈刺激性气味,当温度超过20℃时,挥发速度加快,根据甲醛的这些性质,下列做法错误的是( D )。
A.入住前房间内保持一定温度并通风
B.装修尽可能选择在温度较高的季节
C.请环境监测部门检测室内甲醛含量低于国家标准后入住
D.紧闭门窗一段时间后入住
3.(04年北京理综)心炯胺是治疗冠心病的药物。它具有如下结构简式: ( B )
|
下列关于心炯胺的描述,错误的是 ( )
A.可以在催化剂作用下和溴反应 B.可以和银氨溶液发生银镜反应
C.可以和氢溴酸反应 D.可以和浓硫酸与浓硝酸的是混合液反应、
4.据报道,近来发现了一种新的星际分子氰基辛炔,其结构式为:(B)
HC≡C―C≡C-C≡C-C≡C-C≡N。对该物质判断正确的是
A.晶体的硬度与金刚石相当 B.能使酸性高锰酸钾溶液褪色
C.不能发生加成反应 D.可由乙炔和含氮化合物加聚制得
5.(04年广西化学)我国研制的长征捆绑式火箭在第一、二级发动机中用“偏二甲(基)肼”和四氧化二氮作为液体燃料。
(1)已知偏二甲(基)肼的相对分子质量为60,其中含碳40%,含氢13.33%,其余为氮;
又知其分子中有一个氮原子不与氢原子相连。通过计算写出偏二甲(基)肼的化学式和分子结构简式:
(2)在发动机中偏二甲(基)肼在四氧化二氮中充分燃烧,写出该燃烧反应的化学方程式
(反应中所有的氮元素均转化为N2)
参考答案:(1)![]() H3C
H3C
C2H8N2; N―NH2
![]() H3C
H3C
(2)C2H8N2+2N2O4 2CO2↑+4H2O↑+3N2↑
6.(04年广西化学)维生素C(又名抗坏血酸,分子式为C6H8O6)具有较强的还原性,放置在空气中易被氧化,其含量可通过在弱酸性溶液中用已知溶液的I2溶液进行滴定。该反应的化学方程式如下:
C6H8O6+I2 C6H6O6+2HI
现欲测定某样品中维生素C的含量,具体的步骤及测得的数据如下。取10mL 6mol・L-1CH3COOH,加入100mL蒸馏水,将溶液加热煮沸后放置冷却。精确称取0.2000g样品,溶解于上述冷却的溶液中,加入1mL淀粉指示剂,立即用浓度为0.05000mol・L-1的I2溶液进行滴定,直至溶液中的蓝色持续不褪为止,共消耗21.00mLI2溶液。
(1)为何加入的CH3COOH稀溶液要先经煮沸、冷却后才能使用?
(2)计算样品中维生素C的质量分数。
答案:(1)煮沸是为了除去溶液中溶液的O2,避免维生素C被O2氧化,冷却是为了减缓滴定过程
中维生素C与液面上空气接触时被氧化的速度。
(2)![]() =92.40%
=92.40%
7.(04年江苏化学)石油化工是江苏省的支柱产业之一。聚氯乙烯是用途十分广泛的石油化工产品,某化工厂曾利用下列工艺生产聚氯乙烯的单体氯乙烯:
CH2=CH2+Cl2 →CH2CI―CH2C1…………………①
CH2CI―CH2C1→CH2=CHCl+HCl………………②
请回答以下问题:
(1)已知反应①中二氯乙烷的产率(产率=![]() ×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8t乙烯可制得氯乙烯 t,同时得到副产物氯化氢 t。(计算结果保留1位小数)
×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8t乙烯可制得氯乙烯 t,同时得到副产物氯化氢 t。(计算结果保留1位小数)
(2)为充分利用副产物氯化氢,该工厂后来将下列反应运用于生产:
2CH2=CH2+4HCl+02→2 CH2CI―CH2C1+2H20………―③
由反应①、③获得二氯乙烷,再将二氯乙烷通过反应②得到氯乙烯和副产物氯化氢,副产物氯化氢供反应③使用,形成了新的工艺。
由于副反应的存在,生产中投入的乙烯全部被消耗时,反应①、③中二氯乙烷的产率依次为a%、c%;二氯乙烷全部被消耗时,反应②中氯化氢的产率为b%。试计算:反应①、③中乙烯的投料比为多少时,新工艺既不需要购进氯化氢为原料,又没有副产物氯化氢剩余(假设在发生的副反应中既不生成氯化氢,也不消耗氯化氢)。
答案: (1)5.8; 3.4
(2)设投入反应①、③的乙烯物质的量分别为x、y,则:
由反应①生成的二氯乙烷为x・a%,
由反应③生成的二氯乙烷为y・c%,
则由反应①、③共制得二氯乙烷的物质的量为(x•a%+y•c%),通过反应②可获得HCl的物质的量为
(x•a%+y•c%)・b%。
据题意,反应③消耗的HCl为2•y•c%,则:
2•y•c%=(x•a%+y•c%)•b%
解得:![]() =
=![]()
反应①、③中乙烯的投料比应为![]() 。
。
8.(04年上海高考化学)人们对苯的认识有一个不断深化的过程。
(1)1834年德国科学家米希尔里希,通过蒸馏安息香酸(![]() )和石灰的混合物得到液体,命名为苯,写出苯甲酸钠与碱石灰共热生成苯的化学方程式
)和石灰的混合物得到液体,命名为苯,写出苯甲酸钠与碱石灰共热生成苯的化学方程式
(2)由于苯的含碳量与乙炔相同,人们认为它是一种不饱和烃,写出C6H6的一种含叁键且无支链链烃的结构简式 。
苯不能使溴水褪色,性质类似烷烃,任写一个苯发生取代反应的化学方程式
(3)烷烃中脱水2 mol氢原子形成1 mol双键要吸热,但1,3―环己二烯(![]() )脱去2 mol氢原子变成苯却放热,可推断苯比1,3―环己二烯
(填稳定或不稳定)。
)脱去2 mol氢原子变成苯却放热,可推断苯比1,3―环己二烯
(填稳定或不稳定)。
 (4)1866年凯库勒(右图)提出了苯的单、双键交替
(4)1866年凯库勒(右图)提出了苯的单、双键交替
的正六边形平面结构,解释了苯的部分性质,但还有一些
问题尚未解决,它不能解释下列 事实
(填入编号)
a.苯不能使溴水褪色 b.苯能与H2发生加成反应
c.溴苯没有同分异构体 d.邻二溴苯只有一种
(5)现代化学认为苯分子碳碳之间的键是 。
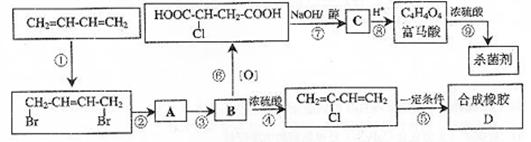 9. (04年上海高考化学)从石油裂解中得到的1,3―丁二烯可进行以下多步反应,得到重要的合成橡胶和杀菌剂富马酸二甲酯。
9. (04年上海高考化学)从石油裂解中得到的1,3―丁二烯可进行以下多步反应,得到重要的合成橡胶和杀菌剂富马酸二甲酯。
(1)写出D的结构简式
(2)写出B的结构简式
(3)写出第②步反应的化学方程式
(4)写出富马酸的一种相邻同系物的结构简式
(5)写出第⑨步反应的化学方程式
(6)以上反应中属于消去反应的是 (填入编号)。
答案:下面28、29答案即为上面第8、9题答案
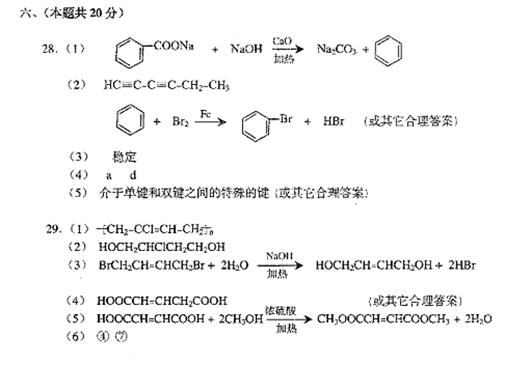
1、据最近的美国《农业研究》杂志报道,美国的科学家发现半胱氨酸能增强艾滋病毒感染者的免疫力,对控制艾滋病毒的蔓延有奇效。已知半胱氨酸的结构简式为:
![]() HS―CH2―CH―COOH,则下列说法错误的是
HS―CH2―CH―COOH,则下列说法错误的是
|
B、半胱氨酸是一种两性物质
C、两分子半胱氨酸,脱水形成的二肽结构简式为:
![]() HS―CH2―CH―C―O―S―CH2―CH―COOH
HS―CH2―CH―C―O―S―CH2―CH―COOH
D、HS―CH2―CH―COONH4可与NaOH溶液反应放出一种碱性气体
2、最近,传媒连续在头版显著版面作了关于“900吨致癌大米的报道,其中部分已经检验证实含致癌物黄曲霉毒素:AFTB,其分子结构式是:
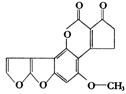 它是污染粮食的真菌霉素,人体的特殊基因在黄曲霉素的作用下会发生突变,有转变成肝癌的可能性,跟1 mol该化合物起反应的H2或NaOH的最大值分别是
它是污染粮食的真菌霉素,人体的特殊基因在黄曲霉素的作用下会发生突变,有转变成肝癌的可能性,跟1 mol该化合物起反应的H2或NaOH的最大值分别是
A.6mol,2mol B.7mol,2mol C.6mol,lmol D.7mol,1mol
3、开关是以二进制为基础的电子计算机的主要器件之一。要在分子水平上研制分子计算机,分子开关十分关键,一种利用化学反应的电控开关;反应如下:
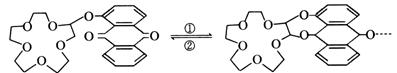
反应①使有机物A“胳膊”接通即“开”;反应②使其“断开”;从而利用有机反应可使计算机处于“开”和“关”两种状态(见上图),试回答下列问题:
(1)有机物A由于其形状酷似美国西部用来捕捉动物的套索,故A可称之为 。
A.套索醇 B.套索醚 C.套索酮 D.套索烃
(2)从有机化学反应的类型来分,当分子计算机开机时进行 反应。分子计算机关机时进行 反应。
(3)反应①和②是否属于可逆反应 ;理由是 。
(4)使1 mol有机物A完全被氢化需要 mol氢气,所得产物在一定条件下与乙酸反应的类型是 。
4、某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用,不仅可以提高经济效应,而且还能防止环境污染,现按下列方式进行综合利用。
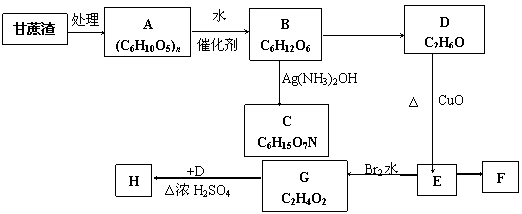 |
|
已知F、H均是具有香味的液体,F为E的三聚物,并且有特殊的六元环状对称结构。
(1)A的名称是____________;F的结构式为 _______,H的其同类物的异构体还有(写结构简式)_________________ ________ __。
(2)写出D→E的化学方程式:
_______________________________ ___;
写出B→C的离子方程式:
_________________________________ ___。