高三第二次化学联考
命题:武汉新洲一中 曹淑梅 审定:武汉审学海教科所
本试卷分第I卷(选择题)和第II卷(非选择题)两部分,共100分。考试时间90分钟。
相对原子质量:C―12 H―1 O-16 N―14 F―19 S-32 Cl―35.5
Na-23 Mg-24 Al-27 Fe-56 Cu―64 Ca―40
第I卷(选择题,共48分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
一、选择题:本大题包括16个小题,每小题3分,共48分。每小题只有一个选项符合题意。
l.我国继启动了食盐补碘工程之后,今年又启动了补铁工程。我国补铁工程的载体主要是
A.食盐 B.淀粉 C.酱油 D.食油
2.为“绿色奥运”某同学提出了下列环保建议,其中你认为可以采纳的是
①用气态燃料代替液态和固态燃料作为发动机动力来源
②开发生产无汞电池
③提倡使用一次性发泡塑料餐具和塑料袋
④分类回收垃圾
⑤开发无磷洗涤剂
⑤提倡使用手帕,减少餐巾纸的使用
A.①③③④ B.②③④⑤ C.①②④⑤⑥ D.全部
3.下列溶液一定呈碱性的是
A.c(OH-)>c(H+) B.c(H+)=1×10-7mol/L
C.使甲基橙变黄 D.含OH-
4.下列分子中所有原子不可能共平面的是
A.![]() B.CF2=CF2
B.CF2=CF2
C.CH≡C―CH=CH2 D.CO2
5.在实验中不慎手指被玻璃划破,可用三氯化铁溶液应急止血,其主要原因可能是
A.FeCl3溶液具有杀菌消毒作用
B.FeCl3溶液能产生Fe(OH)3沉淀堵住伤口
C.FeCl3溶液能使血液聚沉
D.FeCl3溶液对人体无毒
6.下列说法不正确的是
A.胶体能够稳定存在的主要原因是:同种胶体带有同种电荷
B.水的沸点在同族元素形成的氢化物中最高是因为水分子间能形成氢键
高三・二联・化学(小综合)第1页(共6页)
C.苯酚和乙烯都能使溴水褪色,但原理不同
D.25℃时,PH=l的HCI溶液和PH=13的NaOH溶液中,水的电离度相等
7.HgCl2的稀溶液可用作手术刀的消毒剂,已知熔融的HgCl2不导电,而HgCl2的稀溶液
有弱的导电能力,下列关于HgCl2的叙述正确的是
A.HgCl2属于离子化合物 B.HgCl2属于共价化合物
C.HgCl2属于非电解质 D.HgCl2不能使蛋白质变性
8.可逆反应:![]() ,升高温度,气体的平均相对分子质量变小,
,升高温度,气体的平均相对分子质量变小,
则下列判断正确的是
A.B和C一定都是固体
B.B和C一定都是气体
C.若C为固体,则B一定是气体
D.B和C不可能都是气体
9.有一铁的氧化物样品,用5mol・L-1盐酸100mL恰好完全溶解,所得溶液还能吸收标况
下的1.12LCl2,则该氧化物的化学式可表示为
A.FeO B.Fe2O3 C.Fe3O4 D.Fe4O5
10.下列各项中的两个量,其比例最接近2:1的是
A.40℃时pH=7的(NH4)2SO4与NH3・H2O的混合液中,c(NH4+)与c(SO42-)
B.相同温度下,0.01mol/L的醋酸溶液与0.02mol/L醋酸溶液中的c(H+)
C.液面均在“0”刻度时,50mL酸式滴定管和25mL酸式滴定管内所盛溶液的体积
D.硫酸铵晶体中n(NH4+)与n(SO42-)
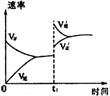 11.在密闭容器中进行反应
;右图是某次实验的化学反
11.在密闭容器中进行反应
;右图是某次实验的化学反
应速率随时间变化的图形,推断在t1时刻突然变化的条件可能是
A.减小容器的体积,增大压强
B.使用催化剂
C.升高体系的温度
D.增大生成物浓度,减小反应物浓度
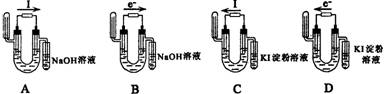
12.下图中能验证用惰性电极电解NaCl溶液(含酚酞)的电解产物的装置的是(![]() 表示直流
表示直流
电源,I表示电流强度,e-表示电子)
13.某芳香族化合物的分子式为C8H6O2,该分子(除苯环外,不含其它环)中不可能有
A.一个―CHO B.一个―COOH C.两个―OH D.两个――CHO
14.某有机物分子中含有C、H、N、O四种元素,以n(C)、n(H)、n(N)、n(O)分别表示C、H、N、O的原子数目,则H原子数目最多为
高三・二联・化学(小综合)第2页(共6页)
A.2n(C)+2+n(N) B.n(C)+n(N)+n(O)+8
C.3n(C)+2n(N) D.2n(C)+n(N)+n(O)+2
5.在恒温、恒容的密闭容器中发生如下反应:![]() ;当H2和Br2的起始浓度均为0.20mol・L-1时,达到平衡时HBr的浓度为0.32mol・L-1,则当H2和Br2的
;当H2和Br2的起始浓度均为0.20mol・L-1时,达到平衡时HBr的浓度为0.32mol・L-1,则当H2和Br2的
起始浓度均为0.10mol・L-1时,达平行时H2的浓度(mol・L-1)为
A.0.01 B.0.02 C.0.04 D.0.08
6.两份等体积、等浓度的NaOH溶液,分别与体积相等的MgCl2、AlCl3溶液混合,充分反应
后,Mg2+、Al3+均恰好形成沉淀,则原MgCl2、AlCl3溶液中Cl-浓度之比为
A.1:1 B.1:2 C.2:3 D.3:2
第II卷(非选择题,共52分)
二、本题包括两小题,共17分。
7.(5分)下面a~e是中学化学实验中常见的几种定量仪器:
(a)量筒 (b)容量瓶 (c)滴定管 (d)托盘天平 (e)温度计
(1)其中标示出仪器使用温度的是___________(填写编号);
(2)能够用以精确量取液体体积的是_____________(填写编号);
(3)由于错误操作,使得到的数据比正确数据偏小的是____________(填写编号);
A.用量筒量取一定量液体时,俯视液面读数
B.中和滴定达终点时俯视滴定管内液面读数
C.使用容量瓶配制溶液时,俯视液面定容后,所得溶液的浓度
(4)称取10.5g固体样品(1g以下使用游码)时,将样品放在了天平的右盘,则所称样品
的实际质量为g。
(5)有下列实验:①苯与溴的取代反应②苯的硝化反应③乙醛的银镜反应④酚醛树脂的制取
⑤乙酸乙酯的制取⑥石油分馏实验;其中需要使用温度计的有____________(填写编号)。
8.(12分)下图是某化学兴趣小组进行丁烷裂解的实验流程。(注:CuO能将烃氧化成CO2
和H2O,G后面的装置与答题无关,省略。铁架台等已省略)
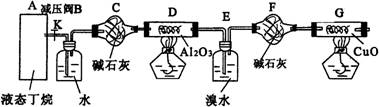
按上图连好装置后,需进行的实验操作有:①给D、G装置加热;②检查整套装置的
气密性;③排出装置中的空气等……
高三・二联,化学(小综合)第3页(共6页)
(1)这三步操作的先后顺序依次是_____________________。
(2)简要说明排空气的方法和证明空气已排尽的方法。
(3)B装置的作用是___________________________________________________________。
(4)若对E装置中的混合物,再按以下流程实验:
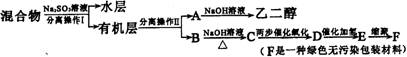
①分离操作I和II的名称分别是:I___________、II________________
②Na2SO3溶液的作用是(用离子方程式表示)___________________________________。
③E的结构简式是:________________________________。
三、本大题包括两小题,共12分。
19.(4分)用“>”、“<”或“=”填写下列空白。
用0.2mol・L-1HA溶液与0.2mol・L-1NaOH溶液等体积混合,测得混合溶液中c(Na+)
>c(A-),则
(1)混合溶液中c(HA)_______c(A-);
(2)混合溶液中c(HA)+c(A-)_____0.1mol・L-1;
(3)混合溶液中,由水电离出的c(OH-)______0.2mol・L-1HA溶液由水电离出的c(H+);
(4)25℃时,如果取0.2mol・L-1HA溶液与0.1lmol・L-1NaOH溶液等体积混合,测得
混合溶液的PH<7,则HA的电离程度____NaA的水解程度。
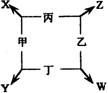 20.(8分)甲、乙、丙、丁四种单质在点燃的条件下反应生成X、Y、Z、W四种化合物,转化关系如右图所示,又知:
20.(8分)甲、乙、丙、丁四种单质在点燃的条件下反应生成X、Y、Z、W四种化合物,转化关系如右图所示,又知:
①甲、乙、丙均为短周期元素的单质,常温下均为气态,丁是日常生
活中的常见金属;
②常温下,X是无色液体,Y是黑色固体;
③丙在乙中燃烧发生苍白色火焰,丁在乙中燃烧生成棕色烟,W的
水溶液呈黄色。请填空:
(1)丁在甲和X同时存在的条件下,容易被腐蚀,写出电子反应式:
负极:__________________________ 正极:_________________________________
(2)将饱和W的溶液滴入到热的X中煮沸几分钟,反应的化学方程式为
___________________________________________________________________________。
高三・二联・化学(小综合)第4页(共6页)
(3)Y与足量的稀HNO3反应的离子方程式为:
________________________________________________________________________。
(4)在一定条件下,丁分别Y、Z反应生成等物质的量的丙时,消耗丁的物质的量之比
为___________。
四、本大题包括两小题,共16分。
21.(8分)烷烃A只可能有3种一氯取代产物B、C和D。C的结构简式是![]()
B和D分别与强碱的醇溶液共热,都只能得到有机化合物E。以上反应及B的进一步反应如下图所示:
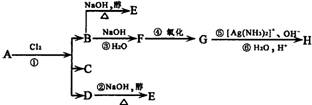
请回答:
(1)写出结构简式A:________________________________________。
(2)B转化生成E的反应类型为_____________反应。
(3)反应①的条件是_________________。
(4)反应②的化学方程式为:
___________________________________________________________________________。
(5)反应⑤的化学方程式为:
___________________________________________________________________________。
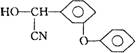
![]() 22.(8分)已知①R―X+NaCN→R―CN+NaX;②R―CN
R―COOH。某高效、低
22.(8分)已知①R―X+NaCN→R―CN+NaX;②R―CN
R―COOH。某高效、低
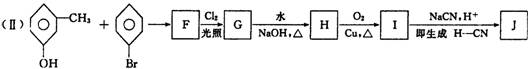
毒的农药K的合成路线如下:(部分无机物已省略)
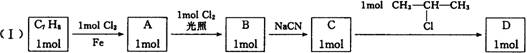
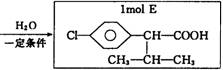
高三・二联・化学(小综合)第5页(共6页)
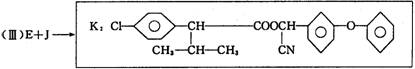
根据以上信息填空:
(1)试推导写出下列物质结构简式:
B:_______________________________,J:___________________________________,
(2)完成化学方程式:
C→D:____________________________________________________________________
H→I:____________________________________________________________________
五、本大题包括一小题,共7分。
23.(7分)气体A由C、H、S、F中的三种元素组成,将标况下的1.12L气体A在过量O2中完全燃烧,恢复到原状态,放出QkJ的热量,已知气态生成物全部被过量的Ca(OH)2溶液吸收,可以得到6.95g沉淀。再取标况下的1.12L气体A装入一个薄膜袋里,袋和气体的总质量为2.20g。(不考虑浮力。已知CaF2、CaSO3、CaCO3难溶于水),根据上述数据:
(1)估算A的相对分子质量不会大于__________________。
(2)确定A的化学式为__________________________。
(3)薄膜袋的质量为__________________。
(4)写出该条件下,A在O2中燃烧的热化学方程式:
________________________________________________________________________。
高三・二联・化学(小综合)第6页(共6页)
高三・二联・化学(小综合)・参考答案
一、(共48分)
1.C 2.C 3.A 4.A 5.C 6.A 7.B 8.C9.D 10.D ll.C 12.D 13.B 14.A 15.B 16.A
二、(共17分)
17.(5分,每空1分)
(1)abc(2)c(3)B(4)9.5(5)②⑥
18.(12分)
(1)②③①(2分)
(2)打开开关K,利用丁烷气体排出空气;用小试管在G装置后收集一试管气体,移近火焰上方,若听到轻微的爆鸣声,表明空气已排尽。(2分)
(3)便于观察丁烷气体的流量,从而控制丁烷气体的流速。(2分)
(4)①分液(1分)蒸馏(1分)
![]()
![]()
三、(共12分)
19.(4分,每空1分)
(l)<(2)=(3)>(4)>
20.(8分)
![]()
![]()
![]()
(4)3:4(2分)
四、(共16分)
21.(8分)
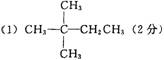
(2)消去(1分)(3)光照(1分)
![]()
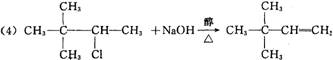
![]()
![]()
22.(8分,每空2分)
二联・答案・化学 第1页(共2页)
![]()
![]()
![]()
![]()
![]()
五、(共7分)
23.(7分)
(1)44(2分)(2)CH3F(2分)(3)0.50g(1分)
![]()
![]()
二联・答案・化学 第2页(共2页)