�����ڶ��ָ�ϰ���ۻ�ѧģ���Ծ����ģ�
�ڢ����ѡ���48�֣����⣺���պ졡��
�ڢ��
�����õ������ԭ��������H��1�� N��14�� O��16�� S��32��Cl��35.5��Fe��56��Cu��64
���������������������� Pb��207�� Cr��52
һ��ѡ���⣨�������8С�⣬ÿС��6�֣���48�֡�ÿС��ֻ��һ��ѡ���������⣩
6�������йػ�������������չ�������У�����ȷ����
A�����������(��������η۳�)�γ����ܽ��������ཡ��Σ������
B������������ɫ��Դ(����̫����)�����ʯȼ��������ɳ�����չ�ı���֮·
C��װ�����еı���Ҫ���Խ�����ȣ���ǿ�°����
��D�������������ǿ��������������Ҫ��Ŀ֮һ
7��2005��1��14�գ��ɹ���½�����������ġ��ݸ�˹����̽����������350����Ƭ�ʹ������ݡ�����ָ���������������Ƶ������ꡱ���������ꡱ�ijɷ���Һ̬���顣���й�����������˵���У�����ȷ����
A���������ϴ����л����ӡ������� B���ر��¶ȼ���
C����ò�γ���Һ̬�����ˢ�йء���D�����������γ��˼������Һѭ��ϵͳ
8�����и�������£���Һ�п��ܴ������ڵ���������
A��ʹpH��ֽ�ʺ�ɫ����Һ�У�I����Cl����NO3����Na+
B������������ɫ��Һ�У�K+��Mg2+��NO3����MnO4��
C����ˮ�������c(H+)=l��10��12mol/L����Һ�У�K+��Na+��Cl����NO3��
D�����н϶��Al3+����Һ�У�K+��Ca2+��ClO����Cl��
9.����ͼ���ֱ�������ˮ����ʢˮ��ijҺ��A���ٷֱ����һ�α���ˮ��Ȼ�������ʹ����ӽ�Һ�棬�������ƶ���ˮ�θ����ƶ��������β��ƶ�����Һ��A����Ϊ��
��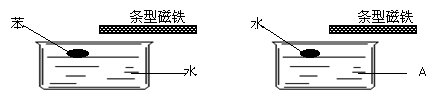
A��ú�͡��� B. �ƾ������� C. ��������D. ���Ȼ�̼
10.�մɱ�����һ��Ѥ����ʵIJ��ԣ��ӹ�����������ͨ�����м���һЩ����Ԫ�أ���������ʱ����������(��������)��ʹ��õ���ͬ����ɫ�����������㣬����ͭ����Ԫ���γɵĻ�������ֵ���ɫ�ֱ��ǣ�����
A. �����̡��졢�ں֡� ����B. ���ơ������Ϻ�
C. �����̡������ں֡� ����D. ���ơ��졢�Ϻ�
 11�����Ӿ硶���μǡ����ɾ�������ۼ����Щ���ɾ����������������NH4NO3��Zn�۰�������8:6.5��Ϸ������ȵ�ʯ�����ϣ�ʹ��ʱ��ˮ���μ����������İ��̡���֪������Ӧ����N2��ˮ���ɡ��йص�˵������ȷ���ǣ�
��
11�����Ӿ硶���μǡ����ɾ�������ۼ����Щ���ɾ����������������NH4NO3��Zn�۰�������8:6.5��Ϸ������ȵ�ʯ�����ϣ�ʹ��ʱ��ˮ���μ����������İ��̡���֪������Ӧ����N2��ˮ���ɡ��йص�˵������ȷ���ǣ�
��
��ˮ�����ܽ�NH4NO3,��������������������Ӧ�ķ��������ã���ÿ��ԭ1molNO3-������1molNH4+��1molZn���۳�������������������С�������ܳ���������Сп��������NH4NO3��Ӧ���ȶ�������
���� A���٢ڡ�����B���ڢۡ����� C���ۢܡ����� D���٢�
![]()
![]()
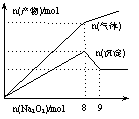
![]() 12����Na2O2���뵽����Al3+��Mg2+��NH4+�Ļ����Һ�в�����5������������������ʵ��������Na2O2�����ʵ����Ĺ�ϵ��ͼ��ʾ����ԭ��Һ��Al3+��Mg2+��NH4+�����ʵ����ֱ�Ϊ
12����Na2O2���뵽����Al3+��Mg2+��NH4+�Ļ����Һ�в�����5������������������ʵ��������Na2O2�����ʵ����Ĺ�ϵ��ͼ��ʾ����ԭ��Һ��Al3+��Mg2+��NH4+�����ʵ����ֱ�Ϊ
A��2 mol��3 mol��8 mol����B��3 mol��2 mol��8 mol��������
C��2 mol��3 mol��4 mol����D��3 mol��2 mol��4 mol
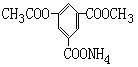 13. ij�л���ṹ��ʽ����ͼ��
13. ij�л���ṹ��ʽ����ͼ��
������1mol������NaOH��Һ��ַ�Ӧ��
����NaOH�����ʵ���Ϊ����������
A. 6mol����B. 5mol���� C. 4mol���� D. 3mol
��II������60�֣�
������������ �༶������������ ��������������
| ��� | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| �� |
|
|
|
|
|
|
|
|
26��(10��)��֪��(I)����ͬϵ���ܱ����Ը���������������磺![]()
|
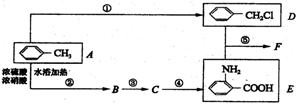
(��)RNH2+R'CH2Cl��������RNHCH2R'+HCl��(R��R'��������)���ݡ��й���ҩ��������������F�������Ʊ������ǵ䡱ҩƷ(��������ʹ)���м�����ϳ�·����ͼ���밴Ҫ����գ�
(1)C�Ľṹ��ʽ��________________��B��E�Ĺ�ϵΪ________________
(2)��Ӧ�ݵĻ�ѧ����ʽΪ____________________________________________________��E��һ�������£��ɾۺϳ��ȹ������õĹ��ܸ߷��ӣ��йط�Ӧ�Ļ�ѧ����ʽΪ______________________________________
(3)��Ӧ�١����У�����ȡ����Ӧ����__________________
(4)���ڻ�����E�ı�����������һ����C2H3ԭ�����γɻ�����M����1 mol M����NiΪ���������¼��������H2________mol��
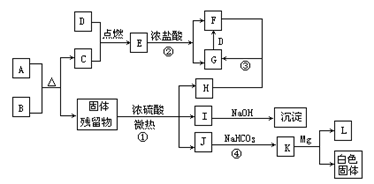 27.��9�֣���ɫ����A���ɫ����B�ɷ�������ͼ��ʾ�ķ�Ӧ����ͼ����ʾ���ʼ���Ӧ�����⣬������Ӧ��������P��Ӧ����������ȥ������D��LΪ��̬���ʣ�C��HΪ��̬���ʣ�J����ɫ��ӦΪ��ɫ��
27.��9�֣���ɫ����A���ɫ����B�ɷ�������ͼ��ʾ�ķ�Ӧ����ͼ����ʾ���ʼ���Ӧ�����⣬������Ӧ��������P��Ӧ����������ȥ������D��LΪ��̬���ʣ�C��HΪ��̬���ʣ�J����ɫ��ӦΪ��ɫ��
(1)д����ѧʽ��A__________________��E__________________��
(2)д������K�ĵ���ʽ______________________��
(3)д����Ӧ�٢ڵĻ�ѧ����ʽ��
��____________________________________________________��
��____________________________________________________��
(4)д����Ӧ�ۢܵ����ӷ���ʽ��_______________________________________________________��
28����19�֣�ʵ�����и���2SO2+O2�P2SO3����H=��196.6KJ/mol�����ͼ��ʾʵ��װ�����Ʊ�SO3���塣��ش��������⣺
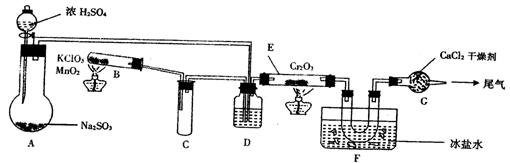
��1��ʵ��ǰ��������еIJ����ǣ���������ƣ�����д������̣������������� ��������������������
��2����Aװ���м���Na2SO3�����ͬʱ������Ӽ���ˮ��Ȼ���ٵμ�Ũ���ᡣ�Ӽ���ˮ������������������������������ ��
��3��С�Թ�C���������������������������� ��
��4�����ƿD��ʢ���Լ����������������������� ��
װ��D�����������ǣ��������������������������������������� ������������ ��
���������������������������������������������������������������������� ��
���������������������������������������������������������������������� ��
��5��ʵ���е�Cr2O3�������ʱ��Ӧ���ƾ����ƿ�һ����ټ��ȣ��Է��¶ȹ��ߣ���������ԭ���������������������������������������������������� �������� ��
��6��װ��F��U�����ռ��������ʵ���ɫ��״̬������������������������ ����
��7��װ��G������������������������������������������������������������ ����
��8����Gװ�õ�����β�������������������������������������������������� ��
26����12�֣��ڱ�״���½�cmolCl2ͨ�뺬amolFeBr2��bmolFeI2����Һ�У���cȡ��ֵͬʱ����Ӧ��������Һ���в�ͬ���ʣ���������������ˮ�ķ�Ӧ����
��1������ ���±��пո�������
| c��ȡֵ���ú�a��b�Ĵ���ʽ��ʾ�� | ��Ӧ����Һ�����ʵĻ�ѧʽ ��ֻҪ��д������ |
|
| FeBr2��FeI2��FeCl2 |
| b��c��1/2��a+3b�� |
|
|
| FeBr3��FeCl3 |
|
| FeCl3 |
��2����a=b=1 ��c=2ʱ����Ӧ����Һ������������������������������������������� ��д��ѧʽ������Щ���ʵ����ʵ���֮���������������������������� ��
��3����a=b=1 ��c=2.5ʱ��д��Cl2ͨ����Һ���ܵ����ӷ���ʽ����дһ��������������е����ӷ�Ӧ����_________________________________________________________.
�����ڶ��ָ�ϰ���ۻ�ѧģ���Ծ�������
�� ��
| ��� | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| �� | D | B | D | D | A | B | C | B |
![]()
26��(10��)(1)�������������� ����Ϊͬ���칹�塣
(2)
(3) �٢ڢݡ��� (4) 4��
27. ��1��KClO3��Fe3O4��
��2��
|
��3����MnO2+2KCl+3H2SO4��Ũ��======2KHSO4+MnSO4+Cl2��+2H2O
��Fe3O4+8HCl=====2FeCl3+FeCl2+4H2O
��4����Cl2+2Fe2+====2Cl2++2Fe3+
��H++HCO3-====CO2��+H2O
28����19�֣��� ��1�����װ�õ�������
���������� ��2��ˮ��Ũ�������÷��ȣ�������SO2�ķų�
��3�����塢��ֹ����
��4��Ũ����
�ٸ���SO2��O2
��ʹSO2��O2��Ͼ��ȡ��������������� ÿ��1�֣�����ÿ��2��
��ͨ���۲������������������ٶ�
��5���¶ȹ��߲�����SO3�����ɣ���Ӱ������Ļ���
��6����ɫ������ɫ����
��7����ֹˮ������SO3�Ӵ�
��8����NaOH��Һ����
�٢ڢ�ÿ��1�֣�����ÿ��2�֡�
29.(10��)
��1����ÿ��1�֣���
|
|
|
| 0��c��b |
|
|
| FeBr2 FeBr3 FeCl2�� FeCl3 |
| 1/2(a+3b) ��c��3/2(a+b) |
|
| c �� 3/2(a+b) |
|
(2)FeBr3��FeCl3������ 1:2������ÿ��2�֣�
��3��4Fe2�� + 4I- + 2Br- +5Cl2 ===4Fe3�� + 2I2 +Br2 + 10Cl-��2�֣�