高三化学选择题错漏专题训练
一、 单项选择题(每小题只有一个答案)
1、25℃时,pH为9的Na2CO3溶液和pH为5的FeCl3溶液中,水的电离程度的大小关系是
A.前者大 B.两者相等 C.后者大 D.无法确定
2、将相等物质的量的CO和H2O(g)混合,在一定条件下反应:CO(g)+ H2O(g)![]() CO2(g)+
H2(g),达到平衡后CO的转化率为25%,平衡混合气体的密度是相同条件下氢气的倍数是
CO2(g)+
H2(g),达到平衡后CO的转化率为25%,平衡混合气体的密度是相同条件下氢气的倍数是
A.46 B.23 C.11.5 D.5.75
3、下列物质中,均直接由原子构成的是
① 二氧化碳 ② 二氧化硅 ③ 铁蒸气 ④ 金刚石 ⑤ 单晶硅 ⑥ 白磷
⑦ 硫磺 ⑧ 氨 ⑨ 钠 ⑩ 氖晶体
A、②③④⑤ B、②③④⑤⑨⑩ C、②③④⑤⑩ D、②④⑤⑥⑦⑨⑩
4、下列变化属于物理变化的是
A、浓硫酸镁溶液与蛋白质溶液混合 B、石墨转变为金刚石
C、稀硫酸溶液导电 D、块状纯碱在干燥空气中变成粉末
5、将3.9g镁铝合金,投入到500mL2mol/L的盐酸中,金属完全溶解,再加入4mol/L的NaOH溶液,若要生成的沉淀最多,加入的这种NaOH溶液的体积是
A、125mL B、200mL C、250mL D、560mL
6、将6.6g可能混有下列物质的(NH4)2SO4样品,在加热的条件下,与过量的NaOH反应,可收集
到2.15升NH3(密度为17克/22.4升),则样品中不可能含有的物质是
A.NH4HCO3,NH4NO3 B.(NH4)2CO3,NH4NO3
C.NH4HCO3,NH4Cl D.NH4Cl,(NH4)2CO3
7.FeSO4和Fe2(SO4)3 的混合物中含硫的质量分数为a%,则含铁的质量分数为
A.2a% B.3a% C.1-2a% D.1-3a%
8、下列有关臭氧的说法错误的是:
A、 它与氧气是氧的同素异形体
B、它具有强氧化性,可以作脱色剂、消毒剂
C、可以在高压放电条件下由氧气制备
D、臭氧层中含有大量的臭氧,可以吸收紫外线,是人类和生物的保护伞
二、选择题(每小题可能有1到2个选项符合题意,)
9、废切消液中含2%~5%的NaNO2,直接排放会造成环境污染,下列试剂中能使其转化为
不引起二次污染的物质是
A.HCl B.NH4Cl C.NaCl D.浓H2SO4
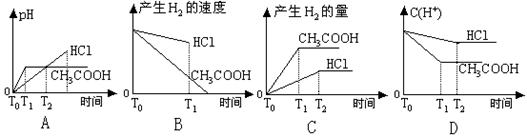
10、在体积都为1L,pH=2的盐酸和醋酸溶液中,投入0.65g锌粒,则下图所示比较符合客观
事实的是 C
11、常温下,pH=9的CH3COONa 溶液由水电离出来的C(H+)为a, pH=9的 NH3·H2O溶液
由水电离出来的C(H+)为b,下列a和b的关系正确的是
A.a=b B.a=104b C.b=10-4a D.a=10-4b
12、在蒸发皿中加热蒸干并灼热(低于400℃)下列物质的溶液,可以得到该物质固体的是
A、氯化铝 B、碳酸钠 C、碳酸镁 D、高锰酸钾
13、某种一元酸(HA)溶液中加入一定量的一种强碱(MOH)溶液后,恰好完全反应,则有关
反应后的溶液的判断中一定正确的是
A.若反应生成的MA水解,则 C(A— ) < C(OH— ) B. C(A— )≥ C(M+)
C.若反应生成的MA不水解,则C(A— ) > C(OH— ) D.C(A— )≤ C(M+)
14、经硫酸酸化的高锰酸钾溶液和过氧化氢溶液混合后,发生反应的化学方程式如下:
2KMnO4 + 5H2O2 + 3H2SO4 = 2MnSO4 + K2SO4 + 5O2↑+ 8H2O 下列对此反应的分析正确的是
A.过氧化氢作还原剂,硫酸作氧化剂 B.过氧化氢既作还原剂又作氧化剂
C.过氧化氢作还原剂,硫酸起酸化作用 D.高锰酸钾作氧化剂,氧气为氧化产物
15、下面的判断中正确的是
A.不用其它试剂只利用液体间的相互混合就能鉴别酒精、四氯化碳、甲苯、溴水和Na2CO3溶液
B.最外层电子数为偶数的短周期元素不会与卤素或氢形成最简式为AB3型的化合物
C.在由水电离提供的C(H+)为10—4mol·L-1的溶液中,Fe3+、SO42-、NO3-、ClO-离子可以
大量共存
![]()
![]()
![]()
![]() D.在CH C
CH2—CH = CH2 分子中所有原子一定处于同一平面
D.在CH C
CH2—CH = CH2 分子中所有原子一定处于同一平面
16、下列溶液,一定呈中性的是
A.C(H+)=1×10— 7mol·L-1的溶液 B.pH=14—pOH的溶液
C.C(H+)=C(OH—)=1×10—6mol·L-1的溶液 D.pH= pOH的溶液
17、在相同条件下,学生甲取100gKNO3饱和溶液,学生乙取50gKNO3饱和溶液,加热,分别
蒸发掉10g水,分别冷却到原来温度,则析出KNO3晶体的质量是
A、甲比乙少 B、乙比甲少 C、一样多 D、无法比较
18、根据热化学方程式:S(s)+O2(g) = SO2(g);△H=-297.23kJ/mol,分析下列说法中正确的是
A、S(g)+O2(g) = SO2(g);△H= -Q kJ/mol 。Q的值大于297.23
B、S(g)+O2(g) = SO2(g);△H= -Q kJ/mol 。Q的值等于297.23
C、1molSO2 的键能总和大于1molS和1mol O2的键能总和
D、1molSO2的能量总和大于1molS和1molO2的能量总和
19、下列事实可以证明氨水是弱碱的是
A、0.1mol/L的氨水可以使酚酞试液变红 B、0.1mol/L的氯化铵溶液的pH约为5
C、在相同条件下,氨水溶液的导电性比强碱溶液弱 D、铵盐受热易分解
20、已知K2HPO4溶液中HPO42— 的水解程度大于其电离程度,对于平衡
HPO42— + H2O ![]() PO43— + H3O+ ,欲使溶液中C(HPO42—)、C(H3O+)、C(PO43—)均减小,
PO43— + H3O+ ,欲使溶液中C(HPO42—)、C(H3O+)、C(PO43—)均减小,
可以采取的方法是
A、加水 B、加热 C、加消石灰 D、加硝酸银
21、膦(PH3)又称为磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含有。它的分子是三角锥形,以下关于PH3的叙述正确的是
A.PH3是非极性分子 B.PH3分子中有未成键的电子对
C.PH3是一种强氧化剂 D.PH3分子中的P—H键是极性键
22、一定条件下,4g和14g的混合气体体积为448mL,相同状况下,8gA和17gB的混合气体
体积为672mL,A、B可能是下列各组的
A.乙烯和乙炔 B.乙炔和苯 C.甲烷和甲醇 D.环己烷和1—丁烯