高三化学全真模拟试卷
第Ⅰ卷(选择题 共74分)
注意事项:
1.回答I卷前,考生务必在答题卡姓名栏内写上自己的姓名、考试科目、准考证号,并用2B铅笔涂写在答题卡上。
2.每小题选出正确答案后,用2B铅笔把答题卡上对应题号的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案。不能答在试题卷上。
3.回答II卷前,考生务必在答卷姓名栏内写上自己的姓名、考试科目、准考证号、所在县市,切勿写在装订线上,II卷答案按要求答在规定地方,只能用黑水笔作答。
4.考试结束,将答题卡和答卷一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Al―27 P-31 S―32 Cl-35.5 K-39 Ca--40 Na—23 Zn—65 Mg--24
一、选择题(本题包括8小题,每小题4分,共32分。每小题只有一个选项符合题意。)
1.我国决定推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇形成的混合燃料。下列相关叙述错误的是
A.使用乙醇汽油能减少有害气体的排放
B.乙醇汽油是一种新型的化合物
C.燃料中的乙醇可以通过粮食发酵或化工合成等方法制得
D.乙醇汽油的推广使用可以缓解石油资源短缺对经济发展造成的压力
2.下列物质的电子式书写正确的是
A.NaCl ![]() B.H2S
B.H2S ![]()
C.-CH3 ![]() D.NH4I
D.NH4I
![]()
3.下列有关实验问题的处理方法正确的是
A.浓硫酸不慎溅到皮肤上,应立即用碳酸钠溶液冲洗
B.实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室
C.在气体发生装置上直接点燃乙炔气体时,必须先检验乙炔气体的纯度
D.铜与浓硫酸反应时,用蘸有浓溴水的棉花放在导管口吸收多余的气体
4.下列各选项中两种粒子所含电子数不相等的是
A.羟甲基(-CH2OH)和甲氧基(CH3O-)
B.亚硝酸(HNO2)和亚硝酸根(NO2-)
C.硝基(-NO2)和二氧化氮(NO2)
D.羟基(-OH)和氢氧根(OH-)
|
A.X元素的氢化物分子间可以形成氢键
B.Y元素的两种同素异形体常温下都是气体
C.最高氧化物对应水化物的酸性:W>Z
D.阴离子半径从大到小排列的顺序为:X>Y>Z>W
6.101kPa时,2g辛烷完全燃烧生成二氧化碳气体和液态水,放出96.81kJ热量,则下列表示辛烷燃烧热的热化学方程式正确的是
A.2 C8H18 (l)+25O2(g) 16CO2(g)+18H2O(1);△H=—96.81kJ·mol-1
B.C8H18 (l)+25/2O2(g) 8CO2(g)+9H2O(1);△H=+5 518kJ·mol-1
C.2 C8H18
(l)+25O2(g) 16CO2(g)+18H2O(1);△H=—11 036kJ·mol-1
D.C8H18
(l)+25/2O2(g) 8CO2(g)+9H2O(1);△H=—5 518kJ·mol-1
7.同位素示踪法可用于反应机理的研究,下列反应或转化中同位素示踪表示正确的是( )
A.2Na218O2 + 2H2O == 4Nal8OH + O2↑
B.2KMnO4 + 5H218O2 + 3H2SO4 == K2SO4 + 2MnSO4 + 518O2↑+ 8H2O
C.NH4Cl
+ 2H2O![]() NH3·2H2O +
HCl
NH3·2H2O +
HCl
D.K37ClO3 + 6HCl == K37Cl + 3Cl2↑+ 3H2O
8.t℃时,将溶质质量分数为a %的NaOH溶液蒸发掉m g水后恢复至原温度,恰好得到质量分数为2a %的NaOH饱和溶液V mL,则下列说法中正确的是
A.t℃时NaOH的溶解度为![]() g
g
B.原溶液的质量为2m g
C.原溶液的物质的量浓度为![]() mol·L-1
mol·L-1
D.保持t℃,向原溶液中加入2a gNaOH可达饱和
二、选择题(本题包括10小题,第9—16题每小题4分,第17、18小题每小题5分,共42分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给满分,但只要选错一个该小题为0分)
9.电视剧《西游记》中仙境美仑美奂,这些神话仙境中所需的烟雾是用NH4NO3和Zn粉按质量比8﹕6.5混合放于温热的石棉网上,使用时滴水数滴即产生大量的白烟。又知发生反应后有N2和水生成。有关的说法中正确的是( )
A.水起着溶解NH4NO3,发生吸热现象以启动反应的发生的作用
B.每还原1molNO![]() 需氧化1molNH
需氧化1molNH![]() 和1molZn
和1molZn
C.成烟物质是两性氧化物小颗粒
D.成烟物质是小锌粒,它由NH4NO3反应放热而蒸出
10.设NA表示阿伏加德罗常数值,下列说法中正确的是( )
A.500 mL 1.0 mol/L的乙酸溶液中含有的H+数为0.5NA
B.1 mol苯分子中含有的碳碳双键数为3NA
C.1molCl2参加化学反应获得的电子数都是2NA
D.0.6 g CaCO3与Mg3N2的混合物中所含质子数为0.3 NA
11.化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语中,错误的是( )
A.钢铁腐蚀时可能发生的正极反应:2H2O + O2 + 4e-== 4OH一
B.硫化钠溶于水中 S2-+2H2O H2S+2OH-
C.硫酸亚铁溶液中加入过氧化氢溶液:2Fe2++H2O2+2H+=2Fe3++2H2O
D.1L 0.5mol·L-1稀硫酸与1L 1mol·L-1氢氧化钠溶液反应放出57.3kJ的热:H2SO4(aq)+2NaOH(aq) === Na2SO4(aq)+2H2O(1);ΔH=-57.3kJ/mol
12.在常温下100mLpH=10的KOH溶液中,加入pH=4的一元酸HA溶液至pH刚好等于
7,则对反应后溶液的叙述正确的是
A.V(混合液)≥200mL B.V(混合液)≤200mL
C.c(H+)= c(OH-)< c(K+)< c(A-) D.c(A-)= c(K+)
13.除去下列物质中所含杂质(括号内为杂质),选用的试剂或分离方法正确的是
| 混合物 | 试剂 | 分离方法 | |
| A | 亚硫酸钠(硫酸钠) | BaCl2溶液 | 过滤 |
| B | 二氧化碳(氯化氢) | 饱和NaHCO3溶液 | 洗气 |
| C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| D | 淀粉(氯化钠) | 蒸馏水 | 渗析 |
14.乙二酸,又称草酸,通常在空气中易被氧化变质,而其两分子结晶水(H2C2O4·2H2O)却能在空气中稳定存在。在分析化学中常用H2C2O4·2H2O做KMnO4的滴定剂,下列关于H2C2O4的说法正确的是( )
A.草酸是二元弱酸,其电离方程式为H2C2O4![]() 2H++C2O
2H++C2O![]()
B.草酸滴定KMnO4属于中和滴定,可用石蕊做指示剂
C.乙二酸可通过乙烯经过加成、水解、氧化再氧化制得
D.将乙二酸滴加到浓H2SO4上使之脱水分解,分解产物是CO2和H2O
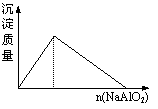
15.下列实验过程中产生的现象与对应的图形符合的是( )
 | |||
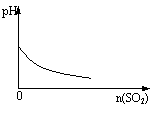 | |||
A、盐酸溶液中加入NaAlO2 B、SO2气体通入溴水中
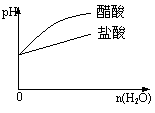 | |||
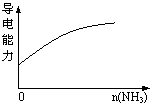 | |||
C、pH=2的醋酸与盐酸溶液分别加水稀释 D、氨气通入醋酸溶液中
16.要求设计实验证明,某种盐的水解是吸热的,下列回答正确的是
A. 将硝酸铵晶体溶于水,若水温下降,说明硝酸铵水解是吸热的
B. 在盐酸中加入相同浓度的氨水,若混合液温度下降,说明盐类水解是吸热的
C. 在醋酸钠溶液中加入醋酸钠晶体,若溶液温度下降,说明盐类水解是吸热的
D. 在醋酸钠溶液中滴入酚酞试液,加热后若红色加深,说明盐类水解是吸热的
17.已知当物质的量浓度相同时,碳酸中c(CO32-)比偏铝酸中c(AlO2-)大得多,则下列推论中正确的是
A. 通入适量CO2于AlO2-溶液中,有CO32-生成
B. 含CO32-的溶液容易使Al(OH)3溶解变成AlO2-
C. HCO3-只能与Al3+反应而不能和AlO2-反应
D. NH4+、AlO2-和HCO3-能大量共存于同一溶液中
18.近年来,加“碘”食盐较多使用了碘酸钾,KIO3在工业上可用电解法制取,以石墨和铁为电极,以KI溶液为电解液在一定条件下电解,反应式为KI+H2O→KIO3+H2↑。下列有关说法中,正确的是
A.电解时,石墨做阳极,铁作阴极 B.电解时,在阳极上产生氢气
C.电解后得到KIO3产品的步骤有:过滤→浓缩→结晶→灼烧
D.电解中,每转移0.6mol电子,理论上可得到0.1mol无水KIO3晶体
第Ⅱ卷(非选择题 共76分)
三、(本题包括两小题,共23分)
19.(10分)试回答下列中学化学实验室中常见仪器的有关问题:
(1)在仪器①分液漏斗、②试剂瓶、③集气瓶、④滴瓶、⑤滴定管、⑥容量瓶、⑦量筒、⑧托盘天平 中,标有“0”刻度的是(填序号,下同)__________________;标有使用温度的仪器是_________________________。
(2)“磨砂”是增加玻璃仪器密封性的一种处理工艺。在仪器 ①试管、②分液漏斗、③细口试剂瓶、④广口试剂瓶、⑤集气瓶、⑥滴瓶、⑦酸式滴定管、⑧碱式滴定管 中,用到“磨砂”的有______________________________。
 (3)在仪器①漏斗、②容量瓶、③蒸馏烧瓶、④分液漏斗、⑤烧杯、⑥蒸发皿
中,可用于粗盐提纯实验的有
;可用于分离两种沸点接近且互不相溶的液态混合物实验的有 。
(3)在仪器①漏斗、②容量瓶、③蒸馏烧瓶、④分液漏斗、⑤烧杯、⑥蒸发皿
中,可用于粗盐提纯实验的有
;可用于分离两种沸点接近且互不相溶的液态混合物实验的有 。
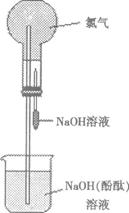
20.(13分)某研究性学习小组在做氯气的喷泉实验时(装置如图),发现含有酚酞的NaOH溶液喷入烧瓶后,溶液的红色褪去。甲、乙两位同学对此现象分别做了如下推测:
甲:因为氯气与NaOH溶液反应,使溶液碱性减弱甚至呈酸性.所以溶液红色褪去。乙:因为氯气溶于水并与水反应生成HClO.由于HClO的氧化漂白作用而使溶液褪色。
(1)验证甲同学的推测是否正确的方法是:_____________________________ .
验证乙同学的推测是否正确的方法是:_______________________________________
(2)如果将NaOH溶液改成酸性KMnO4溶液,把Cl2换成SO2气体,试问用图示所给装置完成喷泉实验是否合理?________________(填“合理”或“不合理”).
如果认为不合理,请说明你的理由________________________________________________________.
(3)类似“褪色喷泉实验”还有多种“变色的喷泉实验”,请你按实验要求,分别设计1个“变色喷泉实验”并填写下列表格:
| 编号 | 实验要求 | 烧杯中的溶液 | 滴管中的液体 | 烧瓶中的气体 |
| ① | 无色变红色喷泉 | H2O | ||
| ② | 红色变无色喷泉 | SO2 |
四、(本题包括两小题,共17分)
21.(5 分)A、B、C、D、E分别代表5种粒子,每种粒子中都含有18个电子。其中A和C都是由单原子形成的阴离子,B、D和E都是分子;又知在水溶液中A跟B反应可生成C和D;E具有强氧化性。请用化学符号表示上述5种粒子:
A ;B ;C ;
D ;E 。
22.(12分)物质的转化关系如下图所示(有的反应可能在水溶液中进行)。其中A为化合物,甲可由两种单质直接化合得到,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化。
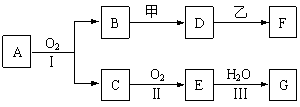 |
⑴若A为黄色固体,C能使品红试液褪色,D的水溶液中加入HNO3酸化的AgNO3溶液有白色沉淀生成。则
①工业上反应Ⅰ在_______________中进行,反应Ⅲ在_______________(均填设备名称)中进行。
②由两种单质直接化合得到甲的反应条件是___________或_____________。
③反应Ⅰ的化学方程式是______________________________________________。
⑵若甲为淡黄色固体,D、F的溶液均呈碱性,用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成。则
①甲的电子式是____________。
②D的溶液与乙反应的离子方程式是__________________________________。
③若1.7 g A与O2反应生成气态的B和C时放出22.67 kJ热量,写出该反应的热化学方程式:___________________________________________________________________。
五、(本题包括2小题,共18分)
23.(8分)有机物A与乙酸无论以何种比例混合,只要质量一定,完全燃烧后产生的水的质量也一定,试回答:
⑴若A与乙酸相对分子质量相等,且既能发生银镜反应又能发生酯化反应,则A的结构简式为_____________。
⑵若A有四种元素形成的两种官能团组成,相对分子质量与乙酸相等,且分子中氢原子都不与碳原子相连,则A的结构简式为_____________。
⑶若A分子中C、H元素质量分数之和为86.67%,其余为O,且A的相对分子质量小于200,则A的分子式为___________。如果A分子每个碳原子都达到饱和,且能与金属钠反应产生氢气,则A的结构简式为________________________。
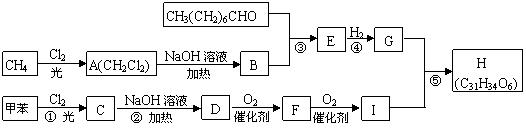
24.(10分)一种用于治疗高血脂的新药灭脂灵可按如下路线合成:
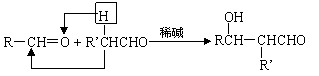 |
已知①
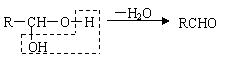 ②
②
又知G的分子式为C10H22O3,试回答:
⑴写出B、E的结构简式:B__________________,E________________。
⑵反应①~⑤中属于取代反应的有_____________。
⑶反应②方程式为______________________________________________。
⑷反应⑤方程式为______________________________________________。
六、(本题包括2小题,共18分)
25.(8分)某有机物A由C、H、O三种元素组成,其分子中有8个原子、46个质子,将其完全燃烧,在相同条件下测得产物CO2气体和水蒸气的体积比为2∶1。另取0.45 g有机物A恰好与10 mL 1 mol·L-1 NaHCO3溶液完全反应。
求: (1)有机物分子式。
(2)有机物结构简式。
26.(10分)将25.0 g胆矾晶体放在坩埚中加热测定晶体中结晶水的含量,固体质量随温度的升高而变化的曲线如下图。
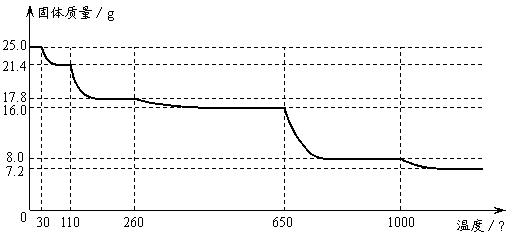 |
请认真分析上图,填写下列空白:
⑴ 30℃~110℃间所得固体的化学式是______________,650℃~1000℃间所得固体的化学式是_______________,温度高于1000℃后所得固体的化学式是______________;
⑵ 常温下无水硫酸铜____________(选填“可以”或“不可以”)用作干燥剂,进行硫酸铜晶体结晶水含量测定实验时,温度应控制在_________________范围内。
19.(各小题全对得2分、漏写得1分、不写或错写得0分)
⑴⑤⑧ ⑤⑥⑦ ⑵②③④⑤⑥⑦ ⑶①⑤⑥ ④⑤
20.(13分)
(1)取烧瓶中的无色溶液加入足量的NaOH溶液,如果溶液恢复红色,则可证明甲同学的推测是正确的;(2分)如果加入足量的NaOH溶液不能恢复红色,则说明乙同学的推测是正确的。(2分)
(2)不合理;(2分) KMnO4溶液可与橡胶塞反应,也不能盛放在倒置的胶头滴管中。(2分)
| 编号 | (其他合理答案照此给分) | |||
| ① | 酚酞试液 | NH3 | ||
| ② | NaOH(酚酞) | NaOH溶液 | ||
﹝3﹞共5分;②组烧杯中填NaOH(酚酞),得2分,其它每空1 分,填品红溶液不给分)
21.(5 分)
S2- HCl Cl- H2S F2 (各1分,5分)
22.⑴①沸腾炉 吸收塔 ②点燃 光照 ③4FeS2+11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
⑵
①Na+[![]() ]2-Na+ ② 2Al+2OH-+2H2O=2AlO2-+3H2↑
]2-Na+ ② 2Al+2OH-+2H2O=2AlO2-+3H2↑
③ 4NH3(g)+5O2(g)=4NO(g)+6H2O(g);ΔH=-906.8 kJ·mol-1
(每小题2分,共12分)
![]() 23.(共8分)⑴HO-CH2CHO ⑵ CO(NH2)2 ⑶ C8H8O -OH
23.(共8分)⑴HO-CH2CHO ⑵ CO(NH2)2 ⑶ C8H8O -OH
(每空2分,共8分)
24.(共10分)⑴HCHO ⑵①②⑤
⑶
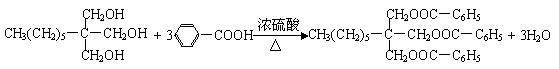 |
(每空2分,共10分)
25.(8分)解: 设有机物分子式CxHyOz
因为V(CO2)/V(H2O)=2/1 所以n(C)/n(H)=1/1 (1分)
根据题意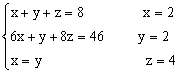 所以:分子式C2H2O4 (3分)
所以:分子式C2H2O4 (3分)
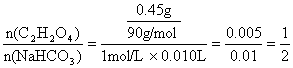 (1分)
(1分)
所以:有机物分子中含有两个羧基,有机物为二元羧酸,结构简式![]() (3分)
(3分)
26.⑴ CuSO4·3H2O CuO Cu2O (每空2分)
⑵ 可以 260℃~650℃ (每空2分)