高三化学化学反应速率化学平衡
★双基知识
1. 化学反应速率
(1)含义: (2)表示方法: (3) 单位:
(4)特点:①是平均速率,均取正值
②同一反应选用不同物质表示速率,数值可能不同
③各物质表示的速率比等于该反应方程式中化学计量数比
(5)影响因素:内因 外因(浓度、压强、温度、催化剂、其它)
2.化学平衡
(1)化学平衡的特征(定、动、变)
(2)影响化学平衡的因素(浓度、压强、温度)
(3)平衡移动原理(勒沙特列原理)
★巧思巧解
1.比较化学反应速率的方法
(1)将不同物质表示的的速率换算为用同一物质表示的速率,再比较大小
(2)比较不同物质表示的速率与对应计量系数比值的大小。
2.如何正确识别图象
(1)看图象:一看面(横轴和纵轴各表示什么)二看线(线的走向,变化趋势),三看点(是否过原点。线的交点及拐点),四看要不要作辅助线(如等压线、等温线)
(2)想规律:联想外界条件对化学平衡对化学反应速率和化学平衡的影响规律。
(3)作判断,依题意仔细分析并作出正确的判断。
★例题精析
[例1]:反应A+3B=2C+2D在四种不同情况下的反应速率分别为:
①V(A)=0.15mol/L・s ②V(B)=0.6mol/L・s
③V(C)=0.4mol/L・s ④V(D)=0.45mol/L・s
该反应进行的快慢顺序是:_____________________________
[例2]甲、乙两位同学在实验室做实验,分别看到如下现象,甲同学将Cu片投入到稀HNO3中发现开始气泡生成速率缓慢,一段时间后速率稍加快了一些;乙同学将KMnO4溶液(用稀H2SO4酸化)滴入到FeSO4溶液中,发现开始褪色较慢,后来非常快,请你用有关知识对甲乙两位同学的实验现象进行解释?
[例3]:在一定温度下,把2molSO2和1molO2通入一个一定容积的密闭容器中,发生如下反应:2SO2
+ O2 ![]() 2SO3 当此反应进行到一定程度时,反应混合物就处于化学平衡态。现在该容器中维持温度不变,令a、b、c分别代表初始加入的SO2 、O2和SO3 的物质的量(mol)。如果 a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的体积分数仍跟上述平衡时的完全相同,请填写下列空白。
2SO3 当此反应进行到一定程度时,反应混合物就处于化学平衡态。现在该容器中维持温度不变,令a、b、c分别代表初始加入的SO2 、O2和SO3 的物质的量(mol)。如果 a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的体积分数仍跟上述平衡时的完全相同,请填写下列空白。
(1)若a=0,b=0,则c=____________________
(2)若a=0.5,则b=________________和c=_________________
(3)a、b、c必须满足的一般条件是(请用两个方程式表示,其中一个只含a和c,另一个只含b和c)____________________________________________________。
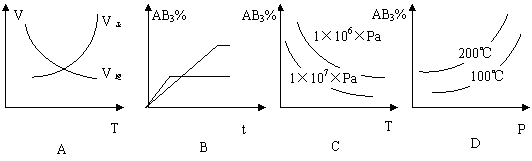 [例4]:对于可逆反应:A2(g)+3B2(g)
[例4]:对于可逆反应:A2(g)+3B2(g)![]() 2AB3(g);△H<0,下列图象正确的是:
2AB3(g);△H<0,下列图象正确的是:
| ||||
| ||||
[例5]I.恒温、恒压下,在一个可变容积的容器中发生如下反应:A(g) + B(g)![]() C(g)
C(g)
(1)若开始时放入1molA和1molB,达到平衡后,生成amolC,这时A的物质的量为______________mol
(2)若开始时放入3molA和3molB,达到平衡后,生成C的物质的量为__________mol
(3)若开始时放入x mol A、2molB和1molC,达到平衡后,A和C的物质的量分别是y mol和3a mol,x=____________mol 、y=_____________mol
平衡时,B的物质的量__________________(选填一个编号)
(甲)大于2mol
(乙)等于2mol
(丙)小于2mol
(丁)可能大于、等于或小于2mol
作出此判断的理由是:________________________________________________
(4)若在(3)的平衡混合物中再加入3 mol C,待再次达平衡后,C的质量分数是____________________
Ⅱ.若在维持温度不变,在一个与(1)反应前起始体积相同,且容积固定的容器中发生上述反应。
(5)开始时放入1mol A和1molB达到平衡后,生成b mol C,将b与(1)小题中的a进行比较____________________(选填一个编号)
(甲)a<b (乙)a>b
(丙)a=b (丁)不能比较a和b的大小
作出此判断的理由是__________________________________________________________
例题解答:
例1 ④>③=②>①
例2Cu与HNO3反应放热,使体系的温度升高;生成的Mn2+作催化剂。
例3(3)a+c=2 b+c/2=1
例4 B
例5(1)(1-a) (2)3a
(3)2, 3-3a, 丁
若3a>1,B的物质的量小于2 mol
若3a=1,B的物质的量等于2 mol
若3a<1,B的物质的量大于2 mol
(4)a/(2-a)
(5)乙;因为(5)小题中容器容积不变,而(1)小题中容器的容积缩小,所以(5)小题的容器中的压强小于(1)小题容器中的压强,有利于逆向反应,故反应达到平衡后,a>b。