�����ֳ����Ľ���������߿���
15���������ʵ�����þ��������,ȡ�������û�����ķ�,�ֱ�ӵ�������������Һ��,��ַ�Ӧ��,�ų�����������(���� )
(A)��3Ħ/��HCl�� �������������������� (B)����4Ħ/��HNO3
(C)��8Ħ/��NaOH������ ���������������� (D)�� 18Ħ��H2SO4
21.0.1Ħþ�۷ֱ���������O2��CO2��N2��ȼ��,���ɹ������������ΪW1��W2��W3.���й�ϵʽ��ȷ����(���� ).
(A)��W2>W1>W3���� ������������������ (B)�� W1=W2>W3
(C)��W1=W2=W3����������������������(D)�� W3>W2>W1
26������Fe��FeO��Fe2O3��ɵĻ�����м���100����2Ħ/�������ᣬǡ��ʹ�������ȫ�ܽ⣬���ų�448�������壨��״��������ʱ��Һ����Fe3+���ӡ��������ж���ȷ����
A����������������ʷ�Ӧʱ������������ʵ���֮��Ϊ1��1��3
B����Ӧ��������Һ�е�Fe2+������Cl- ���ӵ����ʵ���֮��Ϊ1��2
C��������FeO�����ʵ�����ȷ������Fe��Fe2O3�����ʵ�����
D��������Fe2O3�����ʵ�����ȷ������Fe��FeO�����ʵ�����
14������м���ڹ���������ټ����������ʣ��������������ɵ���
������ ��A�����ᡡ���������������� B����ˮ�������� �� C������п����������������������D���Ȼ�ͭ����
20����п����������þ���ֽ����е�������ɵĻ����10�ˣ������������ᷴӦ�����������ڱ�״����Ϊ11.2������������һ�����еĽ�����
������ ��A��п�������������� B���������������������� C���������������������� D��þ
25���ڶ�����Ԫ��R�ĵ��ʼ�����Ӧ������Ļ����12g��������ˮ����ȫ��Ӧ�����ɣ��ù���16g�����Ʋ��Ԫ�ؿ���Ϊ
A��Mg���������� B��Ca���������� C��Sr������������ D��Ba
18���ס������ձ��и���ʢ��100mL 3mol/L�����������������Һ�������ձ��зֱ��������������ۣ���Ӧ�����������ɵ����������Ϊ�ף���=1��2����������۵�����Ϊ
A��5.4g ����������B��3.6g���������� C��2.7g��������������D��1.6g��
2����ͭп�Ͻ��Ƴɵļٽ�Ԫ����ƭ���˵��¼����з��������в�����������α�ķ�����
(A)�ⶨ�ܶȡ������� (B)���������С����� (C)���������С���������(D)�۲����
��22.��ӡˢ��·ʱ�����Ȼ�����Һ��Ϊ����ʴҺ���������ķ�ӦΪ2FeCl3+Cu��2FeCl2+CuCl2����ʢ���Ȼ�����Һ���ձ���ͬʱ�������ۺ�ͭ�ۣ���Ӧ���������н�������ܳ��ֵ���
��A. �ձ�����ͭ���� ����������������������B. �ձ���������ͭ
��C. �ձ�������ͭ���� ��������������������D.�ձ�������ͭ���ޣ�14���Ȼ�����Һ����������������еĹ�ͬ������
A����ɢ�ʿ���ֱ������l��100nm֮�䡡�� B��������Ĥ
C���������ɡ����պ������������ɡ��� D���ʺ��ɫ
7������˵����ȷ����
����A��Ӳˮ��ָ���кܶ��εĺ�ˮ
����B����ˮ��ָ�ܶȴ��Һ̬H2O
����C����ˮ��ָ���ˮ��Һ
����D����ˮ��ָ3���Ũ�����1���Ũ����Ļ��Һ
8��������ұ����̼�ظ�Ҫ�������Ҫ������
����A����ȥ�����еĸ������ʣ��������ᴿ
����B���ʵ�����������ĺ�̼������ȥ�������к�����
����C���û�ԭ�������������ﻹԭ����
����D������Ͻ�Ԫ�ظ�����������
16������Ѫ�쵰���к���Fe2�����ӣ������ʳ�������Σ���ʹ���ж�����Ϊ�������λ�ʹFe2������ת���Fe3�����ӣ����ɸ���Ѫ�쵰��ɥʧ��O2��ϵ�����������ά����C�ɻ����������ε��ж�����˵��ά����C����
A�����ԡ���B�����ԡ���C�������ԡ���D����ԭ��
12����������������þ�Ļ����Һ�У���μ���ϡ����������Һ��ֱ�����������б�ʾ��������������X������Һ�г����������Y���Ĺ�ϵʾ��ͼ����ȷ���ǡ���
Y���������������� Y�������������� Y�������������� ��Y
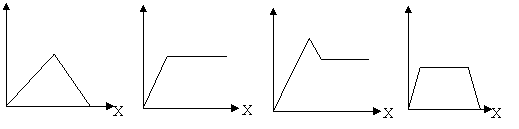 |
A������������������ B���������������� C���������������� D
9�����ó���������ˮ��ϴ���ú��ֺ���ɫ����ߣ��ڴ˱仯�������������Ļ�ѧ��Ӧ��
A��4Fe(OH)2��2H2O��O2��4Fe(OH)3��������B��2Fe��2H2O��O2��2Fe(OH)2��
C��2H2O��O2��4e����OH�������������� ���������� D��Fe��3e��Fe3��
8�����ֱ���������ϡ���������������Һ��Ӧ����������Ӧ�ų�����������ͬ״����������ʱ����Ӧ�����ĵ�HCl��NaOH���ʵ���֮��Ϊ
��A��1:1���������� B��2:1������������ C��3:1������������ D��1:3
16������������ȫ�ۻ�������������������Һ�У����ᷢ����Ӧ���ǡ�����
A��ϡ���ᡡ���� ������ B��ϡ���ᡡ������C������ͭ������ ������ D����������
36.���۸��������ж�,������ˮҪ����ѧ����������ŷ�,���������̷�(FeSO4��7H2O)�ѷ�ˮ�е����۸���ԭΪ���۸�����,�ټ��������ʯ��ˮ,ʹ������ת��Ϊ��������Cr(OH)3����.����Ҫ��Ӧ�Ļ�ѧ����ʽ����:H2Cr2O7+6FeSO4+6H2SO4=3Fe2(SO4)3+Cr2(SO4)3+7H2O
�����Ϸ�����1��104������(+6��)78����/���ķ�ˮ(Cr���ԭ������52),�Իش�:
(1)������,�������г�Cr(OH)3��,������������������(�û�ѧʽ��ʾ).
(2)�����̷�����ǧ��?
37.����AlCl3��FeCl3�����Һ,����Al3+��Fe3+�����ʵ���֮��Ϊ0.1Ħ,�ڴ���Һ�м���90����4Ħ/����NaOH��Һ,ʹ���ַ�Ӧ.��Al3+���ʵ����������ʵ����ı�ֵΪx.
(1)���ݷ�Ӧ�Ļ�ѧ����ʽ����x=0.4ʱ,��Һ�в����ij�����ʲô?���ʵ����ж���?
�� (2)���������ֻ��Fe(OH)3��xȡֵ��Χ.
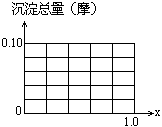
������ͼ�л�����������(Ħ)��x(0��1)�仯������.
(3)��Al3+��Fe3+���ʵ���֮��ΪAĦ(AΪ������ֵ),������������ʱ,�������ͬʱ��Fe(OH) 3��Al(OH) 3��xȡֵ��Χ�����������ʵ���(�ú���A��x��ʽ�ӱ�ʾ
27��������(Na2FeO4)��ˮ����������ʹ�õ�һ�����;�ˮ�����������Աȸ�����ظ�ǿ�������ڷ�Ӧ�б���ԭΪFe3+���ӡ���ƽ��ȡ�����ƵĻ�ѧ����ʽ��Fe(NO3)+NaOH+Cl2��Na2FeO4+NaNO3+NaCl+H2O
��Ӧ������ Ԫ�ر�������ת�Ƶ�������Ϊ����������
������֮�����ܾ�ˮ�������������⣬��һ��ԭ������������������������������
24�����ȵ�ϡ������Һ���ܽ���11.4g FeSO4��������50mL 0.5mol/L KNO3��Һ��ʹ����Fe2+��ȫ��ת����Fe3+��KNO3Ҳ��Ӧ��ȫ������NXOY�������������ݳ���FeSO4 + KNO3 + H2SO4 ��K2SO4 +Fe2(SO4)3+ NXOY+H2O
��1�������X=�������� Y=����������
��2����ƽ�û�ѧ����ʽ��ϵ����д����ʽ�����ڣ�
��3����Ӧ��������Ϊ����������
��4���ö��ߺͼ�ͷ�������ת�Ƶķ��������
32.(6��)ȡһ��þ�����������ڵ�ȼ���õ�����þ�͵���þ������������Ϊ0.470g��ȴ���������ˮ������Ӧ����������ɲ����գ��õ�������þ����Ϊ0��486 g��
����(1)д������þ��ˮ��Ӧ����������þ�Ͱ��Ļ�ѧ����ʽ��
����(2)����ȼ�����û�����е���þ������������
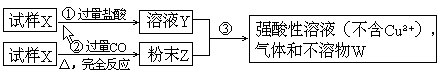 30.(5��)����X����������������ͭ���.ȡ������ȵ�������������ͼ��ʾ����ʵ��:
30.(5��)����X����������������ͭ���.ȡ������ȵ�������������ͼ��ʾ����ʵ��:
(1)��д�����������������ȫ����Ӧ�����ӷ���ʽ.
(2)��ȫ������ҺY��ȫ���ķ�ĩZ��ַ�Ӧ��,���ɵIJ�����W��������m,��ÿ������X������ͭ������Ϊ_____________.(��m��ʾ)
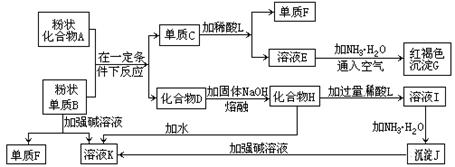 28.(8�֡���ʾ��ijЩ����������������ռӦ�������Ρ��������»�ѧ��Ӧ��ͼ��գ�
28.(8�֡���ʾ��ijЩ����������������ռӦ�������Ρ��������»�ѧ��Ӧ��ͼ��գ�
��
(1)����F��_____________________��
����(2)д����E����G�����ӷ�Ӧ����ʽ����ѧ����ʽ��________________��
����(3)��ҺI����������������_____________________��
����(4)��C��E��F������Ũ�ᣬ����ѡ�õ�Ũ���ǣ�д����ʽ��__________��
29.�ҹ��涨����ˮ�����������������Ҫ��
| PHֵ | 6.5-8.5 |
| Ca2+,Mg2+��Ũ�� | <0.0045mol/L |
| ϸ������ | <100��/mL |
������Դˮ����������ˮ�Ĺ�������ʾ��ͼ
|
|
|
|
|
���������������� ��
Դˮ�к�Ca2+��Mg2+��![]() ��CL-�ȣ�����ʯ�Һ�����Ca(OH)2,�����������ɸ��ֽⷴӦ��д������һ�����ӷ���ʽ_____________
��CL-�ȣ�����ʯ�Һ�����Ca(OH)2,�����������ɸ��ֽⷴӦ��д������һ�����ӷ���ʽ_____________
���ۼ���ȥ������������Ĺ���__________����д��ţ���ѡ���ۣ�
��ֻ���������̡�����ֻ�ǻ�ѧ���̡��� ���������ͻ�ѧ����
FeSO4��7H2O���õ����ۼ�������ˮ����������___________������
ͨ�������̼��Ŀ����_________________��_____________��
����A��������__________�����������ǻ�������A��ˮ��Ӧ�IJ������______________�ԡ�
���������У�______________������Ϊ����A�Ĵ���Ʒ������д��ţ���ѡ���ۣ�
��Ca(ClO)2����������NH3(Һ)��������K2FeO4������ ��SO2
31����֪Fe2O3�ڸ�¯�������з�Ӧ��Fe2O3��CO��2FeO��CO2
��Ӧ�γɵĹ������Fe2O3��FeO���У�Ԫ������������������ mFe�UmO��ʾ��
��1���������������У�mFe�UmO�������������� ��ѡ�� a��b��c��ѡ�۷֣�
��a��21�U9��������b��21�U7.5������ ��c�� 21�U6
��2����mFe�UmO��21�U8������Fe2O3��CO��ԭ�İٷ���
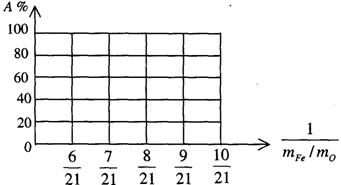 ��3���� Fe2O3��CO��ԭ�İٷ���ΪA������A���ͻ������mFe�UmO�Ĺ�ϵʽΪ���ú�mFe��mO�Ĵ���ʽ��ʾ����
��3���� Fe2O3��CO��ԭ�İٷ���ΪA������A���ͻ������mFe�UmO�Ĺ�ϵʽΪ���ú�mFe��mO�Ĵ���ʽ��ʾ����
A����������������������������������
������ͼ�л���A%��mFe/mO��ϵ��ͼ�Ρ�
��4����� Fe2O3��CO�ķ�Ӧ���������У�
3Fe2O3��CO��2Fe3O4��CO2
Fe3O4��CO��3FeO��CO2
�Է�����Ӧ�γɵĹ���������ܵ���ɼ���Ӧ��mFe�UmO����mFe�UmO��21�Ua��д��a��ȡֵ��Χ��������������±���
| �������ɣ��û�ѧʽ��ʾ�� | a��ȡֲ��Χ |
22����10�֣���֪XΪFeO��CuO�Ļ���ȡ���ݵ�������X��Ʒ��������ʵ�飺
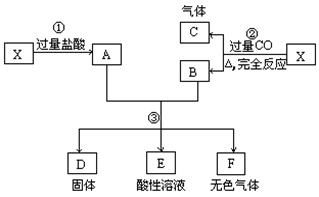 ��1��д���١��ں͢۲����з�Ӧ�Ļ�ѧ����ʽ��
��1��д���١��ں͢۲����з�Ӧ�Ļ�ѧ����ʽ��
�������������������������������������������������������������������������������������������������������������������������������������������������������� ��������������������������������������������������������������������������������������������������������������������������������������������������������������������
��2����Ӣ۲����ù���D������Ϊ32 g����ҺE��ֻ����һ�ֽ������ӣ�����F�ڱ�״�������Ϊ5.6 L���Լ���ȡ�õ�ÿ��X��������X��FeO��CuO�������ȡ�
31������������¿�������������������4FeS2��11O2��8SO2��2Fe2O3
�������N2��O2�ĺ����ֱ�Ϊ0.800��0.200������������������庬���������������ʾ������������и��⣺
��1��1.00mol FeS2��ȫ��������Ҫ�������������״����Ϊ��������L
��2��55L����������FeS2��ȫ��Ӧ�����������ͬ��ͬѹ����Ϊ��������L
��3���ÿ�������FeS2���������������У�O2�ĺ���Ϊ0.0800������SO2�ĺ�����
��4����FeS2������������������Ϊ100L������O2ΪaL��SO2ΪbL��
�� д��a��b�Ĺ�ϵʽ
�� ����ͼ�л���a��b�Ĺ�ϵ���ߣ�FeS2����ʱ����������20%��
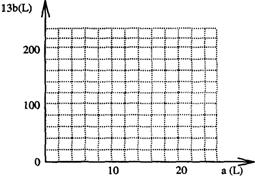 ˵����Ϊ������ͼ����������13b��ʾ
˵����Ϊ������ͼ����������13b��ʾ
 33����22�֣����������ַ��������Ƶð�ɫ��Fe(OH)2������
33����22�֣����������ַ��������Ƶð�ɫ��Fe(OH)2������
����һ���ò���Fe3����FeSO4��Һ���ò���O2������ˮ���Ƶ�NaOH��Һ��Ӧ�Ʊ���
��1������������������������FeSO4��Һʱ����������������� ��
��2����ȥ����ˮ���ܽ��O2������������ �ķ�����
��3�����ɰ�ɫFe(OH)2�����IJ������ó��ι���ȡ����O2��NaOH��Һ������FeSO4��ҺҺ���£��ټ���NaOH��Һ������������������������������������ ��
������������ͼװ���У���NaOH��Һ����м��ϡH2SO4���Լ��Ʊ���
��1�����Թܢ��������Լ������������� ��
��2�����Թܢ��������Լ������������� ��
��3��Ϊ���Ƶð�ɫFe(OH)2���������Թܢ�͢��м����Լ�����ֹˮ�У��������Ӻ��ʵ�鲽�������������������������� ��
��4���������ɵ�Fe(OH)2�����ܽϳ�ʱ�䱣�ְ�ɫ���������� ������������ ��
30����ϸ��������ĩ���㷺Ӧ���ڴ��ģ���ɵ�·��������������ȡԭ��Ϊ��Al2O3��N2��3C![]() 2AlN��3CO���ڷ�Ӧ����ȫ����������Ʒ����������̿�����������ʡ�Ϊ�ⶨ�ò�Ʒ���йسɷֵĺ�������������������ʵ�飺
2AlN��3CO���ڷ�Ӧ����ȫ����������Ʒ����������̿�����������ʡ�Ϊ�ⶨ�ò�Ʒ���йسɷֵĺ�������������������ʵ�飺
��1����ȡ10.00g��Ʒ��������������NaOHŨ��Һ�й��Ȳ����ɣ�AlN��NaOH��Һ��Ӧ����NaAlO2�����ų�����3.36L����״������
��������Ӧ�Ļ�ѧ����ʽΪ������������������ ��
�ڸ���Ʒ�е�A1N����������Ϊ�������� ��
��2����ȡ10.00g��Ʒ���ڷ�Ӧ���У�ͨ��2.016L����״����O2���ڸ����³�ַ�Ӧ����������ܶ�Ϊ1.34g��L��1��������ɱ�״����AIN����O2��Ӧ��������Ʒ�к�����̿�������� g��
26����12�֣�
������ ��ȸʯ��ʯ������Ȼ����ڵ�����̼������ͭ�����ǵĻ�ѧ��ɿɱ�ʾΪ��
xCuCO3��yCu(OH)2(x��y��������![]() )
)
��1����ȸʯ��ʯ��ֱ���������ᷴӦʱ����ȸʯ���õ���������ʵ��������ɵ�CO2�����ʵ���֮��Ϊ4��1��ʯ����Ϊ3��1�����������ǵĻ�ѧ��ɡ�
��ȸʯ������������������������ ��ʯ�ࣺ������������������������ ��
��2�����п�ȸʯ��ʯ������Ʒ��ȡ���ݵ���������Ʒ����һ���м���������ᣬ����CO23.36L����״���£���������һ����Ʒʹ����ȫ�ֽ⣬�õ�CuO 20g����ͨ������ȷ��
�û�����п�ȸʯ��ʯ������ʵ���֮�ȡ�
��04�Ϻ���31����ͭ����Ҫ�ɷ�CuFeS2������ȡͭ����Ҫԭ��
��1��ȡ12��5g��ͭ����Ʒ�����ⶨ��3��60g�����ʲ�����������CuFeS2����Ϊ
|
��2����֪ 2CuFeS2 + 4O2 ������������Cu2S + 3SO2 + 2FeO (¯��)
����Cu2S��1200������°������Ӧ��
2Cu2S + 3 O2 �� 2Cu2O + 2 SO2
2 Cu2O + Cu2S �� 6Cu + SO2
�ٶ�������Ӧ����ȫ��������м��㣺
����6 mol CuFeS2����6 mol Cu��������O2�����ʵ���
��6 mol CuFeS2��14��25 mol O2��Ӧ�������Ͽɵõ�����Ħ��ͭ
��6 mol CuFeS2��15��75 mol O2��Ӧ�������Ͽɵõ�����Ħ��ͭ