高三化学单元测试
《氧族元素、环境保护》单元测试
第Ⅰ卷(选择题,共74分)
一、选择题(本题包括8小题,每小题3分,共24分。每小题只有1个正确选项符合题意。)
1、下列关于某些社会热点问题的说法中,错误的是
A.光化学烟雾的产生与人为排放氮氧化物有
B.臭氧空洞的形成与氟氯烃或氮氧化物泄漏到大气中有关
C.甲醛是某些劣质装饰板材释放的常见污染物之一
D.禁止使用含铅汽油是为了提高汽油的燃烧效率
2.下列各组气体中,在通常状况下能共存,并且都能用浓硫酸干燥的是
A.SO2、H2S、Cl2 B.NO、O2、HBr
C.HCl、HBr、HI D.SO2、CO2、O2
4、下列各组微粒是同素异形体的是
A、![]() 与
与![]() B、D2O与T2O C、O2与O3 D、甲烷与乙烷
B、D2O与T2O C、O2与O3 D、甲烷与乙烷
5、关于SO2和SO3的说法错误的是:①都是酸酐,②与水化合都能生成相应的酸,③都能与碱反应生成正盐或酸式盐,④标准状况下都是气体,⑤都有还原性
A.①④ B.④⑤ C.③⑤ D.②③
6、某无色气体可能含有H2S、SO2、CO2、HI、HCl气体中的一种或几种。将气体通入氯水后,得无色溶液,向该溶液中滴加氯化钡溶液,有白色沉淀产生。则下列叙述正确的是
A.该气体中肯定含有H2S和SO2 B.该气体中肯定含有SO2
C.该气体中肯定含有CO2和SO2 D.该气体中肯定含有H2S、CO2和HI
7、用10 mL的0.1 mol/L BaCl2溶液恰好使相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液中的
硫酸根离子完全转化成硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是
A. 3︰2︰2 B. 1︰2︰3 C. 1︰3︰3 D. 3︰1︰1
8、实验室将NaClO3和Na2SO3按分子个数比为2∶1倒入烧瓶中,同时滴入适量硫酸,并用
水浴加热,产生棕黄色的气体X,反应后测得NaClO3和Na2SO3恰好完全反应,则X为
A.Cl2 B.Cl2O C.ClO2 D.Cl2O3
二、选择题(本题包括10小题,每小题5分,共50分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给满分,但只要选错一个该小题就为0分。)
9、在下列反应中,浓硫酸既表现氧化性,又表现酸性的是
A.FeO+H2SO4(浓) B.Cu+H2SO4(浓)
C.C+H2SO4 (浓) D.CuO+H2SO4 (浓)
10、某溶液中含HCO3-,SO32-,CO32-,CH3COO-等四种阴离子,向其中加入足量的Na2O2固体后,溶液中离子的浓度基本保持不变的是
A.CH3COO- B.SO32- C.CO32- D.HCO3-
11、a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化:![]()
其中: a是单质;b是气体;c、d是氧化物;e是最高价氧化物对应的水化物。则a可能是
A、Cl2 B、N2 C、S D、C
12、有一FeSO4、Fe2(SO4)3的混合物,经测定其中含硫质量分数为22.73%,则此混合物中Fe元素的含量为
A.31.81% B.68.19% C.22.73% D.45.46%
13、设NA为阿伏加德罗常数。下列说法正确的是
A、标准状况下,22.4 L SO3所含分子数为NA
B、常温常压下,16 g O2和O3的混合气体所含氧原子数为NA
C、25℃时,1 L pH=1的稀硫酸中约含2NA个H+
D、密度不等,质量分别为16 g和32 g的O2和SO2所含分子数相同,为NA个
14、在含大量I-的溶液中,因发生氧化还原反应而不能大量共存的时是
A、Mg2+、Ca2+、HCO3—、Cl— B、Na+、AlO2—、Cl—、SO42—
C、K+、Fe3+、SO42—、S2— D、H3O+、Ca2+、Cl—、NO3—
15、下列书写的离子方程式中正确的是
A.向次氯酸钙溶液中通入少量的SO2 Ca2++2ClO-+SO2 CaSO3↓+2HClO
B.向氨水中通入足量SO2
2NH3·H2O+SO2
2NH4++SO32-+H2O
C.向硫酸铁溶液中通入H2S
2Fe3+ +S2- S↓+2Fe2+
D.向溴水中通入SO2
Br2+2H2O+SO2
4H++SO42-+2Br-
16、有一瓶Na2SO3溶液,由于它可能部分被氧化,某同学进行如下实验:取少量溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀。对此实验下述结论正确的是
A.Na2SO3已部分被空气中的氧气氧化
B.加入Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4
C.加硝酸后的不溶沉淀一定是BaSO4
D.此实验不能确定Na2SO3是否部分被氧化
17、在1000 mL含有等物质的量的HBr和H2SO3溶液中通入0.01 molCl2,有一半Br-变为Br2,原溶液中HBr和H2SO3的浓度都等于
A.0.0075 mol·L-1 B.0.008 mol·L-1 C.0.075 mol·L-1 D.0.08 mol·L-1
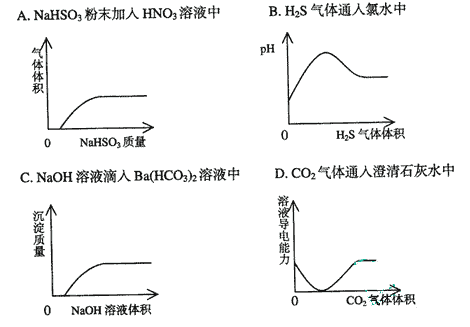
18、下列实验过程中产生的现象与对应的图形相符合的是
选择题答案:
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | ||
| 答案 | ||||||||||
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 答案 |
第Ⅱ卷(非选择题,共76分)
三、(本题包括2小题)
19、(1)新浪网曾经报道,重庆开县发生特大井喷事故,造成大量人员牲畜伤亡。其中罪魁祸首是喷出大量的有毒气体H2S,为了解毒,政府采用了点燃的方法,写出完全燃烧化学方程式_____________________ _______,但是会造成空气污染,易形成_______ __________。
(2)央视《每周质量报告》曾报道有些不法商贩用硫磺熏蒸银耳、生姜、粉丝等食品,可使食品雪白光亮。有些使用工业H2O2,使果肉雪白鲜嫩来制果冻。以上硫磺熏蒸利用生成的________的漂白性,使用工业H2O2利用了H2O2的漂白性,但二者的原理不同,前者是因为__________________而使物质漂白,后者则是双氧水的_______性而使物质漂白。
20、2003年8月4日在齐齐哈尔市发生了侵华日军遗留的芥子气毒气罐泄漏伤人事件。芥子气,化学名为二氯二乙硫醚,是微黄色或无色的油状液体,具有芥子末气味或大葱、蒜臭味。芥子气的化学式为:(ClCH2CH2)2S
(1)芥子气可用两种方法制备。其一是ClCH2CH2OH与Na2S反应,反应产物之一接着与氯化氢反应;其二是CH2=CH2与S2Cl2反应,反应物的物质的量之比为2:1,试写出反应的化学方程式:
、 ;
(2)碱液可以解毒,写出化学方程式:
(3)对局部中毒,如皮肤上的毒液,可立即采用什么措施进行简单的处理
A.用可溶解芥子气的溶剂如酒精 B.用漂白粉,双氧水浸润的棉球吸去毒液
C.用浓NaOH 溶液浸润的棉球擦洗 D.将中毒局部的皮肤割除
四、(本题包括2小题)
21、工业上测量SO2、N2、O2混合气体中SO2含量的装置如下图;反应管中装有碘的淀粉溶液。SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O H2SO4+2HI
⑴ 混合气体进入反应管后,量气管内增加的水的体 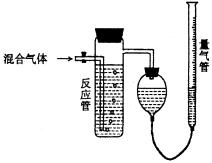 积等
积等
于 的体积(填写气体的分子式)
⑵ 反应管内溶液蓝色消失后,没有及时停止通气,则测
得的SO2含量 (选填:偏高,偏低,不
受影响)
⑶ 反应管内的碘的淀粉溶液也可以用 代替
(填写物质名称)
⑷ 若碘溶液体积为Va mL,浓度为c mol·L-1,N2与
O2的体积为Vb mL(已折算为标准状况下的体积)。用C、Va、Vb表示SO2的体积分数
为: 。
⑸ 将上述装置改为简易实验装置,除导管外,还需选用的仪器为 : (选下列仪器
的编号) a.烧杯 b.双孔塞 c.广口瓶 d.容量瓶 e.量筒 f.单孔塞
22、某同学运用已有的Na2O2和CO2反应的知识进行迁移,认为Na2O2也可和SO2反应,反应式可能为:2Na2O2+2SO2
2Na2SO3+O2,为此设计如下一套装置,来验证Na2O2和SO2的反应产物。
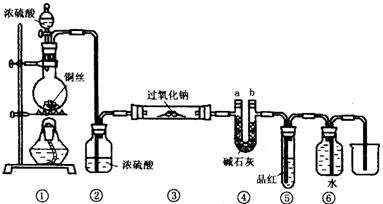
如图安装仪器,检查装置气密性后添加药品并滴入适量浓硫酸。回答下列问题:
(1)点燃①处酒精灯,不久,观察到①处产生大量气体;③处两通管管壁发热,管内药品的
颜色变化为色逐渐变为 色。
(2)在反应过程中如何用较简便的操作证明反应产生了O2?
_______________________________________________________________________________
(3)⑤处用排水法收集气体,从什么现象可证明收集的气体中已不含SO2?
_______________________________________________________________________________
(4)待反应结束后,取两通管内少量固体,装入试管中,加水溶解时未产生气体,如何证
明产物中有Na2SO3?
_______________________________________________________________________________
(5)待反应结束后,取两通管内少量固体,装入试管中,加入足量盐酸溶液,再加入氯化钡
溶液,有白色沉淀生成,试分析产生沉淀的原因。
_______________________________________________________________________________
五、(本题包括2小题)
23、据著名网站-网易报道,意大利科学家使用普通氧分子和带正电的氧化离子作用,制出了
新型的氧分子O4,它的结构很复杂,可能具有与S4相似的长方形结构。
(1)下列有关O4的说法正确的是
A、O4分子内存在极性共价键
B、合成O4的反应可看作核聚变反应,即不属于化学变化
C、O4与O3、O2都是氧的同素异形体
D、O4将来可用作更强有力的火箭推进的氧化剂
(2)制备O![]() 、O
、O![]() 甚至O
甚至O![]() 的化合物是可能存在的,通常它们是在氧分子进行下列各种反应时生成的:
的化合物是可能存在的,通常它们是在氧分子进行下列各种反应时生成的:
|
|
|
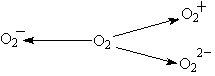
上述反应中, (填序号)相当于氧分子的氧化; (填序号)相当于氧分子的还原。
(3)写出O22-的电子式: 。
(4)O2[PtF6]是一种含有O![]() 的化合物,请写出一种含有O
的化合物,请写出一种含有O![]() 的氧化物的化学式:
的氧化物的化学式:
2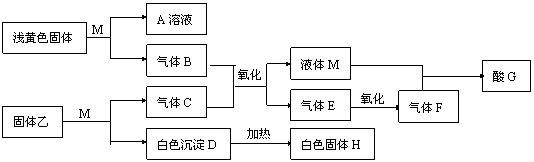 4、M为一种常见的液体试剂。下列物质在一定条件下可发生如下图所示的转化关系。
4、M为一种常见的液体试剂。下列物质在一定条件下可发生如下图所示的转化关系。
试填写题中空白:
⑴ 若固体乙是硫化铝,试回答:
①C、E、F化学式C 、E 、F
②E→F的化学方程式
③D溶解于A溶液的离子方程式
⑵若白色沉淀D不能溶解于A溶液,气体C能使湿润的试纸变蓝,回答:
④固体乙可能
⑤B+C→M+E的化学方程式
六、(本题包括2小题)
25、有一因储存时间长而变质的亚硫酸钠样品,称取0.200 g 此样品溶于水,加入用盐酸酸化的氯化钡溶液10.0 mL,恰好完全反应,产生的沉淀经过过滤、洗涤、干燥后称得质量为0.233g。求:
①样品中亚硫酸钠的质量分数;
②所用氯化钡溶液的物质的量浓度。
26、NaHSO3和KHSO3的固体混合物1.12 g跟100 mL盐酸反应,若NaHSO3和KHSO3的物质的量相同:
①欲求标准状况下生成SO2的体积,还需要什么数据? 。(在讨论②的问题中,该数据可用a表示)
②讨论:a值的变化对产生SO2体积(标准状况)的影响。(表格可不填满,也可自己添加)
| a的取值范围 | 生成SO2的体积(L) |
高三化学单元测试
《氧族元素、环境保护》单元测试答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | ||
| 答案 | D | D | D | C | B | B | C | C | ||
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 答案 | AB | A | BC | A | BD | CD | D | CD | D | D |
三、(本题包括2小题)
19、(1)2H2S+3O2 2SO2+2H2O 酸雨(2)SO2 化合生成无色不稳定物质 氧化性
20、(1)2ClCH2CH2OH+Na2S (HOCH2CH2)2S+2NaCl
(HOCH2CH2)2S+2HCl (ClCH2CH2)2S+2H2O
2CH2=CH2+S2Cl2→(ClCH2CH2)2S+S
(2)(ClCH2CH2)2S+2NaOH→2NaCl+(HOCH2CH2)2S(3)AB
四、(本题包括2小题)
21、(1)N2、O2的体积 (2)偏低 (3)酸性高猛酸钾溶液或溴水
(4)22.4cVa/(22.4cVa+Vb)(其它合理答案也给分)(5)bceg或beg或ceg
22、(1)淡黄;白
(2)打开④处U型管a处橡皮塞,插入带火星的木条,如果带火星的木条复燃,说明产生了氧气
(3)③处品红溶液不褪色,说明氧气中不混有二氧化硫
(4)向该溶液中加入稀盐酸,有气体产生
(5)由于过氧化钠有氧化性,反应过程中有部分亚硫酸钠被氧化为硫酸钠,和氯化钡反应产生难溶于盐酸的硫酸钡
 五、(本题包括2小题)
五、(本题包括2小题)
23、(10分)(1)CD(2)②;①③(3)[: O : O :]2- (4)KO2
|
![]() ② 2 SO2 + O2
2SO3③Al(OH)3+OH-
② 2 SO2 + O2
2SO3③Al(OH)3+OH- AlO2-+2H2O
(2) ④Mg3N2 ⑤ 4NH3+5O2 4NO+6H2O (2分)
六、(本题包括2小题)
25、(1)n(BaSO4)=0.001mol=n(Na2SO4)故m(Na2SO4)=0.142g所以,w(Na2SO4)=0.142/0.200=71%,于是:w(Na2SO3)=1-w(Na2SO4)=29%
(2)n(BaSO4)=0.001mol=n(BaCl2),所以c(BaCl2)=0.001mol/10mL=0.1mol/L
26、(1)盐酸的物质的量浓度
(2)
| a的取值范围 | 生成SO2的体积(L) |
| 0<a<0.1 | 2.24a L |
| a≥0.1 | 2.24 L |