高考化学复习无机物的综合推导专题
东山区教育发展中心教研部 化学科
|
|
|
甲、![]()
![]()
![]()
![]() 乙是两种常见的化合物,这些单质和化合
乙是两种常见的化合物,这些单质和化合
![]()
![]() 物之间存在如图关系。试根据该图推断X、Y、
物之间存在如图关系。试根据该图推断X、Y、
|
|
(可以填满或不填满或增加下表)
| 1组 | 2组 | 3组 | 4组 | 5组 | 6组 | 7组 | 8组 | 9组 | 10组 | 11组 | |
| X | |||||||||||
| Y | |||||||||||
| Z | |||||||||||
| 甲 | |||||||||||
| 乙 |
2、如图所示, X Z
![]()
![]()
![]()
![]()
![]()
![]() 丙
丙
![]()
![]() 甲
乙
甲
乙
![]()
![]()
![]()
![]() 丁
丁
Y W
己知①甲、乙、丙、丁为前三周期元素的单质。②在一定条件下甲与丙和甲与丁都按物质的量之比1:3反应,分别生成X和Y,在产物中元素甲呈负价。③在一定条件下乙与丙和乙与丁都按物质的量之比1:2反应,分别生成Z和W,在产物中元素乙呈负价。
请填空:(1)甲是 乙是 。
(2)甲与丙反应生成X的化学方程式是
(3)乙与丁反应生成W的化学方程式是
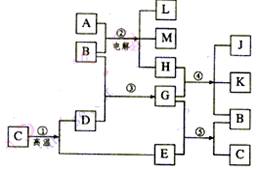 3、根据下列反应框图填空,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应。
3、根据下列反应框图填空,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应。
(1)单质L是 。
(2)化合物B是 。
(3)图中除反应①以外,还有两个用于工业生产的反应,是 和 (填代号)。
它们的化学反应方程式分别是 和 。
4、下图为一些常见物质的转化关系图。已知:①电解C溶液的反应是无机化工生产中的一种重要反应,②Q、M为常见单质 ③F、L是含有同一种元素的化合物,该元素在两种化合物中的化合价不同。
|
![]()
![]()
|
|
|
|
![]()
![]()
![]()
|
|
 | |||||
 | |||||
稀盐酸
|
|
试回答下列问题:![]()
![]()
(1)B、D的化学式为:B D
(2)完成下列反应的化学方程式:
① F + L → M + H2O
②电解C的饱和溶液
(3)R与NaOH溶液反应的离子方程式
5、下图是物质之间转化关系,每个方框代表一种物质。
 |
(1)当X为两种非金属元素所组成的化合物时,化学式为:
甲 乙 丙 X Y Z
(2)当X为金属与非金属元素所组成的化合物时,化学式为:
甲 乙 丙 X Y Z
6、下图是物质之间转化关系,每个方框代表一种物质。
![]()
|
|
|
|
|
![]()
![]()
|
![]()
![]() H2O
适量硫酸,蒸发结晶
H2O
适量硫酸,蒸发结晶
![]()
![]()
![]()
![]()
|
|
![]()
|
|
|
|
![]()
![]()
![]() 点燃
点燃
![]()
![]() X
X
|
![]()
![]() 蒸发结晶
蒸发结晶
回答下列问题:(1)A物质是 B固体是
(2)写出固体I和气体J反应生成K的化学反应方程式
(3)写出C的溶液与气体D反应的离子方程式
7、A、B、C、D四种常见短周期非金属单质,这些单质式量中,B最小,C此之,且室温下它们之中有三种是气体,一种是固体,相互关系如下图:
|
|
![]()
![]()
![]()
![]() Δ
Δ
 | |||||
|
|
![]()
![]()
![]() 化合物甲
化合物甲
(1)写出化学式:X B D
![]() (2)写出Y + 甲 Δ Z +
丙 的化学方程式
(2)写出Y + 甲 Δ Z +
丙 的化学方程式
8、下列物质间有如下转化关系。其中A是一种固体单质,E是一种白色沉淀。

![]()
|
|
|
![]()
![]()
![]()
![]() O2
O2
a溶液
|
|
![]()
![]()
![]() Δ
Δ
![]()
回答:(1)B的化学式是 ,B在固态时属于 晶体。
(2)B和a溶液反应的离子方程式是
(3)A和a溶液反应的离子方程式是
9、已知①X、Y、Z三中短周期元素的核电荷数依次增大 ②X与Y同族,Y与Z同周期 ③Y与Z能形成原子个数比为1∶1的离子化合物A ④X与Z能形成原子个数比为1∶1的共价化合物E ⑤C和D可以发生反应。 A及其生成物之间的相互关系如下图(各反应所需的水和生成的水及其必要的其它试剂已略去)。
|
|
|
|
![]()
![]()
![]()
![]()
|
![]()
![]()
|
|
![]()
![]()
![]() 电解
单质F
④
电解
单质F
④
![]()
![]() ②
②
|
|
|
回答:(1)写出元素X Y Z ,B的化学式
(2)写出①②④反应的离子方程式:
①
②
④
10、下图是物质之间转化关系,每个方框代表一种物质。
|  | |||
![]()
|
![]()
|
|
| ||||||||
|
|
![]()
某温度下,C和D反应生成I的起始和某时刻的反应混合物如下表所示。
| C | D | I | |
| 起始组成/mol | 6 | 4 | 0 |
| 某时刻始组成/mol | 3 | 3 | 2 |
回答:(1)H的化学式 (2)反应①方程式
(3)反应②方程式
高考化学复习无机物的综合推导专题 参考答案
东山区教育发展中心教研部 化学科
1、
| 1组 | 2组 | 3组 | 4组 | 5组 | 6组 | 7组 | 8组 | 9组 | 10组 | 11组 | |
| X | Cl2 | F2 | Cl2 | O2 | C | O2 | Cl2 | Mg | Al | C | Mg |
| Y | Br2 | O2 | S | S | Si | N2 | N2 | C | Fe | Cu | S |
| Z | H2 | H2 | H2 | H2 | O2 | H2 | H2 | O2 | O2 | O2 | O2 |
| 甲 | HBr | H2O | H2S | H2S | SiO2 | NH3 | NH3 | CO2 | Fe3O4 | CuO | SO2 |
| 乙 | HCl | HF | H2O | H2O | CO | H2O | HCl | MgO | Al2O3 | CO2 | MgO |
|
|
|
|
或:O2 + Mg 2MgO
3、(1)H2 (2)H2O (3)②,④ 2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
2Ca(OH)2+2Cl2=Ca(OCl)2+CaCl2+2H2O
4、(1)FeCl2, FeS(2)①SO2
+ 2H2S === 3S + 2H2O ②2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑(3)Al2O3 + 2 OH― === 2 AlO2― + H2O
2NaOH+H2↑+Cl2↑(3)Al2O3 + 2 OH― === 2 AlO2― + H2O
5、(1)甲 Mg 乙 O2 丙C X CO2Y MgO Z CO(2)甲Cl2乙Fe丙Br2X FeBr2Y FeCl3 Z FeBr3
6、(1)NaCl; S (2) Na2O2 +SO2 === Na2SO4;
|
7、(1)X:P2O5;B: H2 ;D: Cl2 (2) PCl5 + 4H2O H3PO4 + 5HCl
8、(1)SiO2;原子, (2)SiO2 + 2 OH― === SiO32― + H2O
(3) Si + 2 OH― + H2O === SiO32― + 2H2↑
9、(1)H, Na, Cl, H2 (2) ① 2 Cl―+2H2O![]() 2 OH―+ H2↑+ Cl2↑
2 OH―+ H2↑+ Cl2↑
② 2Al + 2 OH― + 2H2O === 2 AlO2― + 3H2↑
③
|
10、(1)HCl (2) 2Cl2+2NaOH=NaOCl+NaCl+H2O (3) N2 + 3H2 2NH3