赏析几例化学实验的改进与创新的试题
王穗萌 武汉大学附中
化学实验的改进与创新的试题大多来源于教材,又充分体现高于教材的命题思路,如2002年的喷泉2的引发及2003年的方法二制Fe(OH)2 。解答这类试题的一般思路是:先理解该实验的原理 、目的,再找出实验的不足、错误,最后依据实验的科学性、可行性、安全性、简约性进行评价、优化,即改进与创新。
 例1.甲同学按教材中图4―6(如图)做新制氯水受日光照射分解放出02的验证实验,结果现象不明显。
例1.甲同学按教材中图4―6(如图)做新制氯水受日光照射分解放出02的验证实验,结果现象不明显。
(1)写出氯水受日光照射的化学方程式
_________________________________________
(2) 乙同学反思了此实验的本质后,将新制氯水先在暗处存放
三四天,再拿出来做如图实验,结果效果十分明显。请解释乙
同学实验取得成功的原理。
(3) 请再设计一种方法,使刚制的氯水经过简单的处理后,做 HClO受日光照射分解实验,效果也十分明显。
![]() 分析:氯水中的次氯酸见光分解产生氧气,因此次氯酸的浓度高低是决定本实验的现象是否明显的关键。促使氯水中存在的平衡: H20 + Cl2 HClO + HCl向右移, 显然可提高次氯酸的浓度。
分析:氯水中的次氯酸见光分解产生氧气,因此次氯酸的浓度高低是决定本实验的现象是否明显的关键。促使氯水中存在的平衡: H20 + Cl2 HClO + HCl向右移, 显然可提高次氯酸的浓度。
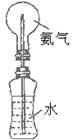
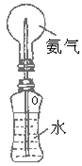
 例2.某同学受课本图1―11演示实验(左图)的启发,
设计了一个由不太易变形的矿泉水瓶与烧瓶组成的简易装置(右图),以方便、快速做喷泉的
例2.某同学受课本图1―11演示实验(左图)的启发,
设计了一个由不太易变形的矿泉水瓶与烧瓶组成的简易装置(右图),以方便、快速做喷泉的
实验,但实际操作中发现喷泉稍有产生不久即停止。
(1) 请指出右图装置的设计缺陷_____________
____________________________________
(2) 如何改进这一装置? 简述改进后的引发上喷
的最简单操作。
分析:喷泉产生的关键在于装置内外有较大的压强差。
新设计的装置由于不宜变形,因此当喷泉发生后矿泉水
瓶内气体的压强变小而接近圆底烧瓶内气体的压强时,喷泉即停止。进一步改进的思路是使矿泉水瓶内气体的压强始终保持不变。
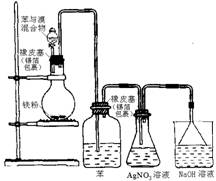
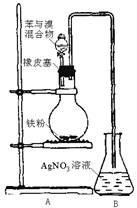 例3.课本中介绍了在有催化剂存在时溴与苯发生取代反应。甲同学提出可用下图装置进行实验加以验证。
例3.课本中介绍了在有催化剂存在时溴与苯发生取代反应。甲同学提出可用下图装置进行实验加以验证。
(1) 写出烧瓶中的有机反应_________________________
(2)认为苯与溴反应为取代反应的实验现象将是______
________________________
(3) 乙同学建议圆底烧瓶上的橡皮塞最好用锡箔包住,原因
是_________________________________________。
(4) 丙同学认为用上述装置①难以确证苯与溴的反应为取代反应,理由是___________
______________________________________________________, ②可能导致环境污染。
(5)丁同学同意丙同学的看法,认为应将锥形瓶口塞上双孔橡皮塞,并进行两处改进,即可达到确证反应类型及用液体消除污染的目的,请推测其改进的要点:
改进1:_____________________________________________
改进2:_____________________________________________
分析:若溴与苯发生取代反应,则必有溴化氢气体产生。溴易挥发,溴蒸汽与溴化氢气体一样,不仅能腐蚀橡胶,而且与硝酸银溶液能产生浅黄色沉淀,因此要用洗气等方法排除溴蒸汽的干扰。溴化氢气体极易溶于水,溴化氢气体的吸收要防倒吸。
例4.欲测定在干燥空气中已部分氧化的Na2SO3样品中 Na2S03的质量分数,甲、乙两组分别设计并完成实验如下:
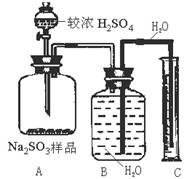 甲组:称取a g样品,利用下图所示装置(B、C之间导管先充满水),测出A中加入足量较浓H2SO4反应后,量筒C中水的体积VmL。
甲组:称取a g样品,利用下图所示装置(B、C之间导管先充满水),测出A中加入足量较浓H2SO4反应后,量筒C中水的体积VmL。
(1)B、C之间导管先充满水的目的
_______________________________________________
(2)你认为本组实验的Na2S03测定值将偏 _____(高、低),
主要原因是_____________________________________,
(3)简述最简单改进的方法_____________________
_____________________________________________
乙组:称取a g样品,利用下图所示装置,测出A中加入足量较浓H2SO4反应后装置C中足量碱石灰增重为b g。
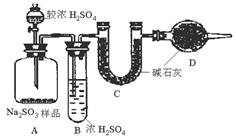 (1)B装置的作用是________________________
(1)B装置的作用是________________________
(2)你认为本组实验的Na2S03测定值将偏 _____
(高、低),主要原因是______________________,
(3)简述改进的方法
______________________________________
分析:本实验为定量实验, 因此要考虑误差。甲组采用排液量气法,关键在于要确保排到量筒内的液体体积与进入广口瓶B中的气体体积相等。甲组中二氧化硫在水中有较大的溶解(1:40), 显然是误差的来源。乙组采用的是气体吸收称重法,关键在于产生的二氧化硫要能完全被U型管C所吸收。二氧化硫比空气重,导致在A、B中有较大量的残留而造成误差。
参考答案:
1.(1)略;(2)氯气与水的反应是可逆的,新制的氯水中HClO的浓度不大,分解速率慢,产生O2少,而将这种氯水在暗处存放三四天,使溶于水的C12尽可能多的与水反应,生成HClO的浓度明显提高。(3)向刚制的氯水中加入CaCO3粉末至不再产生气泡为止,取过滤后的液体做光照实验。
2.(1)矿泉水瓶内的压强难始终与大气压保持一致, 使瓶中的水不能顺利上喷;(2)在该矿泉水瓶上烧一个小洞(如图1),先有手指堵住该小孔,轻轻一捏瓶身,使水进入烧瓶后,手指离开该小孔。
3.(1)略。(2) 锥形瓶中产生浅黄色沉淀。(3)溴及苯蒸气、溴化氢气体会损坏橡皮塞。
(4)溴易挥发,溴蒸汽与水作用可产生溴离子, 与硝酸银溶液同样也产生浅黄色沉淀。
(5)在A、B之间增加一个盛有苯洗气装置,橡皮塞最好用锡箔包住;在B的右侧增加一个具有防倒吸装功能的盛有NaOH溶液的装置(如图2)。
4.甲组:(1)排出B、C之间导管中的空气, 减少测量误差,(2)低 ,部分SO2 溶于了B中的水,(3)B装置中的水面加一层植物油。(如图3)
乙组:(1) 干燥气体,减少测定误差,(2)低 SO2比空气重,部分残留A、B,(3)增加一个可向A中通入能除去CO2且干燥的空气的装置。(如图4)
 | |||||
 | |||||
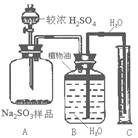 | |||||
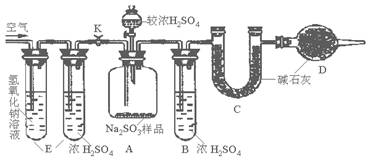 图1
图2
图3
图1
图2
图3
图4