高中化学毕业会考模拟题
一、选择题 (每小题2分,共30分;每个小题只有1个选项符合题意。)
1.材料科学是信息技术发展的支柱,信息技术需要使用大规模集成电路,制造大规模集成电路的半导体材料是
A,SiO2 B.Si C.Fe 、 D.塑料
2.SO2是造成大气污染的主要气体,造成大气中SO2含量增加最主要原因是
A.实验室排放的SO2 B.火山爆发产生的SO2
C.人们燃烧煤和石油产品产生的SO2 D.工业制硫酸排放的SO2
3. 下列物质互称同分异构体的是
A.氧气和臭氧 B.16O与18O
C.甲烷和乙烷 D.正丁烷和2―甲基丙烷
4.在O℃,1.O1×l05Pa的条件下,等体积的下列物质质量最大的是( )
A.水 B.氢气 C.二氧化碳 D.氯气
5.既有离子键,又有共价键的化合物是
A.KBr B.NaOH C.HBr D.N2
6.下列各组物质的性质比较,正确的是
A.酸性:HClO4>H3PO4>H2SO4 B.氢化物稳定性:H2S>HF>H2O
C.碱性:Mg(OH)2>NaOH D.氧化性:F2 > Cl2 > Br2 > I2
7.下列洗涤仪器的方法错误的是
A.用稀氨水洗涤做过银镜实验的试管
B.用NaOH溶液洗涤粘有苯酚的试管
C.用盐酸洗涤装过石灰水的试管
D.用硝酸洗涤粘有铜粉的试管
8.在下列含氮元素的物质发生的化学反应中,含氮元素的物质做还原剂的是
A.4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
B.3Cu+8HNO3==3Cu(NO3)2+2NO↑+4H2O
C、NO2+SO2==NO+SO3
D.N2+3H2![]() 2NH3
2NH3
9.下列反应,一定是属于混合物的是
A.漂白粉 B.胆矾 C.明矾 D.冰醋酸
10.下列条件下化学反应速率最大的是
A.20℃,0.1mol・L-1的盐酸溶液与块状碳酸钙反应
B.10℃,0.1mol・L-1的盐酸溶液与块状碳酸钙反应
C.10℃,0.2mol・L-1的盐酸溶液与粉状碳酸钙反应
D.20℃,0.2mol・L-1的盐酸溶液与粉状碳酸钙反应
11.因为水解而显碱性的溶液是
A.氢氧化钠溶液 B.食盐溶液 C.醋酸溶液 D.碳酸钠溶液
12.下列反应达到平衡后,增大压强或升高温度,平衡都向正反应方向移动的是
![]() A.2NO2 N2O4(正反应为放热反应)
A.2NO2 N2O4(正反应为放热反应)
![]() B.3O2 2O3(正反应为吸热反应)
B.3O2 2O3(正反应为吸热反应)
![]() C.H2(g)+I2(g) 2HI(g)(正反应为放热反应)
C.H2(g)+I2(g) 2HI(g)(正反应为放热反应)
![]() D.NH4HCO3(s) NH3+H2O(g)+CO2(正反应为吸热反应)
D.NH4HCO3(s) NH3+H2O(g)+CO2(正反应为吸热反应)
13.某有机物为:HO―CH2―CH2―CH==CH―COOH, 该有机物不含的官能团是 A.羟基 B.羧基 C.醛基 D.双键
14.某溶液中含有较多OH-,下列离子可以大量共存的是
A.Ag+、NO3-、Na+ B.SO42-、Mg2+、K+
C.Na+、HCO3-、NO3- D.CO32-、SiO32-、K+
|
|
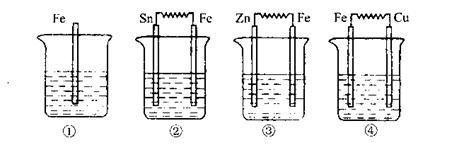
15.下图各烧杯中盛有稀硫酸,能形成原电池,且铁为正极的是:
A.① B.② C.③ D.④
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | ||||||||
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | |
| 答案 |
二、填空题(每空1分,共15分)
16.下表是元素周期表前三周期部分元素所在周期表中的位置:
IA 0
| A | IIA | IIIA IVA VA VIA VIIA | |||||
| D | F | H | |||||
| B | C | E | G | ||||
(1)A、B、C、D、E、F、G、H中化学性质最不活泼的元素是_______(填元素符
号),其原子的电子式为__________;
(2)比较B、C、E、G原子的原子半径大小:______>_____>_____>______;
(3) C的最高价氧化物对应的水化物的化学式:___________
G的最高价氧化物对应的水化物的化学式:___________
17.除去下列物质中的杂质(括号内为杂质),请你选择试剂或方法。
(1)Na2CO3(NaHCO3),你选择的方法是____________________;
(2)FeCl2溶液(FeCl3),你选择的试剂是__________________;
(3)NO(NO2),你选择的试剂是_________,反应的化学方程式为:
_________________ ____
18.有中学化学的常见仪器:A.量筒、 B.容量瓶 C.酸式滴定管 D.托盘天平 E.温度计 F.分液漏斗
(1): 配制lmol・L―1NaCl溶液,一定要用到的仪器是_______________(填番号)
(2);量液体的体积要用到的仪器是_____________________(填番号)
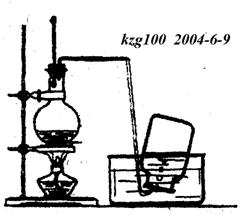 19.实验室制备乙烯实验装置如图所示。
19.实验室制备乙烯实验装置如图所示。
(1)写出实验室制取乙烯的化学方程式:___________________________________
(2)该装置有一个典型错误,该错误是________________________________
(3)乙烯通入溴水中,现象是_______________________________,
发生的化学反应方程式为:
___________________________________ 。
三、计算题(共5分)
20、一种白色粉末由碳酸氢钠和碳酸钠混合而成,称取混合物4.42g,加热至恒重,得标准状况下的气体448毫升。求原混合物中碳酸氢钠和碳酸钠的质量
高中化学毕业会考模拟题参考答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | B | C | D | D | B | D | A | A |
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | |
| 答案 | A | D | D | B | C | D | C |
二、填空题(每空1分,共15分)
16. (1)Ne ;(2)B>C>E>G;(3)Al(OH)3、HClO4
17.(1)加热; (2)铁粉; (3)水,3NO2+H2O===NO+2HNO3
![]() 18、B D;A
18、B D;A
19.(1)CH3CH2OH CH2==CH2↑+H2O; (2)温度计的水银球没有插入液面以下; (3)溴水褪色,CH==CH2+Br2→CH2Br-CH2Br;
三、计算题(共5分)
20、m(NaHCO3)=3.36g;m(NaCO3)=1.06g