������ѧ��ʱѵ����1��
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | ||
| �� | ||||||||||
| ��� | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| �� |
һ��ѡ���⣨�������8С�⣬ÿС��3�֣���24�֡�ÿС��ֻ��1����ȷѡ��������⡣��
1��������ȼ���ױ��ж��Ļ�ѧ���ʣ������������װ������Σ�վ����ǩ�������������ʣ������˰�װ��ǩ����
| A | B | C | D | |
| ���ʻ�ѧʽ | ŨHNO3 | CCl4 | P4 | KClO3 |
| Σ�վ����ǩ |
��ʴ�� |
��ȼ�� |
��� |
��ը�� |
2��������һ���Ƽ���ʡ��ӵ�С����ײ��Ϲ����ص�ʵ���ҡ����ҹ���ѧ�������ײ����о�����λ������ǰ�С�����ǰ�ҹ���ѧ�ҳɹ����Ƴ���3mm���Ĺ�״����̼���ܣ����Ⱦ�����֮�ס�����̼��ά����ǿ�ȸߡ��նȴ��ܶ�С���۵�ߡ���ѧ�ȶ��Ժõ��ص㣬�������Ϊ��������ά�������жԴ�̼���ܵ�˵��������ȷ����
A����������ɻ���������ϡ������������� B������ʯī��Ϊͬ��������
C������̼�����к��зǼ��Թ��ۼ���������D��̼��ά���ϲ���Ϊһ�ָ߷��ӻ�����
2004��ĩһ��������̫ƽ������ֽ��٣����Ѳ�����ȡ��15�����˵������������Ҵ�����������˵��δ��������������ȫ����Ŀ��⡣�ش�3-5��:
3����������ˮ�dz���Ҫ�����й���ˮ��˵������������
�������Ǻ�ˮ�����ķ���֮һ���ڵ�ˮ���ܶ�С�ں�ˮ���ܶȡ����ڻ���ѩˮ�п����ʺ������ˮ�е��١���0�����ϣ��¶�Խ�ߣ�ˮ���ܶ�ԽС
A���٢ܡ��������� B���ۢܡ��������� C���ڢۡ����������� D����
4����������ӡ�����ذ���ֹ���ģ���ߵļ�����Ʒ������ȫ����Ĵ������������������͵���������һЩ�������Dz���ͬʱ���õģ� �ݱ�����������������������Ͻ��ۼ������������ж��¼����ݴ��Ʋ⣬���ϵĽ��ۼ������п�������
A��ClO3����Cl����H+�� ������������������������������B��ClO����Cl����H+
C��NaClO��NaClO3��������������������������������D��NaClO��NaCl
5��������������ijЩ���ⳣ���漰����ѧ֪ʶ��������������ȷ����
A�����ʵ���֬�����ŵ�������ζ����������֬������ˮ�ⷴӦ
B������������������ԭ������ʯī���缫��ⱥ���Ȼ�����Һ���Ƶ��н�ǿɱ������������Һ
C��ѪҺ����Ѫ����Ѫ�����γɵĽ��壬���������˥�ߵIJ���ѪҺ�еĶ��ؿ���ͨ�����ķ�����ȥ
D�����϶�ҧ�˵�Ƥ��ʱ�����������ע�����壬��ʱ���ڻ���ͿĨС�մ���Һ��ˮ
6�������ѧ������ã���������̼(C3O2)�ǽ��Ǵ�����ijɷ�֮һ�������й�C3O2��˵���������
A��C3O2��CO2����̼��������
B��C3O2��CO2����̼���Ӧ������������
C��C3O2�Ľṹʽ��O=C=C=C=O
D��C3O2��CO��ȼ�ղ��ﶼ��CO2
7�����м��������У�������ͬ�ķ����ܳ�ȥ���е����ʣ�������Ϊ�������ʣ�����
A��������Һ(NaCl)��������Һ(NaCl)
B��Fe(OH)3����(KCl)��������Һ(KI)
C��Na2CO3����(NaHCO3)��NaHCO3����(Na2CO3)
D�����ۣ���ۣ����⣨ʳ�Σ�
8���ϳɸ߾���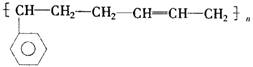 �ĵ�����
�ĵ�����
��![]() ����
����![]() ����CH��C��CH3 ��CH3��CH�TCH��CH3
����CH��C��CH3 ��CH3��CH�TCH��CH3
��CH2�TCH��CH�TCH2
����A���٢ݡ��������� B���٢ܡ��������� C���ڢۡ������� ��D���ڢ�
����ѡ���⣨�������10С�⣬ÿС��5�֣���50�֡�ÿС����һ��������ѡ��������⡣����ȷ��ֻ����һ��ѡ���ѡʱ����С��Ϊ0�֣�����ȷ�𰸰�������ѡ�ֻѡһ������ȷ�ĸ�2�֣�ѡ�����Ҷ���ȷ�ĸ����֣���ֻҪѡ��һ����С���Ϊ0�֡���
9�������£���һ��Ũ�ȵİ�ˮ����μ������ᣬ�ڴ˹����У�����˵����ȷ����
A����pH>7ʱ��c(Cl��)>c(![]() )>c(OH��) >c(H+)
)>c(OH��) >c(H+)
B����pH=7ʱ��c(![]() )>c(Cl��)>c(H+)=c(OH��)
)>c(Cl��)>c(H+)=c(OH��)
C����pH<7ʱ��c(![]() )>c(Cl��)>c(H+)>c(OH��)
)>c(Cl��)>c(H+)>c(OH��)
���� D������ˮ������ǡ����ȫ��Ӧʱ��c(Cl��)>c(![]() )>c(H+)>c(OH��)
)>c(H+)>c(OH��)
10�����и������������Ժ��ֱ�����ϣ�ֻҪ�ܵ����ʵ���һ������ȫȼ��ʱ�������������Ƕ�ֵ����
A��CH2��CH2��C2H5OH��HOCH2CH2COOH��������B��CH2O��C2H4O2��C6H12O6
C��C6H6��C5H10��C7H6O2������������������������ D��H2��CO��CH3OH
11���ҹ���ѧ�����ߺϳ�������ṹ���ӵ���Ȼ�л�������磺Ҷ���ء�Ѫ���ء�ά����B�ȣ�Ҷ���صĽṹ����ͼ��ʾ�������й�˵����ȷ����
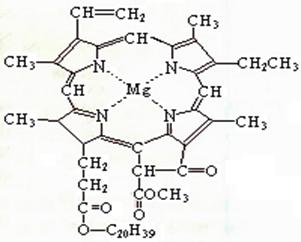
A��Ҷ�������ڸ߷��ӻ�����
B��Ҷ���ط����к����������͵�˫��
C��Ҷ���ز����ڷ�����
D����һ�������£�Ҷ�����ܼӳɡ�ˮ�⡢�����ȷ�Ӧ
12�����������ӡ��⡱ʳ�ν϶��ʹ���˵���أ�KIO3����������ڹ�ҵ�Ͽ��õ�ⷨ��ȡ����ʯī�Ͳ����Ϊ�缫����KI��ҺΪ���Һ����һ�������µ�⣬��Ӧ����ʽΪ��
KI��3H2O![]() KIO3��3H2���������й�˵����ȷ����
KIO3��3H2���������й�˵����ȷ����
A�����ʱ��ʯī�������������������
B�����ʱ��������Ӧ�ǣ�I�D�D6e����3H2O��IO3����6H��
C����Һ������ǿ���ԣ�����������
D�����ǰ����Һ��pH��������
13��NA���������ӵ�����������˵����ȷ����
A��1LŨ��Ϊ0.1 mol / L AlCl3��Һ�к��е���������0.4NA
B��3��9gNa2O2����������CO2ʱת�Ƶĵ�������0.05NA
C����״���£�3.2gͭ��������Ũ���ᷴӦ���ɵ����庬�еķ�������0.1NA
D����״���£�1.12L��SO3������ԭ������0.2 NA
14���������ӷ���ʽ��д��ȷ����
A����������Һ��ͨ��������CO2 ��������C6H5O��+H2O+CO2 �� C6H5OH +HCO3��
B��KAl(SO4)2�еμ�Ba(OH)2ʹSO42��ǡ����ȫ����
�� ������������������������ 2Al3++3 SO42��+3 Ba2++6 OH��=2Al(OH)3�� +3BaSO4��
C�����������Һ��ͨ������SO2������������ Ca2++2ClO��+SO2+H2O=CaSO3��+2HClO
D��FeI2��Һ��ͨ������ʵ�����Cl2��������2Fe2++2I��+2Cl2=2Fe3+��4Cl��+I2
15��T��ʱ��A������B���巴Ӧ����C���塣��Ӧ������A��B��CŨ�ȱ仯��ͼ������ʾ�������������������䣬�¶ȷֱ�ΪT1��T2ʱ��B�����������ʱ��Ĺ�ϵ��ͼ������ʾ�������н�����ȷ����
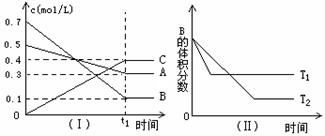
A���ڣ�t1+10��minʱ�����������������䣬����ѹǿ��ƽ�����淴Ӧ�����ƶ�
B�������������䣬�����¶ȣ������淴Ӧ���ʾ�������A��ת��������
C��T��ʱ������ͬ�����У�����0.4mol/L A��0.4mol/L B��0.2mol/L C��Ӧ���ﵽƽ���C��Ũ����Ϊ0.4mol/L
D����t1+10��minʱ������ѹǿ���䣬ͨ��ϡ�����壬ƽ�����淴Ӧ�����ƶ�
16��2003��ŵ������ѧ��������������ѧ��Peter Agre��Roderick Mackinnon�Ա��������ڡ�ˮͨ�����͡�����ͨ�������о��ɾ͡�Mackinnon���ڵ��о�������Ҫ��Na+��K+����ܽӽ��������������ڳ��ֵIJ��ȴ�ߴ�1���������Ե��ÿ�ѧ�ҹ۲�Na+��K+�ڽ�������ͨ��ǰ��ͨ�����Լ�����ͨ�����״̬����Ϊ�����ڡ�����ͨ������Ѱ�Ҿ���IJ���������Ӧҩ����й����ơ��ص�˵����ȷ����
A�������Ƶ��ܶȱȼص��ܶ�С
B���ƺͼ��ڿ�����ȼ�յIJ��ﶼ�ǹ�������
C���ƺͼض��Ƕ�����Ԫ��
D���ƺͼصĺϽ�[��(K)��50%��80% ]�������³�Һ̬
17���ֱ���pH����1������Һ��pH����13������������Һ�У��ֱ������������ۣ�������Һ�ų��������࣬����ܵ�ԭ����
A������Һ�����ͬ�����Ƕ�Ԫǿ��
B������Һ�����ͬ����������
C������ǿ�ᣬ������Һ��Ũ���Ǽ���ҺŨ�ȵ�3������
D������ǿ�ᣬ������Һ������Ǽ���Һ�����3������
18��a mol FeS��b mol FeOͶ�뵽V L��c mol•L��1��������Һ�г�ַ�Ӧ������NO���壬���ó�����Һ�ijɷֿɿ�����Fe(NO3)3��H2SO4�Ļ��Һ����Ӧ��δ����ԭ���������Ϊ
A��(a+b)��63g�������� ������������������������ B��(a+b)��189g
C��(a+b)mol��������
���������������������������� D��(Vc��![]() )mol
)mol
������ѧ��ʱѵ����
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | ||
| �� | B | D | D | B | A | B | B | A | ||
| ��� | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| �� | D | AC | C | BD | B | A | CD | D | BD | BD |


