高考前化学实验专题讲练(7个方面)
一、仪器的排列组合与选择连接顺序
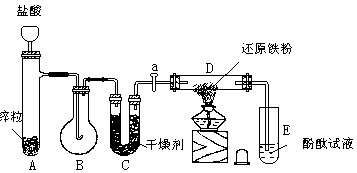
【例1】 欲制无水氯化铝并保存备用。现有仪器如下图所示,并有食盐晶体、水、固体烧碱、铝粉、二氧化锰、浓硫酸等六种试剂。
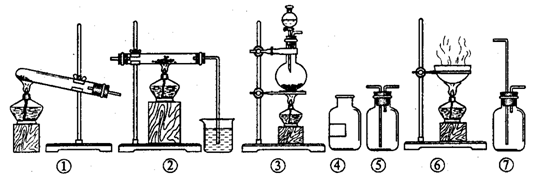
设计的制取过程是:制氯气 → 加净化和干燥氯气 → 制氯化铝
请回答下列问题:
(1)从上列仪器中选取必须的几种,连接成一个制无水氯化铝的连续装置,按前后顺序填写图的编号(不一定填满),并写出各仪器里放入的试剂的化学式。
仪器编号 ___________________________________________________;
放入试剂 ___________________________________________________;
(2)写出实验过程中有关反应的化学方程式。____________________________
______________________________________________________________。
【思维训练】实验室用Zn粒和盐酸反应制H2,其中含酸雾、水气、硫化氢及少量氧气等杂质气体,某同学设计了以下几种装置,按一定顺序连接,气体通过时,达到每一装置除去一种气体的目的。
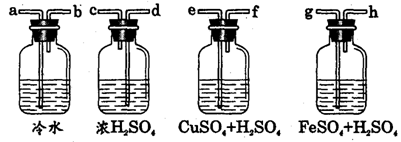 |
(1)它们连接的顺序为 ;
(2)除去H2S的离子方程式为 ;
(3)除去O2观察到的现象为_______________________________________。
二、实验产物的验证
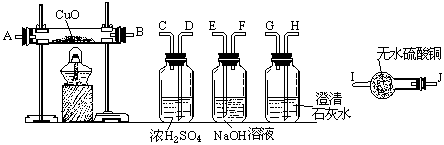
【例 2】 水蒸气通过灼热的煤所产生的混和气,其主要成份是CO、H2还含有CO2和水蒸气.请用下列装置设计一个实验,以确认上述混和气中含有CO和H2.
(1)混和气→( )( )接( )( )接( )( )接( )( )接( )( ).
(2)确认混和气中含有H2的实验现象是 ;其理由是 .
 |
三、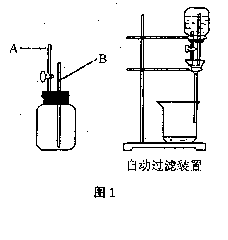 气密性检查和防倒吸
气密性检查和防倒吸
【例3】 某学生设计一个自动过滤装置,在普通过滤装置的漏斗上安装一个自动加液装置(左图)。使用时,滤液不会溢出,过滤又较快,整个过程无须人照顾。回答下列问题:
(1) 如何检查该自动过滤装置的气密性?
(2) 分析自动加液装置A管上口高出B管口
约1cm 的理由
|
|
【思维训练1】
【思维训练2】
四、实验中的定性与定量问题
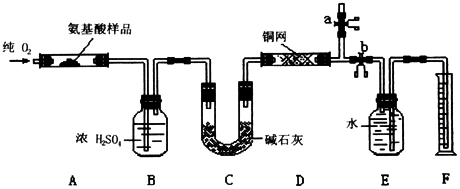 【例4】实验室用燃烧法测定某种氨基酸
【例4】实验室用燃烧法测定某种氨基酸![]() 的分子组成。取w g该种氨基酸放在纯氧中充分燃烧,生成
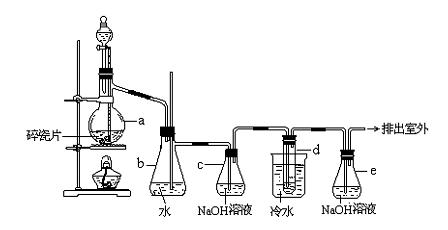
的分子组成。取w g该种氨基酸放在纯氧中充分燃烧,生成![]() 。现用下图所示装置进行实验(铁架台、铁夹、酒精灯等未画出),请回答有关问题:
。现用下图所示装置进行实验(铁架台、铁夹、酒精灯等未画出),请回答有关问题:
(1)实验开始时,首先打开止水夹a,关闭止水夹b,通一段时间的纯氧,这样做的目的是 ;之后则需关闭止水夹 ,打开止水夹 。
(2)以上装置中需要加热的有(填装置代号) 。操作时应先点燃 处的酒精灯。
(3)装置A中发生反应的化学方程式为 ;
(4)装置D的作用是 ;
(5)为将![]() 所排水的体积测准,反应前应将连接E和F装置的玻璃导管中充满 (水、空气或氧气),简述理由
所排水的体积测准,反应前应将连接E和F装置的玻璃导管中充满 (水、空气或氧气),简述理由
(6)读取![]() 所排水的体积时,要注意:
___________________。
所排水的体积时,要注意:
___________________。
(7)实验中测得![]() 的体积为V mL(已换算成标准状况)。为确定此氨基酸的分子式,还需得到的数据有(填字母)
。
的体积为V mL(已换算成标准状况)。为确定此氨基酸的分子式,还需得到的数据有(填字母)
。
A.生成二氧化碳气体的质量 B.生成水的质量
C.通入氧气的体积 D.该氨基酸的摩尔质量
(8)如果将装置中B、C的连接顺序变为C、B,该实验的目的能否达到?简述理由
。
五、实验方案的设计
【例5】 “套管实验”是将一支较小的玻璃仪器装入另一玻璃仪器中,经组装来完成原来需要两只或更多普通玻璃仪器进行的实验。因其具有许多优点,近年被广泛开发并应用于化学实验中。下述两个实验均为“套管实验”,请观察实验装置、分析实验原理,回答下列问题:
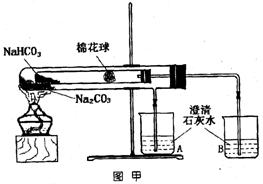
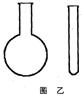
实验一:如图甲,小试管内塞有沾有无水硫酸铜粉末的棉花球。(如何检验气密性?)
(1)从点燃酒精灯开始,试管及烧杯A、B中能观察到的现象有
(2)整个实验结束时,在操作上需要特别注意的问题是
(3)通过该实验可以得出的结论是
实验二:在氨气的喷泉实验中,将圆底烧瓶集满氨气的操作很麻烦。请设计一个简单的操作方法,只用一支试管(如图乙),选用下列药品;A.氯化铵固体B.氢氧化钠固体C.浓氨水D,浓硫酸E.湿润的红色石蕊试纸,采用“套管法”在圆底烧瓶中集满喷泉实验用的氨气。
 (4)所用的试剂为:
(4)所用的试剂为:
 (5)请简述所设计的操作及到定集满氨气的现象:
(5)请简述所设计的操作及到定集满氨气的现象:
六、元素化合物知识与实验的结合题
【例6】研究某一化学反应的实验装置如下图所示:
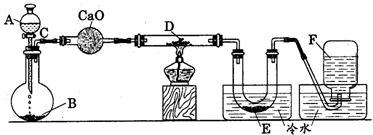 |
A~F属于下列物质中的六种物质:浓硫酸、浓盐酸、浓氨水、稀硫酸、稀盐酸、稀氟水、水、锌粒、铜片、食盐、高锰酸钾、氯化钙、氧化钙、四氧化三铁、氧化铁、氧化铜、氢气、二氧化碳、二氧化氮、一氧化碳、氯气、氯化氢、氨气、氮气、氧气。
实验现象;
(1)D物质由黑色变为红色
(2)无水硫酸铜粉末放入无色透明的E中得到蓝色溶液
(3)点燃的镁条伸入无色无味的F中.镁条表面生成一种灰黄色固体物质。将该发黄色物质放入水中,有气体放出,该气体具有刺激性气味。并能使润湿的红色石蕊试纸变蓝。通过分析回答:
l、写出A~F的物质名称: A ,B ,C ,D ,E ,F 。
2、写出有关的化学方程式: A与B__________________________________;C与D_________________________________________;E与无水硫酸铜___________
_______________________;F与Mg______________________________________;
F与Mg的反应产物与水 。
七、完成实验报告
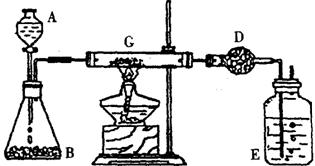
【例7】某同学加热炭粉(过量)和氧化铜的混合物,并用如下图所示的装置对获得的铜粉(含炭)样品进行实验测定,请完成实验报告。
(一) 实验目的: 。
(二) 实验用品:
仪器;天平,分液漏斗,锥形瓶,硬质玻璃管,干燥管,酒精灯,洗气瓶等;
药品:红褐色铜粉(含炭)样品,过氧化氢溶液,二氧化锰,碱石灰,浓硫酸等。
(三) 实验步骤:
(1) 在G中加入样品粉末W;在D中装入药品后,称得质量为m1;选择仪器安装后,检查气密性。
(2) 打开A的活塞,慢慢满加溶液,在B中进行的化学反应方程式为
(3) 对G进行加热,当G中药品充分反应后,关闭A的活塞,停止加热,G中发生反应的方程式为 。 (4)冷却后,称量D的质量为m2。
(四) 计算:实验时,G中反应完全,D中吸收也完全,根据所得数据,样品中铜的质量分数= (用含W,m1,m2的代数式表示)。
(五)问题讨论:
(1) E中所盛试剂为,其作用是
(2) 根据上述实验方案测得的铜的质量分数,跟实际铜的质量分数相比,是偏高、偏低、还是相等? ,原因是
(3) 如需要对该同学设计的实验装置进行改进,请提出改进的方案是 。