![]()
 �����������¿���ѧ��
�����������¿���ѧ��
����ѧ��������������
�Ծ�˵�������Ծ��ֵڢ����ѡ���⣩�͵ڢ������ѡ���⣩�����֣�����100�֣�����ʱ��100����
�����õ������ԭ��������H��1��C��12��O��16��A1��27��C1��35.5��Na40��Cu��64��Mg��24
�ڢ������60�֣�
һ��ѡ���⣨���20��С�⣬ÿ��3�֣���60�֣�ÿ��ֻ��һ��ѡ��������⣩
1���ܶѧ���������к��С�ˮ������ˮ��ͨ�������ֺ��壺�ٱ�ʾˮ�������ʣ��ڱ�ʾˮ��Һ���۱�ʾ���ʴ���Һ̬���������������е�"ˮ"�������������ֺ�����ǡ��� ��������
A��ˮ���������� B��ˮ�������� C����ˮ������ D����ˮ
2�����»�ѧ������ȷ���ǡ��� ��������
������ A����ϩ�Ľṹ��ʽCH2CH2�� B������ķ���ʽC2H4O2
������ C�������Ļ�ѧʽKALSO412H2O�� D���Ȼ��Ƶĵ���ʽ![]()
3���������±�����γɵĻ�������е������ǡ����� ��������
������ �ٸ߷е㣻��������ˮ����ˮ��Һ�ܵ��磻�ܵ��۵㣻������״̬�����硣
������ A���٢ڢۡ� B���ۢܢݡ���C���٢ܢݡ��� D���ڢۢ�
4��2004��ijһ�ڵġ�������ѧ��־���������й���ѧ���Զ�����̼Ϊ̼Դ��������Ϊ��ԭ������470�桢80Mpa�ºϳɽ��ʯ��������Զ���塣����˵������ȷ���ǡ��� ��������
������ A���ɶ�����̼�ϳɽ��ʯ�ǻ�ѧ�仯���� B�����ʯ��̼��һ��ͬλ��
������ C���Ʊ�������������̼���ơ��������� D�����ʯ��ֻ���зǼ��Թ��ۼ�
5�����г�ȥ���ʵķ�������ȷ���ǡ����� ��������
A��þ���л����������ۣ���������ռ���Һ��ַ�Ӧ������
B��SO2�л�������SO3��ͨ������ŨH2SO4���ռ�����
C��Cl2�л�������HC1��ͨ����ʯ���ռ�����
D��A1(OH)3�л�������Mg(OH)2�����������ռ���Һ����ַ�Ӧ�����ˣ�����Һ��ͨ�����CO2������
6�������ۡ����ŵijɹ�����ͷ��أ���һ��ʵ�����ҹ����˲���Ŀռ��ѧʵ�顣�����ɴ�Ӧ���������˵ĺϳɲ��ϡ����������У����ڸ��ϲ��ϵ��ǡ��� ��������
A������˿���� B���л�����������C�������������� D�������մ���
7�������йرȽ��У���С˳�����д�����ǡ��������� �� �� ��
A�����ȶ��ԣ�PH3��H2S��HBr��NH3
B�����ʵ��۵㣺ʯӢ��ʳ�Σ�������
C��������ӵ�������CO32- ��CH3COO-��SO42-
D����ɢϵ�з�ɢ�����ӵ�ֱ����Fe(OH)3����Һ��Fe(OH)3���壾FeCI3��Һ
8�����г�ȥ���ʵ�ʵ�鷽����ȷ���ǡ���������������
A����ȥK2CO3����������NaHCO3�����������м���
B����ȥ�������е��������ӣ���������Ũ��ˮ��Ӧ�����
C����ȥFeC13 ������Һ��������FeC12�������Թ���˫��ˮ�����
D����ȥ��������Һ�л���������Ȼ��ƣ���AgNO3��Һ�����
9����ǰһ�ַ�ɢϵ�������ص����һ����Һ���۲쵽���������ȳ�����������ǣ�������
A��������������μ����ᡡ������������������ B�����ǻ�����������Һ�м�����
C���Ȼ�����Һ�еμ�����������Һ������������ D���Ȼ�����Һ�еμӰ�ˮ
10��
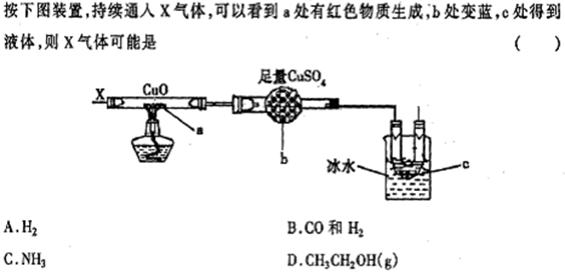
11��

12��2004��7�µ¶�������ѧ�ҹ�ͬ�������ڸ�ѹ�µ�����ۺ����ɸ߾۵������ָ߾۵�
�ľ�����ÿ����ԭ�Ӷ�ͨ������������������ԭ�ӽ�ϲ���ռ䷢չ����������״�ṹ����֪������N��N�����ļ���Ϊ160 kJ/mol����N��N�����ļ���Ϊ942kJ/mol�����ܱ�ʾ�γɻ�ѧ���ͷŵ����������ƻ���ѧ�����ĵ����������������й�˵������ȷ���ǡ���������
������ A������Խ��˵����ѧ��Խ�ι̣������ɵ�����Խ�ȶ�
������ B������ըҩ����ܲ��Ͽ����Ǹ߾۵�DZ�ڵ�Ӧ��
������ C���߾۵��������ڷ��Ӿ��塡
����D���߾۵���������ԭ�Ӿ���
13���⻯泥�NH4H�����Ȼ�淋Ľṹ���ƣ���֪NH4H��ˮ��Ӧ��H2���ɣ�����������ȷ���ǡ����������� ������ ��
�� ��A��NH4H�ǹ��ۻ���������������� B��NH4H����ˮ�����γɵ���Һ�Լ���
������ C��NH4H��ˮ��Ӧʱ��ˮ����ԭ������ D��NH4H�е�HԪ��ֻ��һ�ֻ��ϼ�
14�����з�Ӧ�����ӷ���ʽ������ǡ����� ������ ��
A����̼�������Һ�м��������������
Ca2+��2HCO3����2OH��=CaCO3����2H2O��CO32��
B������������ʵ���Ũ�ȵ�����������Һ��̼�������Һ���
Ba2+��2OH����NH4+��HCO3��=BaCO3����NH3��H2O��H2O
C�������������������ᷴӦ�� Al(OH)3��3H+ =Al3+��3H2O
D������CO2ͨ������������Һ�� CO2��2OH��=CO32����H2O
15������˵������ȷ���ǣ�NA��ʾ�����ӵ�������������
����A��28 g�������е�ԭ����ĿΪNA
����B��4 g�����Ʊ�ɸ�����ʱʧȥ�ĵ�����ĿΪ0.1NA
����C��1 mol�����������NA��������ӵ�����֮�����
D��22.4 L��������Ȳ�Ļ��������������ΪNA
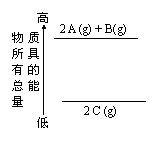
16.�����й�������ȷ���ǣ��� ��
 A. ���������š��ɴ����زյı�����ø���ʱ�Զ���ʴ�����¡����������������ǽ������ϴ��������Ӷ���֤�ڲ��¶Ȳ��¹��ߡ�
A. ���������š��ɴ����زյı�����ø���ʱ�Զ���ʴ�����¡����������������ǽ������ϴ��������Ӷ���֤�ڲ��¶Ȳ��¹��ߡ�
B.���ӵ�ʳ�Ρ� ���������ࡱ������Ӫ��Ʒ�� ���߸�ţ�̡����������͡��ȵȣ�����ĵ⡢������ָ���Ƿ��ӣ��ơ�����ֱ��Ǹ����Ӻ������ӡ�
C. ��ͼ�Ƿ�Ӧ���������������仯ʾ��ͼ��������ܷ����ķ�Ӧ�ġ� �Ȼ�ѧ����ʽ�ɱ�ʾΪ��
2 A��g��+ B(g) = 2 C��g������H=Q kJ��mol-1��Q��0 ��
D.���ˮ��ȡ����������ʱ��ͨ�����������Ƶ�ǿ����ʣ���˵��ǿ����ʵĵ����Ա�������ʵĵ�����ǿ


19.����ʦ����һ����ͼ��ʾ��ʵ�飬�����ձ�������KMnO4��Һ��ɫ�������ձ��е���Һ����������KSCN��FeCl2��Һ����Һ�Ժ�ɫ���ж�����˵������ȷ���ǡ���������
������ A�������������ɵ�ˮ���ӻ�ѧ���ʱȽϻ���
������ B����������H2����ȴΪҺ̬�⣬Һ���ˮ��Һ���л�ԭ��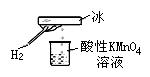
������ C����������H2ȼ��������ֻ���������Ե�����
������ D����������H2ȼ�յIJ����п��ܺ���һ������H2O2
20��14C��һ�ַ�����ͬλ�أ��ڸ߲���������������߲��������ӻ�˱�ը���������Ӻ��14N��ʹ��ת��Ϊ14C��14N+![]() ��14C+
��14C+![]() ������˵����ȷ���ǡ���������
������˵����ȷ���ǡ���������
������ A��14C��14N��Ϊͬλ��
������ B��14C��C60��ͬ��������
������ C��14CO2��Ħ������Ϊ46������
������ D�������ϻ��ŵ��������ڣ������³´�������Ҳ����14C
�ڢ�������ѡ���⣺��40�֣�
���������������С�⣬��19�֣�
21��(9��) (1) �����й�ʵ��������жϲ���ȷ���� _________�����й���ţ���
A����10 mL��Ͳ��ȡϡ������Һ 8.0 mL
B���ø����pH��ֽ�ⶨ��ˮ��pH
C���ü�ʽ�ζ�����ȡKMnO4��Һ 19.60 mL
D��ʹ������ƿ������Һʱ������Һ�涨�ݺ�������Һ��Ũ��ƫ��
E��Բ����ƿ����ƿ�����������ʱ��Ӧ����ʯ������
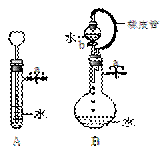 ��2��������ͼ�����ش��������⣺
��2��������ͼ�����ش��������⣺
���ر�ͼAװ���е�ֹˮ��a�ӳ���©�����Թ�
��ע��һ������ˮ�����ú���ͼ��ʾ�����жϣ�Aװ����
��©�������©����������©����������ȷ������������
���ر�ͼBװ���е�ֹˮ��a��������b��ˮ����
���µΣ�ֱ��ȫ��������ƿ�����жϣ�Bװ���Ƿ�©����
���©����������©����������ȷ���������������� ��
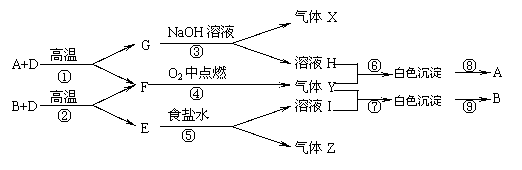 22.( 10��)��֪A��B��E�ǹ��廯���D��G�ǹ��嵥�ʣ�X��Z��FΪ��ȼ�����壬F��X�Ļ���ʵ���ɫ������֮��������ת����ϵ��
22.( 10��)��֪A��B��E�ǹ��廯���D��G�ǹ��嵥�ʣ�X��Z��FΪ��ȼ�����壬F��X�Ļ���ʵ���ɫ������֮��������ת����ϵ��
��д��A��B��Z�����ƣ�A������������ ��B������������ ��Z������������
��д��Y�Ľṹʽ���������������� ��A�ľ���ṹ���ͣ������������������� ��
�� ��ҺH�ı���Ҫ������������ ���������������������������� ��
�ǰ�Ҫ��д����Ӧ����ʽ��
�ٵĻ�ѧ����ʽ������������������������������������������
�����ӷ���ʽ��������������������������������������������
���������9�֣�
23����A��B��C��D��E���ֶ�����Ԫ�أ����ǵ�ԭ���������ε�������֪��A��C��B��D�ֱ�λ��ͬ���壬��B��D��������֮����A��C������֮�͵�2����E��ͬ����Ԫ����ԭ�Ӱ뾶��С����ش�
��A2B��A2D�ķе�ϸ���Ϊ���� ���ѧʽ������ԭ���������������������������� ��
����A��B��C��D����Ԫ���γɵ����ֻ�������䷴Ӧ�����ӷ���ʽΪ��������������
��д����B��C��Ԫ�����γɵ�ԭ�Ӹ�����Ϊ1�U1�Ļ�����ĵ���ʽ__________���侧���д��ڵĻ�ѧ����____________________���ѧ�����ƣ���
���ö��ʯī�缫�����з�̪��C��E�γɵĻ�����ı�����Һ����ͨ��Դһ��ʱ���������������缫���ƣ��������ֺ�ɫ����һ���ĵ缫��ӦʽΪ������������������ �������������������������� ����ü����ò��
![]()
 �ģ�������(��12��)
�ģ�������(��12��)
24����12�֣���50mLNaOH��Һ����������ͨ��һ������CO2�����ȡ����Һ100mL�������ϡ�ͺ����Һ����μ���0.1mol/L��HCl��Һ��������CO2�������������������������������֮��Ĺ�ϵ����ͼ��ʾ��
|
�Է���NaOH������CO2������ڼ�������Һ�д��ڵ��������������������� ��
�����ʵ���֮���������� ���� ��������CO2������������������������������ ��
��������Һ�д��ڵ������������������������������������������������� ��
�����ʵ���֮���������� ��������CO2������������������������ ��
����������
һ��ѡ���⣨���20��С�⣬ÿ��3�֣���60�֣�ÿ��ֻ��һ��ѡ��������⣩
| ��� | 1 | 2 | 3 | ��4 | 5 | 6 | 7 | 8 | 9 | 10 |
| �� |
|
|
|
|
|
|
|
|
|
|
| ��� | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| �� |
|
|
|
|
|
|
|
|
|
|
���������������С�⣬��19�֣�
21��(ÿ�ո�3�֣���9��) ( 1 ) �����й�ʵ��������жϲ���ȷ���� _________�����й���ţ���
��������2 ����_______________�� ����_______________;
22.( ����ʽ2�֣������1�֡���10��)
��д��A��B��Z�����ƣ�A������������ ��B������������ ��Z������������
��д��Y�Ľṹʽ���������� ��������A�ľ���ṹ���ͣ������������������� ��
�� ��ҺH�ı���Ҫ���������������������������������������� ��
�ǰ�Ҫ��д����Ӧ����ʽ��
�ٵĻ�ѧ����ʽ������������������������������������������
�����ӷ���ʽ��������������������������������������������
23.����9�֣�
��1��(1��)____________________. (2��) _______________________________________;
(2) (2��)_________________________________________.
(3) (1��)��_______________ (1��).________________
(4) (2��)_______________________________________;
24.( ÿ��2�� ��12��)
�ڼ�������Һ�д��ڵ��������������������� �������ʵ���֮�������������� ��������CO2������������������������������ ��
��������Һ�д��ڵ������������������������������������������������� ��
�����ʵ���֮���������� ��������CO2������������������������ ��