高考化学第一轮单元测试题(9)
第九单元 氮族元素
本试卷分第Ⅰ卷和第Ⅱ卷两部分,共100分,考试时间100分钟,可能用到的相对原子质量:
H: 1 O:16 C:12 Cu:64 N:14 Fe:56
第Ⅰ卷(选择题,共49分)
一、选择题(本题包括5小题,第小题2分,共10分。每小题只有一个选项符合题意)
1. 下列各组物质中,互为同位素的是 ( )
A.重氢、超重氢 B.氧、臭氧 C.红磷、白磷 D.乙酸、丙酸
2. 起固定氮作用的化学反应是 ( )
A.![]() 与
与![]() 反应生成
B.
反应生成
B.![]() 与
与![]() 反应生成
反应生成![]() 气体
气体
C.![]() 经催化氧化生成
经催化氧化生成![]() D.由
D.由![]() 制
制![]() 和
和![]()
3.
氨与重水(![]() )形成的碱与盐酸反应,这一反应生成的盐在溶液中电离生成的阳离子的化学式为
(
)
)形成的碱与盐酸反应,这一反应生成的盐在溶液中电离生成的阳离子的化学式为
(
)
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
4.在食品加工或餐饮业中使用量特别要注意严加控制的物质是 ( )
A.氯化钠 B.谷氨酸钠(味精) C.碳酸氢钠 D.亚硝酸钠
5.一定质量的铜和足量的浓硝酸或稀硝酸完全反应,在相同条件下用排水集气法收集产生的气体。下列叙述正确的是 ( )
①硝酸浓度越大,消耗的硝酸越少
②硝酸浓度不同,生成的![]() 的物质的量相同 ③硝酸浓度越大,产生的气体越少
④用排水集气法收集到的气体在相同状况下体积相同
的物质的量相同 ③硝酸浓度越大,产生的气体越少
④用排水集气法收集到的气体在相同状况下体积相同
A.只有② B.②④ C.③④ D.①②③
二、选择题(本题包括8小题,第小题3分,共24分。每小题有一个或两个选项符合题意)
6.对下列事实的解释正确的是 ( )
A.浓硝酸在光照下变黄,说明浓硝酸不稳定,且生成的产物可溶于浓硝酸
B.向某溶液中加入氯化钡溶液和稀硝酸。有白色沉淀生成,说明该溶液中一定含有![]()
C.常温下,将铜放入浓硫酸中无明显变化,说明铜在冷浓硫酸中钝化
D.氯气使湿润的碘化钾淀粉试纸变蓝,说明氯气与淀粉反应
7.据报道,近日某地一辆满载砒霜的大货车翻下山坡, 滑下河道,部分砒霜散落到河水中。砒霜的主要成分是![]() ,剧毒,致死量为0.1 g,可用于制造杀虫剂和灭鼠剂等。
,剧毒,致死量为0.1 g,可用于制造杀虫剂和灭鼠剂等。![]() 是两性偏酸性氧化物,其无色晶体在193℃升华,微溶于水,生成
是两性偏酸性氧化物,其无色晶体在193℃升华,微溶于水,生成![]() ;其对应的盐也均有毒性,其中碱金属对应的盐溶于水,其他金属对应的盐几乎不溶于水。根据以上信息判断,下列说法正确的是
( )
;其对应的盐也均有毒性,其中碱金属对应的盐溶于水,其他金属对应的盐几乎不溶于水。根据以上信息判断,下列说法正确的是
( )
A.![]() 的晶体为原子晶体
的晶体为原子晶体
B.![]() 是砷酸的酸酐
是砷酸的酸酐
C.可向该河中撒人生石灰,以消除砷对河水的污染
D.可向该河水中撤入氢氧化钠,以消除砷对河水的污染
8.氨是产量最大的化工产品,旧法亦称哈伯法:是在20―50![]() ,500℃,铁做催化剂下合成的;希腊化学家发明了一种新法,在常压下,把氢气和用氮气稀释的氮气分别通入一个加热到570℃的电解池,利用能通过氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,有关新法合成氨的说法不正确的是
,500℃,铁做催化剂下合成的;希腊化学家发明了一种新法,在常压下,把氢气和用氮气稀释的氮气分别通入一个加热到570℃的电解池,利用能通过氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,有关新法合成氨的说法不正确的是
( )
A. 新法与旧法相比不需要高温
B. 新法与旧法相比氮气的转化率高
C.新法阴极的电极反应为:![]()
D.电解时![]() 从阳极向阴极移动
从阳极向阴极移动
9.氢化铵(![]() )与氯化铵的结构相似,又知
)与氯化铵的结构相似,又知![]() 与水反应有
与水反应有![]() 生成,下列叙述不正确的是 ( )
生成,下列叙述不正确的是 ( )
A.![]() 是离子化合物
是离子化合物
B.![]() 溶于水后所形成的溶液显酸性
溶于水后所形成的溶液显酸性
c.![]() 与水反应时,
与水反应时,![]() 是氧化剂
是氧化剂
D.![]() 固体投入少量的水中,有两种气体产生
固体投入少量的水中,有两种气体产生
10.某单质跟浓硝酸反应时,每有0.25![]() 单质反应就消耗1
单质反应就消耗1![]() 硝酸,则该单质氧化后元素的化合价可能是
( )
硝酸,则该单质氧化后元素的化合价可能是
( )
A.+1 B.+2 C.+3 D.+4
11.将7g铁粉加入200 mL![]() 的硝酸溶液中,使之充分反应放出NO气体,所得溶液中主要离子浓度的关系是 ( )
的硝酸溶液中,使之充分反应放出NO气体,所得溶液中主要离子浓度的关系是 ( )
A. ![]()
B. ![]()
C. ![]()
D. ![]()
12.将![]()
![]()
![]() 、
、![]()
![]()
![]() 、
、![]()
![]()
![]() 的气体混合于同一试管里,将试管倒插于水中,充分反应后试管内气体全部消失,则
的气体混合于同一试管里,将试管倒插于水中,充分反应后试管内气体全部消失,则![]() 对
对![]() 、
、![]() 的函数关系式
的函数关系式![]() 是 ( )
是 ( )
A.![]() B.
B.![]() C.
C.![]() D.
D. ![]()
13.![]() 是离子化合物,它与水作用可产生
是离子化合物,它与水作用可产生![]() ,下列叙述正确的是 (
)
,下列叙述正确的是 (
)
A.![]() 与足量盐酸反应后生成两种盐
与足量盐酸反应后生成两种盐
B.在![]() 与水的反应中,
与水的反应中,![]() 作还原剂
作还原剂
C.![]() 与
与![]() 的电子层结构都与氖原子相同
的电子层结构都与氖原子相同
D.![]() 的半径大于
的半径大于![]() 的半径
的半径
三、选择题(本题包括5小题。每小题3分,共15分。每小题只有一个选项符合题意。)
14.相同状况下,在体积相同的三个烧瓶中分别盛满![]() 、
、![]() 和
和![]() 气体,并分别倒立在水槽里,充分溶解后烧瓶内三种溶液中溶质的物质的量浓度之比为(设烧瓶内液体未扩散到水槽里)
气体,并分别倒立在水槽里,充分溶解后烧瓶内三种溶液中溶质的物质的量浓度之比为(设烧瓶内液体未扩散到水槽里)
A.1:1:1 B.2:2:3 C.3:3:2 D.2:2:l
15.密度为0.91![]() 的氨水,质量分数为25%,该氨水用等体积的水稀释后,所得溶液的质量分数为 (
)
的氨水,质量分数为25%,该氨水用等体积的水稀释后,所得溶液的质量分数为 (
)
A.等于12.5% B.大于12.5% C.小于12.5% D.无法确定
16.已知![]() ,
,
![]() 由
由![]() 和
和![]() 组成的混合气体,其组成可表示为
组成的混合气体,其组成可表示为![]() 。该混合气体通入
。该混合气体通入![]() 溶液被完全吸收时,
溶液被完全吸收时,![]() 的值为 ( )
的值为 ( )
A. ![]() ≤1.5 B.
≤1.5 B.![]() =1.2
C.
=1.2
C. ![]() ≥1.5 D.无法确定
≥1.5 D.无法确定
17. 1.92g ![]() 投人到一定量的浓
投人到一定量的浓![]() 中,
中,![]() 完全溶解,生成气体颜色越来越浅,共收集到标准状况下672mL气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的
完全溶解,生成气体颜色越来越浅,共收集到标准状况下672mL气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的![]() ,恰好使气体完全溶于水,则通入
,恰好使气体完全溶于水,则通入![]() 的体积为 (
)
的体积为 (
)
A.504 mL B.336 mL C.224 mL D.168 mL
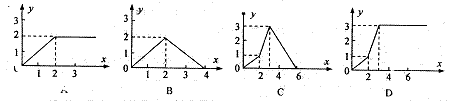
18.向含3![]()
![]() 的石灰水中逐滴加入
的石灰水中逐滴加入![]() 溶液至不再发生反应为止,所得沉淀的物质的量(纵坐标y)与加入
溶液至不再发生反应为止,所得沉淀的物质的量(纵坐标y)与加入![]() 的物质的量(横坐标
的物质的量(横坐标![]() )的关系图是 ( )
)的关系图是 ( )
 |
第Ⅱ卷(非选择题,共51分)
 四、(本题包括2小题,共15分)
四、(本题包括2小题,共15分)
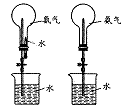
19.(7分)制取氨气并完成喷泉实验(图中夹持装置均已略去)
(1)写出实验室制取氨气的化学方程式: 。
(2)收集氨气应使用 法,要得到干燥的氨气可选用 做 干燥剂。
(3)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷 的操作是 。该实验的原理是 。
(4)如果只提供如图2的装置,请说明引发喷泉的方法。
20.(8分)为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去)。B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球。
(1) 实验时,先将B装置下移,使碳酸钙和稀硝酸接触产生气体;当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离。该组学生设计此步操作的目的为 。
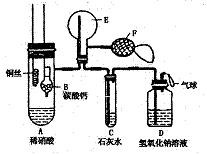 |
(2)将A中铜丝放人稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为 。
装置E中开始时出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深,产生上述现象的原因是 ;一段时间后,C中白色沉淀溶解,其原因是 。
(3)装置D的作用是 。
五、(本题包括2小题,共11分)
21.(5分)从某些方面看,![]() 和
和![]() 相当,
相当,![]() 与
与![]() 相当,
相当,![]() 和
和![]() 相当,
相当,![]() 、
、![]() 与
与![]() 相当。
相当。
(1)已知在液氨中能发生下列两个反应
①![]() ②
②![]()
试写出在水溶液中发生的与上述2个反应相当的化学方程式
,
(2)完成并配平下列反应方程式(M为二价金属)
![]() ――
;
――
;
![]() ―― ;
―― ;
![]() ―― 。
―― 。
22.(6分)亚磷酸![]() 是一种无色晶体,有大蒜气味和强吸湿性。
是一种无色晶体,有大蒜气味和强吸湿性。
(1)在亚磷酸溶液中加入过量的氢氧化钠溶液,生成的主要产物是![]() ,这一实验事实可证明亚磷酸是几元酸
,试写出亚磷酸的电离方程式:
。
,这一实验事实可证明亚磷酸是几元酸
,试写出亚磷酸的电离方程式:
。
(2)亚磷酸具有强还原性,当它与碘水混合后,可以看到碘水的棕黄色褪色,并有![]() 生成,写出有关方程式:
。
生成,写出有关方程式:
。
(3)在亚磷酸溶液中加入![]() 后,有黑色沉淀生成并且生成无色气体,试管口有红棕色气体产生。写出有关方程式
。
后,有黑色沉淀生成并且生成无色气体,试管口有红棕色气体产生。写出有关方程式
。
六、(本题包括2小题,共12分)
23.(6分)物质A--H有如下图所示转化关系(部分反应物、生成物没有列出)。其中,B的浓溶液与单质X在加热时才能发生反应①,B的稀溶液与足量X发生反应②,向C溶液中滴入KSCN溶液呈红色。试填写下列空白:
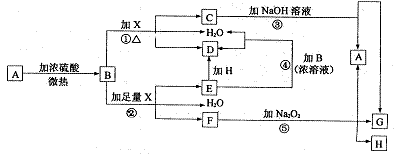 |
(1)晶体A是(化学式) ;
(2)反应②的离子方程式: ;
(3)根据图示信息判断,足量B的浓溶液与单质X共热时能否产生E,说明理由(用化学 方程式回答): .
(4)在反应⑤中,若生成物G与H的物质的量之比为4:1,写出F溶液与![]() 反应的化 学方程式:
。
反应的化 学方程式:
。
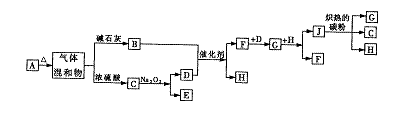 |
24.(6分)下图中A~J分别代表着有关反应中的一种物质,请填写以下空白:
(1)写出下列物质的化学式:
A. ;B: ;D: ;
(2)写出下列反应的化学方程式
①
![]()
②J和炽热的碳
③![]()
七、(本题包括2小题,共13分)
25.(7分)铁与![]() 作用时,还原产物除与
作用时,还原产物除与![]() 浓渡有关外,还与温度有关。已知在与冷稀
浓渡有关外,还与温度有关。已知在与冷稀![]() 反应时,主要还原产物为
反应时,主要还原产物为![]() 气体;在与热的稀
气体;在与热的稀![]() 作用时,主要还原产物为
作用时,主要还原产物为![]() 气体;当
气体;当![]() 更稀时,其重要还原产物是
更稀时,其重要还原产物是![]() 。现有铁与稀
。现有铁与稀![]() 的作用,请分析下图,回答有关问题。
的作用,请分析下图,回答有关问题。
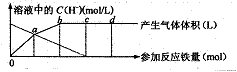 |
假设曲线的各段内只有一种还原产物。
(1)0点到a点的还原产物是: ;
(2)a点到b点的还原产物是 ,其原因是 ;
(3)试完成b点到c点的反应方程式:
![]()
(4)反应过程中,到达 点时![]() 已完全反应;
已完全反应;
(5)已知到达d点时,反应结束,此时溶液中的主要阳离子是 ;
(6)c点和d点参加反应的铁的物质的量之比是 。
26.(6分)硝酸工业尾气中氮的氧化物(![]() 、
、![]() )是大气污染物,可用基于下述反应的方法治理:
)是大气污染物,可用基于下述反应的方法治理:
![]()
![]()
现有标准状况下a L ![]() 和b L
和b L![]() 的混合气体(本题不考虑
的混合气体(本题不考虑![]() 的存在),恰好可被200mL
的存在),恰好可被200mL ![]() 溶液完全吸收。
溶液完全吸收。
(1)欲保证工业尾气全部被吸收,则a:b的值应控制在 范围;
(2) ![]() 溶液的物质的量浓度是
溶液的物质的量浓度是
![]() (用含a、b的代数式表示);
(用含a、b的代数式表示);
(3)试讨论a、b的值与生成的![]() 和
和![]() 的物质的量(设分别为
的物质的量(设分别为![]() )之间的关系:
。(用含a,b的代数式表示);
)之间的关系:
。(用含a,b的代数式表示);
①当生成的产物全部为![]() 时,
时,![]() 与a、b的关系;
与a、b的关系;
②当产物中兼有![]() 和
和![]() 时,
时,![]() 与a、b的关系;
与a、b的关系;
(4)若在标准状况下有![]() 、
、![]() 的混合物恰好与50 mL 2.0
的混合物恰好与50 mL 2.0 ![]() 的
的![]() 溶液反应完全。且生成
溶液反应完全。且生成![]() 和
和![]() 的物质的量的比值为4:1,则在混合气体中
的物质的量的比值为4:1,则在混合气体中![]() 气体的体积分数多大?
气体的体积分数多大?
单元检测题(九)参考答案
1.A 2.A 3.A 4.D 5.B 6.A 7.C 8.A 9.BC 10.BD 11.AD 12.C 13.AC
14.A 15.C 16.C 17.B 18.C
19.(1) ![]() (2)向下排空气 碱石灰
(2)向下排空气 碱石灰
(3)打开止水夹,挤出胶头滴管中的水 氨气极易溶于水,致使烧瓶内气体压强迅速减小
(4)打开夹子,用手(或热毛巾等)将烧瓶捂热,氨受热膨胀,赶出玻璃导管中的空气,氨气与
水接触,即发生喷泉.
20.(1)利用![]() 将装置内的空气排尽,避免生成的
将装置内的空气排尽,避免生成的![]() 被氧化
被氧化
(2) ![]() ;
;
![]()
(3)吸收尾气,防止污染
21.(1) ![]()
![]()
(2) ![]()
![]()
![]()
22.(1)二元酸; ![]()
![]()
(2) ![]()
(3) ![]()
![]()
23.(1) ![]()
(2) ![]()
(或![]() )
)
(3)由反应④![]() (浓)
(浓) ![]() 可知在浓
可知在浓![]() 中不可能生成
中不可能生成![]()
(4) ![]()
24.(1) A:![]() B:
B: ![]() D:
D: ![]()
(2)①![]()
②![]() (浓)
(浓) ![]()
③![]()
25.(1) ![]() (2)
(2) ![]() ;反应放热,使溶液温度升高
;反应放热,使溶液温度升高
(3)8,30,8,![]() ,9 (4) C (5)
,9 (4) C (5) ![]() (6)2:3
(6)2:3
26.(1)![]() (2)
(2)![]()
(3)①![]() ②
②![]()
(4)37.5%