高考化学试测题4
第Ⅰ卷
一、选择题(本题包括6小题,每小题4分,共24分,每小题只有一个选项符合题意)
1.某气体在近地面空气中浓度稍大时是一种污染物,而在高空却对人类有保护作用,该气体是
A.NO B.O3 C.CO D.氯氟烃
2.以石墨作电极,电解氯化铜溶液,若电解时转移的电子数是3.01×1023,则此时在阴极析出铜的质量是
A.8g B.16g C.32g D.64g
3.室温下0.1mol·L-1NaOH溶液滴定amL某浓度的HCl溶液,达到终点时消耗NaOH溶液bmL,此时溶液中氢离子的浓度[H+]/mol·L-1是
A.![]() B.
B.![]() C.1×107 D.1×10-7
C.1×107 D.1×10-7
4.可以将反应Zn+Br2=ZnBr2设计成蓄电池,下列4个电极反应
①Br2+2e=2Br- ②2Br-—2e=Br2
③Zn-2e=Zn2+ ④Zn2++2e=Zn
其中表示充电式的阳极反应和放电时的负极反应的分别是
A.②和③ B.②和① C.③和① D.④和①
5.分子式与苯丙氨酸(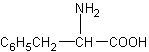 )相同,且同时符合下列两个条件:①有带两个取代基的苯环 ②有一个硝基直接连接在苯环上的异构体的数目是
)相同,且同时符合下列两个条件:①有带两个取代基的苯环 ②有一个硝基直接连接在苯环上的异构体的数目是
A.3 B.5 C.6 D.10
6.将氨水逐滴加入到稀盐酸中,使溶液成中性,则此时
A.[NH4+]=[Cl-] B.[NH4+]>[Cl-] C.[NH4+]<[Cl-] D.[NH4+]与[Cl-]之间关系不确定
二、选择题(本题包括6小题,每小题4分,共24分,每小题有一个或两个选项符合题意。若正确答案包括一个选项,多选时,该题为0分。若正确答案包括两个选项,只选一个,且正确的,给2分;选两个且都正确的,给4分,但只要选错一个,该小题为0分)
7.在锌片和盐酸的反应中,加入下列试剂,可是生成氢气的速率变慢的是
A.硫酸铜晶体 B.水 C.氯化钡晶体 D.醋酸钾晶体
8.某溶液中含三种离子,加入过量氨水有沉淀,过滤后滤液中加入过量盐酸,又有沉淀声称,再过滤,滤液中加入过量Na2CO3溶液,仍有沉淀声称,原溶液中含有的离子可能是
A.Ag+、Fe2+、Ca2+ B.Al3+、Mg2+、Ba2+
C.Ca2+、Fe2+、Ba2+ D.Ag+、Mg2+、Ba2+
9.在一杯透明的液体中加入一小颗固体,整杯液体完全转变成固体,则原液体和析出的固体分别可能是
A.过饱和溶液,不带结晶水的晶体 B.饱和溶液,带结晶水的晶体
C.过饱和溶液,带结晶水的晶体 D.-10℃的过冷水,冰
10.A和M为两种元素,已知A位于短周期,且A2-与M+的电子数之差为8,则下列说法正确的是
A.A和M原子的电子总数之和可能为11 B.A和M的原子序数之差为8
C.A和M原子的最外层电子数之和为8 D.A和M原子的最外层电子数之差为7
11.下列说法正确的是
A.电解NaOH溶液时,溶液浓度将减小,pH增大
B.电解H2SO4溶液时,溶液浓度将增大,pH减小
C.电解Na2SO4溶液时,溶液浓度将增大,pH不变
D.电解NaCl溶液时,溶液浓度将减小,pH不变
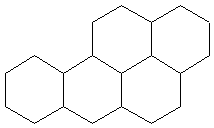 12.苯并[a]芘是一种稠环芳香烃(它的分子是研究致癌效应的参照标准),其结构式中有5个环互相并和如图。每个碳原子上都一个双键(C=C),分子中共有m个双键,五个环都处于同一平面上,分子中可能同时处于一个平面上的原子数为n个,则m、n分别等于
12.苯并[a]芘是一种稠环芳香烃(它的分子是研究致癌效应的参照标准),其结构式中有5个环互相并和如图。每个碳原子上都一个双键(C=C),分子中共有m个双键,五个环都处于同一平面上,分子中可能同时处于一个平面上的原子数为n个,则m、n分别等于
A.10、30 B.10、32 C.11、30 D.11、32
第Ⅱ卷
(共四大题,9小题,共76分)
三、(本大题共2小题,共19分)
13.(6分)把淀粉溶液溶于沸水中,制成淀粉胶体。
(1)鉴别水溶液和胶体可以利用的方法是
。
(2)60℃左右时,在淀粉胶体中加入淀粉酶,充分反应。然后把反应后的全部液体装入半透膜袋里,系紧袋口,并把它悬挂在盛有蒸馏水的烧杯里。从半透膜袋里析出的物质是
,该操作的名称是 。
14.(13分)1,2,3,4—四氢化萘的结构简式是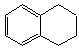 ,分子式是C10H12。常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2
,分子式是C10H12。常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2![]() C10H8Br4+4HBr。生成的四溴化萘常温下为固态,不溶于水。有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下:
C10H8Br4+4HBr。生成的四溴化萘常温下为固态,不溶于水。有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下:
①按一定质量比把四氢化萘和水加入适当的容器中,加入少量纯铁粉。
②慢慢滴入液溴,不断搅拌,直到反应完全。
③取下反应容器,补充少量四氢化萘,直到溶液颜色消失。过滤,将滤液倒入分液漏斗,静置。
④分液,得到的“水层”即氢溴酸溶液。
回答下列问题:
(1)下面示意图中的装置,适合步骤①和②操作的是 。
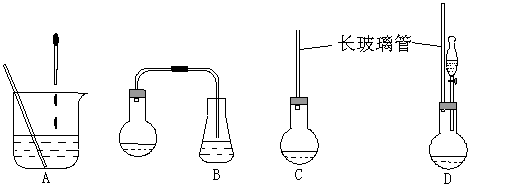
(2)步骤②中如何判断“反应完全” 。
(3)步骤③中补充少量四氢化萘的目的是 。
(4)步骤③中过滤后得到的固体物质是 。
(5)已知在实验条件下,饱和氢溴酸水溶液中氢溴酸的质量分数是66%,如果溴化反应进行完成,则步骤①中四氢化萘和水的质量比约是1︰ (保留小数点后1位)。
四、(本大题共3小题,共22分)
15.(6分)若以X、Y和Z代表三种元素,且知X与Y可形成原子数之比为1︰1的化合物甲,Y与Z也可形成原子数之比为1︰1的化合物乙,又知甲分子含18个电子,乙分子含38个电子,请填空:
(1)元素Y在第 周期。
(2)化合物甲的分子式是 。
(3)化合物乙的分子式是 。
16.(5分)请写出10个分子式,使每个分子中都含有18个电子。
、 、 、 、 、
、 、 、 、 、
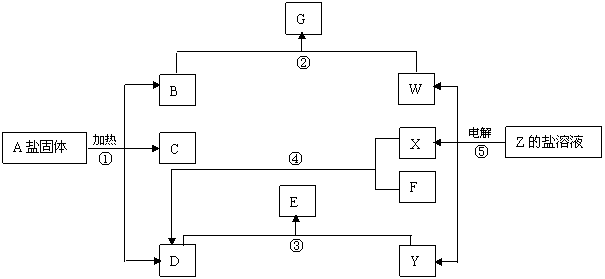
17.(11分)
在一定条件下(不许添加别的反应物),经不同的化学反应,可实现如上图的各种变化。其中,反应③、④、⑤属氧化还原反应,而反应①、②属非氧化还原反应。X、F和Y为单质,且F是空气的主要成分之一,其余为化合物,据此请填空:
(1)物质A是 ,F是 ,X是 ,Y是 。
(2)写出反应②的化学方程式 。
(3)写出反应④的化学方程式 。
五、(本大题共2小题,共16分)
18.(6分)ATP(三磷酸腺苷)的结构如下:
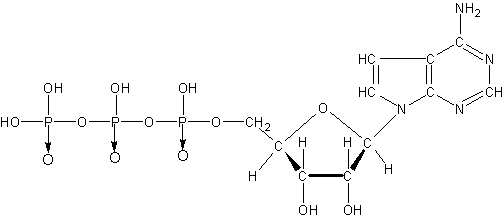
(式中“→”表示配位键,粗线表示这个环上的这些键在纸平面的前面。)
|
又知ATP+H2O![]() ADP+Pi(磷酸)+能量
ADP+Pi(磷酸)+能量
请写出:
(1)ATP的分子简式是 ,它的摩尔质量是 。
(2)ADP的结构式是 。
19.(10分)有三个只含C、H、O的有机化合物A1、A2、A3,它们互为同分异构体。室温时A1为气态,A2、A3是液态。分子中C与H的质量分数是73.3%。在催化剂(Cu、Ag等)存在下,A1不起反应。A2、A3分别氧化得到B2、B3。B2可以被硝酸银的氨水溶液氧化得到C2,而B3则不能。
上述关系也可以表示如下图:
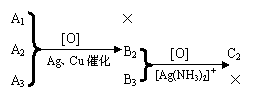 |
请用计算、推理,填写下列空白:
(1)A2的结构简式 ;
(2)B3的结构简式 ;
(3)A3 和C2的反应产物 。
六、(本大题共2小题,共19分)
20.(9分)某有机化合物爆炸后的气体中,各组份的体积分数如下:CO241.38%,H2O(气)34.48%,N220.69%,O23.45%。设爆炸时,并没有掺入空气,试推算该化合物的:
(1)最简式 。
(2)分子式 。
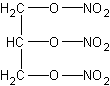
(3)结构式 。
21.(10分)某化工厂每小时生产98%(质量分数)硫酸at(吨),为使硫充分燃烧,且在下一步催化氧化时不再补充空气,要求燃烧后的混合气体中含氧气的体积分数为b%。若空气中氧气的体积分数为21%,且不考虑各生产阶段的物料损失,则
(1)该厂每小时消耗标准状况下空气的体积为 m3。
(2)为满足题设需求,b%的下限等于 。
化学试测题答案
一、(每小题4分,共24分)
1.B 2.B 3.D 4.A 5.C 6.A
二、(每小题4分,共24分)
7.BD 8.AD 9.C 10.A 11.BC 12.B
三、(本大题共2小题,共19分)
13.(6分)
(1)用可见光照射胶体,观察有无“丁达尔现象”,有就是胶体
(2)麦芽糖 渗析
14.(13分)
(1)D
(2)加入的液溴颜色基本不褪
(3)出去过量的溴
(4)四溴化萘、铁粉
(5)1.3
15.(6分)
(1)第二周期
(2)H2O2
(3)Na2O2
16.(5分)
(1)Ar、F2、HCl、H2S、PH3、SiH4、H2O2、N2H4、C2H6、CH3OH、CH3NH2……
只回答出其中的10种即可,其它合理答案都可以。
17.(11分)
(1)A是(NH4)2CO3(或NH4HCO3),F是N2,X是H2,Y是Cl2。
(2)CO2+2NaOH=Na2CO3+H2O(或CO2+NaOH=NaHCO3)
 |
(3)N2+3H2![]() 2NH3
2NH3
五、(本大题共2小题,共16分)
18.(6分)
(1)A—P~P~P;507
(2)
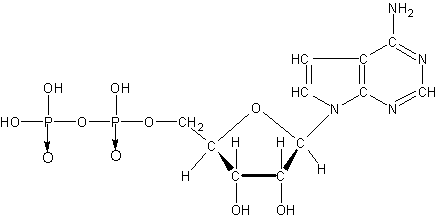
19.(10分)
(1)CH3CH2CH2OH
(2)
![]()
(3)CH3CH2COOCH(CH3)2
六、(本大题共2小题,共19分)
20. (9分)
(1)C3H5N3O9
(2)C3H5N3O9
(3)
21.(10分)
(1)![]()
(2)7%