|
2005-2006学年度上学期
高中学生学科素质训练
高三化学同步测试(新授2)―《物质的检验》
第I卷(选择题,共72分)
一、选择题(共8小题,每小题4分,每小题只有一个答案符合题意)
1.鉴别纯碱、石灰石、芒硝和石膏四种固体,应选用 ( )
A.烧碱溶液 B.水和盐酸 C.硝酸 D.氯化钡和硝酸混合液
2.能对Ca(OH)2、K2SO3、NaCl和Na2CO3四种溶液作出鉴别的试剂是 ( )
A.NaHCO3 B.HNO3 C.MgCl2 D.H3PO4
3.只用水就鉴别的一组物质是 ( )
A.苯、乙酸、四氯化碳 B.乙醇、乙醛、乙酸
C.乙醛、乙二醇、硝基苯 D.苯酚、乙醇、甘油
4.使用一种试剂,可以把甲醇、乙醛、乙酸、葡萄糖的水溶液区别开来,应选 ( )
A.溴水 B.银氨溶液 C.FeCl3溶液 D.新制Cu(OH)2
5.把五瓶有编号的溶液K2CO3、KNO3、K2SO4、KOH、Ba(OH)2一一区别开来,则所用试
剂的种类是 ( )
A.不用任何其它试剂 B.只用一种试剂
C.两种试剂 D.用三种试剂
6.下列各组溶液,只用组内溶液互相混合的方法(不外加试剂)就能鉴别的一组是( )
A.BaCl2 K2SO4 KNO3 NaCl B.Na2SO4 Na2CO3 BaCl2 KCl
C.NaOH Na2SO4 FeCl3 MgCl2 D.NaCl AgNO3 NaNO3 HCl
7.能大量共存于同一溶液中,且在该溶液中加入足量NaOH溶液有沉淀析出,若加入足量
H2SO4也有沉淀生成的下列离子组是 ( )
A.AlO2- Na+ K+ NO3- B.Ag+ K+ H+ NO3-
C.Fe3+ Cl- Ba2+ Na+ D.K+ SiO32- Ca2+ PO43-
8.除去下列气体中的有关杂质(括号内为杂质),选用的试剂最好的是 ( )
A.SO2(SO3气体),用Na2SO3饱和溶液和P2O5
B.C2H6(C2H4):用溴水和石灰水
C.H2S(H2O蒸气):用浓H2SO4
D.NO(NO2) ;用烧碱溶液和浓H2SO4
二、选择题(共10小题,每小题4分,每小题有1-2个答案符合题意)
9.检验下列各物质是否已部分氧化而变质,所选用的试剂(括号内)不正确的是 ( )
A.福尔马林溶液(石蕊试液) B.碘化钾溶液(淀粉溶液)
C.Na2SO3溶液(BaCl2溶液) D.FeCl2溶液(KSCN溶液)
10.有Na2CO3 AgNO3 BaCl2 HCl及NH4NO3五瓶无标签的溶液,为鉴别它们,取四支试管分
别装入一种溶液,再向上边四支试管中加入少许剩下的一种溶液,则下列表述错误的是
( )
A.若三支试管出现沉淀时,则后加入的是AgNO3
B.全部没有什么现象变化时,则后加入的是NH4NO3
C.一支试管出现气体,另两支试管出现沉淀时,最后加入的盐酸
D.若只有两支试管出现沉淀时,则后加入的是BaCl2溶液
11.能将分别含有Cu2+、Fe3+、Al3+、Mg2+、Fe2+、NH4+、Na+等离子的七种溶液一次性鉴别
开来的试剂是 ( )
A.NaHCO3溶液 B.KSCN溶液 C.NaOH溶液 D.NH3・H2O溶液
12.只用一种试剂就可以鉴别NaHCO3、Na2S2O3、K2SO3、Na2SiO3、KCl、K2S六种无色溶
液,这种试剂是 ( )
A.硫酸 B.硝酸 C.澄清的石灰水 D.盐酸
13.下列五种粉末状物质:硅酸、氧化镁、碳酸钠、硫酸铝、氢氧化铝,为鉴别它们,除已
有蒸馏水外,还必须使用的一组试剂应该是 ( )
A.NaOH溶液和CO2 B.盐酸和NaOH溶液
C.盐酸和CO2 D.BaCl2溶液和H2SO4
14.只用一种试剂即可区别NaBr、NaI、NaOH、Na2CO3、 NaSCN、H2S、AgNO3、C6H5OH
等8种无色溶液,这种试剂为 ( )
A.硫酸 B.氨水 C.FeCl3溶液 D.盐酸
15.常温下用化学方法,但不用其它试剂就能区别开来的溶液组是 ( )
A.AlCl3 CaCl2 H2SO4 NaHCO3
B.BaCl2 NaNO3 Na2SO4 Na2CO3
C.Ca(OH)2 BaCl2 Na2CO3 NaCl
D.FeCl2 Na2SO4 AlCl3 Ba(OH)2
16.下列各组物质的溶液,不用其它试剂就可以将它们区别开的是 ( )
A.C6H5OH、C2H5OH、CH3COOH、AgNO3、FeCl3
B.NaOH、Na2CO3、NaAlO2、Na2S2O3、HCl
C.NaOH、Al2(SO4)3、NaHSO4、Na2CO3、MgSO4
D.BaCl2、Na2SO4、CaCl2、Ca(NO3)2、Na2CO3
17.为了检验某溶液中是否含有SO42-,下列操作最合理的是 ( )
A.加入用HNO3酸化的Ba(NO3)2溶液
B.先用HNO3酸化,再加Ba(NO3)2溶液
C.先用盐酸酸化,再加BaCl2溶液
D.直接加入盐酸酸化的BaCl2溶液
18.含8.0g NaOH的溶液中通入一定量H2S后,将得到的溶液小心蒸干,称得无水物7.9g,则该无水物中一定含有的物质是 ( )
A.Na2S B.NaHS
C.Na2S和NaHS D.NaOH和NaHS
第Ⅱ卷 (共78分)
![]()
![]() 19.(10分)有编号为A、B、C、D、E的五种透明溶液,它们是:盐酸、AgNO3、 BaCl2、
19.(10分)有编号为A、B、C、D、E的五种透明溶液,它们是:盐酸、AgNO3、 BaCl2、
Na2CO3和Al2(SO4)3,下表是它们彼此两两混合进行实验的现象:(↑表示有气体生成,
↓表示有沉淀生成)。
溶液编号:A+B A+C A+E C+D B+D
![]()
![]()
![]()
![]()
![]()
![]() 实验现象:
实验现象:
则各编号的物质是:A B C D E
20.((10分)贮气袋中贮有有色气体,可能由NO2、 CH4 、CO2、 HCl 、NH3 、Br2 (蒸
气)等气体中的几种混合而成。现进行如下实验:
①通入少许水中,得无色溶液;
②通入少许AgNO3溶液中,有沉淀析出;
③通入少许澄清石灰水中,无浑浊现象;
④通过盛水的洗气瓶后,导出的气体再通入澄清的石灰水,石灰水变浑浊
试回答:由①可判断一定存在 ,一定不存在 ;由②可判断一定
存在 ,一定不存在 ;由③④可判断一定存在 ,可能存在
的是 。
21.(8分)某无色溶液可能是由Na2CO3、 NaOH 、MgCl2 、AlCl3、 BaCl2 、Fe2(SO4)3 、
(NH4)2SO4溶液中的两种或两种以上混合而成。取该溶液,向其中加入H2SO4,有白色
沉淀生成,继续加入H2SO4时沉淀又完全消失,整个实验过程中无气体产生,则原溶液
是由 和 混合而成,实验过程中有关的离子反应方程式是
__________________________________________________
22.(12分)实验室常用燃烧分析法来测定有机物中碳和氢的质量分数,这种方法是用氧化
铜作催化剂,在750℃时,用氧气流将样品氧化成CO2和H2O,再根据CO2和H2O的质
量求出有机物中碳和氢的质量分数.现用下列各仪器装置来确定乙炔分子中碳、氢两种
元素的质量比.
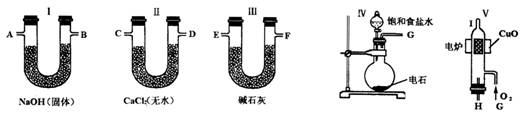
回答下列问题:
(1)若产生的气体由左向右流向,各装置导管的连接顺序是:________接________、
________接________、________接________、________接________、________接
________.
(2)装置Ⅰ的作用是_______;装置Ⅱ的作用是________;装置Ⅲ的作用是________.
(3)装置Ⅳ中的化学方程式______ ________;
装置Ⅴ中的化学方程式______________ __.
(4)实验前称得Ⅰ、Ⅱ两装置的质量分别变为m2g和n2g,实验完毕,称得Ⅰ、Ⅱ两装
置的质量分别变为m2g和n2g和,则乙炔分子中碳原子和氢原子的原子个数比为___ _ (列出算式).
23.(16分)某无色溶液,其中有可能存在的离子如下:Na+、Ag+ 、Ba2+ 、Al3+ 、AlO2- 、
S2- 、CO32- 、SO32- 、SO42-。现取该溶液进行有关实验,实验结果如下图所示:
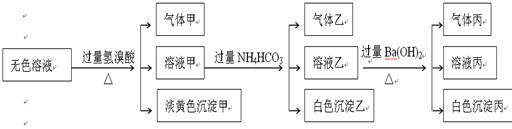
请回答下列问题:
(1)沉淀甲是 ,生成沉淀的离子方程式 。
(2)沉淀乙是 ,由溶液甲生成沉淀乙的离子方程式 。
(3)沉淀丙是 ,如何用一化学实验来确定其成分 。
(4)气体甲成分有哪几种可能? 。
(5)综合上述信息,可以肯定存在的离子有 。
24.(10分)(05上海高考)某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图。
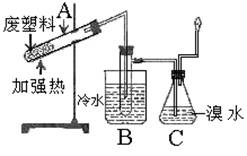 |
加热聚丙烯废塑料得到的产物如右表:
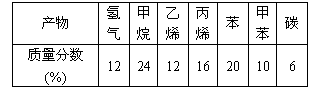
(1) 试管A中残余物有多种用途,如下列转化就可可制取高聚物聚乙炔。
|
|
|
|
|
|
![]()
![]()
![]() A中残留物
A中残留物
写出反应②~③的化学方程式 、
。
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有
种。
(3)锥形瓶C中观察到的现象 。
经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为 。
(4)写出C中逸出的气体在工业上的两种用途 、
。
25.(12分)植物生长需要营养,实验室现有一包由氯化铵和硫酸铵混合而成的白色粉末,课外小组的同学按下图实验设计进行实验,测定这种混合物中各组分的含量,以便给植物施用.
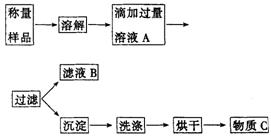
(1)溶液A中溶质的化学式_______________________________________________.
(2)他将样品放入托盘天平的右盘中,样品质量记录游码为0.4g,左边的托盘里的砝
码为16g,则样品质量是________g.
(3)若过滤使用的仪器和用品已有:滤纸、铁架台、铁圈、烧杯、漏斗,还需要补充的
仪器或用品是________________________.
(4)怎样证明滴加溶液A已经过量,简述操作方法______________________________.
(5)若物质C的质量为23.3g,那么原混合物中氯化铵的质量分数为________.
物质的检验参考答案
1、B 2、D 3、A 4、D 5、C 6、C 7、C 8、D 9、C 10、C 11.C
12.A、D 13.B 14.C 15.A、D 16.B、C 17、C 18、A
19、A、Na2CO3 B、HCl C、BaCl2 D、AgNO3 E、Al2(SO4)3
20、NO2;Br2(蒸气);HCl ; NH3 ;CO2 ; CH4
21、AlCl和NaOH ; Al3++4OH-=AlO2-+2H2O
![]() AlO2-+H++H2O=Al(OH)3 Al(OH)3+3H+=Al3++3H2O
AlO2-+H++H2O=Al(OH)3 Al(OH)3+3H+=Al3++3H2O
22、本题考查学生乙炔的制取方法、干燥、氧化原理及产物的吸收测定顺序.由于制得的乙炔气含水对燃烧及产物测定有影响,故制得的乙炔气体必须先干燥,然后再进行题中的催化氧化,乃至测定产物的质量.所以(1)G、E、F、H、I、C、D、A
(2)吸收燃烧产生的![]() 气体;吸收产生的水蒸气;吸收乙炔中的水蒸气.
气体;吸收产生的水蒸气;吸收乙炔中的水蒸气.
(3)![]()
![]()
(4)![]()
![]() 23、(1)S 2S2-+SO32-+6H+=3S
+3H2O
23、(1)S 2S2-+SO32-+6H+=3S
+3H2O
![]()
![]() (2)Al(OH)3 Al3+3HCO3-
= Al(OH)3 +3CO2
(2)Al(OH)3 Al3+3HCO3-
= Al(OH)3 +3CO2
(3)BaCO3,BaSO4必在其一,取沉淀加稀HNO3,若沉淀完全消失,则为BaCO3,若沉淀部分溶解且产生气泡,则二者都有,若沉淀无任何变化,则为BaSO4
(4)H2S SO2 CO2 H2S和CO2 SO2和CO2
(5)S2- SO32- AlO2-
24、(本题共8分)
![]()
![]() (1)CaC2 + 2H2O → Ca(OH)2 + C2H2↑ nHC≡CH → [ HC=CH ]
(1)CaC2 + 2H2O → Ca(OH)2 + C2H2↑ nHC≡CH → [ HC=CH ]
(2)4
(3)棕黄色溶液变无色或褪色 4.8
(4)合成氨原料,作燃料或有机化工原料(其他合理答案均给分)
25.(1)BaCl2 [或Ba(NO3)2] (2)15.6g (3)玻璃棒
(4)取经过沉降后的上层清液,逐滴加入稀H2SO=4溶液,若观察有沉淀生成,说明滴
加BaCl2溶液已过量.(5)15.4%
