����ʦ���и����������¿�
��ѧ�Ծ�
�����ˣ�Ф���ɡ��������ˣ�������ѧ������
���ԭ��������H��1����C��12����O��16
�ڢ��(ѡ���⣬��48��)
��1�����۲�H2ȼ�յ���ɫ��ȼ�����ܿڵIJ��������
����A���Ʋ�������B���ز�������C��ʯӢ��������D��ͭ��
��2�����и������ʵ����ʱȽϣ�����ȷ����
����A���۵�![]() �� �� B���ܽ��
�� �� B���ܽ��![]()
����C����ԭ��![]() ����D��������
����D��������![]()
��3������ȥС�մ���Һ�л��е������մ���ü���(��ͨ��)
����A����ʯ�ҡ���B��̼����ơ���C�����ᡡ��D��������̼
��4�����н���ұ���ķ�Ӧԭ�����������
����A��![]()
![]()
![]() B
B![]() ��MgO+H2
��MgO+H2![]() Mg+H20
Mg+H20
����C��Fe304+4CO![]() 3Fe+4C02����D��2HgO
3Fe+4C02����D��2HgO![]() 2Hg+02 ��
2Hg+02 ��
5���õ�����С�մ���ȡC02�����â����շ����������÷������ַ����õ�CO2����
A���ٴ��ڢڡ����� B����С�ڢڡ���
C����ȡ��������� D�����Ƚ�
��6�����г����ʵķ��������е���
����A���ù�����ˮ��ȥAl3+��Һ�е�����Fe3+
����B�����������ͨ�����ȵ�ͭ����ȥN2������02
����C�������Ƶ���ʯ�ң�ͨ�����������Գ�ȥ�Ҵ��е�����ˮ
����D���������ȥAgCl��������Ag2C03
��7����1L 1��Omol/L NaOH��Һ����0��8mol C02��������Һ�к���
����A��C032-����B��HC03-����C��C032-��HC03-��D��C032-��OH-
��8��1mol������������(1)Na20(2)Na0H(3)Na202(4)Na2S03�����ڷ����ڿ����У�����������(�����dz�������)��ȷ����
����A��(1)=(2)>(3)>(4)����B��(1)>(3)>(4)>(2)
C��(2)>(1)=(3)>(4)����D��(4)>(2)>(3)>(1)
9����0��2mol������Ͷ�뵽1��0��1mol��L�������У���Ӧ��ȫ����Ͷ��0��1mol�����ң������������зų��������Ľ�������
| �� A | �� B | �� C | �� D | |
| ������ | �� Mg | �� Na | �� K | �� Al |
| ������ | ����Al | �� K | �� Al | �� Mg |
��10��þ���ں��н϶�C02�Ŀ�����ȼ�պ���������
����A��MgO����B��MgO��Mg3N2����C��MgO��Mg(OH)2 ��D��MgO��Mg3N2��C
��11�������� ����������Ʒʢװ��ҩƷ��
����A��Ũ���ᡡ��B��Ũ���ᡡC��ϡ���ᡡD��CuSO4��Һ
��12��ij��ɫ����Һ��������Ӧ�ų�H2�������Һ�пɴ��������������
����A��H+��Cl-��Ba2+��Cu2+����B��OH-��Ba2+��K+��Na+
����C��H+��Na+��N03-��C1-���� D��OH-��Mg2+��NH4+��Cl-
��13�����з�Ӧ�����ӷ���ʽ��ȷ����
����A���������뱥��ʳ��ˮ��Na+2H20=Na++20H-+H2��
����B�������������Na20+2H+=2Na++H20
����c��С�մ����������Һ��HC03-+OH-=C02��+H20
����D��̼������������ʯ��ˮ��2HCO3-+Ca2++20H-=CaCO3 +C032-+2H2O
��14�����г������Լ�(�����е�����)��ѡ����ȷ����
����A��KHC03���K2C03(C02)����B��NaOH���Na202(H20)
����C��Na2C03���NaHC03(CaCl2)D��KN03���KHC03(HN03)
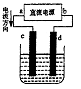 ��15����ͼ�ǵ��Na2C03��Һ��װ�ã�����c��dΪʯī�缫���������йص��ж���ȷ����
��15����ͼ�ǵ��Na2C03��Һ��װ�ã�����c��dΪʯī�缫���������йص��ж���ȷ����
����A��a������b������������������ B��a������b����
����C���������У�d�缫���������䡡��D���������У�C032-Ũ�Ȳ���
��16���ں���1molKAl(S04)2����Һ����μ���2molBa(OH)2��Һ�������й�˵������ȷ����
����A�������ɳ����������ȫ���ܽ�
����B������Һ��A13+��SO42-ȫ����������ʱ�������������ʵ������
����C�����õ��ij�����BaSO4
D�����ij���Ϊ2molBaS04��lmolAl(OH)3
�ڢ��(��ѡ���⣬��60��)
17��(8��)������ƿ��ɫ��Һ��һƿ��AlCl3��Һ��һƿ��NaOH��Һ�������κ��Լ����������ǵ�ʵ������������������� ������ʵ���������������ж���������������
������������ ������������������ �� �������Ļ�ѧ���ӷ���ʽΪ������������������
������������������ ��
����
18��(10��)����5ƿʧȥ��ǩ����Һ��ֻ֪�����Ƿֱ��ǣ�HCl��Na2C03��NaHC03��NaOH��Ca(HC03)2��ˮ��Һ��Ϊ�˼������ǣ��ֱ���A��B��C��D��EΪ���ţ������ǽ���һЩʵ�飬��¼���£�A��B���ʱ����������B��C���ʱ�г������ɣ�B��D��Ϻ�������E��A��ʹʯ����Һ��졣�ɴ���֪��
����A���������� B���� ������ C���������� D���������� E���������� ��
����
19��(22��)��ͼ��ʾ�������ʼ���������ת����ϵ������FΪ�������ܺ���������Ӧ�����������ʡ�E��KΪ��ɫ���嵥�ʣ��������ʾ�Ϊ�����AΪ��ɫ���壬CΪ��ɫҺ�塣�Իش��������⣺
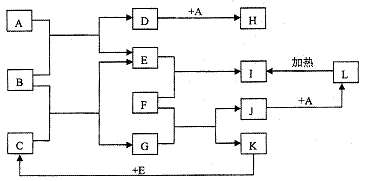 |
����(1)д��F����������Ӧ�Ļ�ѧ��Ӧ����ʽ��������������
����(2)д��E�����ƣ�������������
����(3)������B�ĵ���ʽΪ��������������
����(4)����A�ķ����д������������� ���������� ���ӣ�������������������� ���塣
����(5)д��B��C��Ӧ�Ļ�ѧ����ʽ������������
����(6)�ֱ�д��F��G��Ӧ�����ӷ�Ӧ����ʽ��J����L�����ӷ�Ӧ����ʽ��
(7)�ֱ�д��H�Ĺ���ת��ΪD��H����Һת��ΪD�Ļ�ѧ��Ӧ����ʽ��
������������������������������ ����������������������������������
20��(12��)ijУ��ѧС��ѧ��������ͼ����װ�ý��С�����ˮ��Ӧ����ʵ�飬�����ò����һ����ȡFeCl3��6H20���塣(ͼ�мгּ�β������װ�þ�����ȥ)
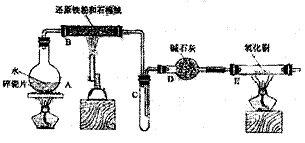 |
��(1)װ��B�з�����Ӧ�Ļ�ѧ����ʽ������������������������ ��
��(2)װ��E�е����������������������������������������� ��
��(3)ֹͣ��Ӧ����B����ȴ��ȡ���еĹ��壬�������ϡ�����ַ�Ӧ�����ˡ�����������Һ��Fe3+�IJ����������������������������������������������� ��
��(4)��С��ѧ������������Һ��ȡFeCl3��6H20���壬����������£�
������Һ FeCl3��Һ FeCl3��6H20����
���ٲ���I��ͨ��C12�������������������� ��
���ڲ���II��FeCl3ϡ��Һ�еõ�FeCl3�q6H20�������Ҫ����������
���۸��������豣�������������Ҫԭ����(������ӷ���ʽ��Ҫ˵��)��
���� ������������������������������������������������������������ ��
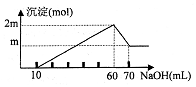
21��(8��)��һ��������������þ��Ʒ����30mL 1mol��Lϡ�����У���Ʒ��ȫ�ܽ⣬�����Һ����μ�������������Һ�����ɳ��������ͼ��ʾ���Իش�
��1�����ﵽ������ʱ����������������Һ�����Ϊ������ ml����ʱ����Һ�е�����Ϊ��������
��2) NaOH��Һ��Ũ��Ϊ��������������
��3��ԭ��Ʒ����������þ�����ʵ����ֱ�Ϊ����?
��4�������ɵij���Ϊ1��5mʱ������NaOH��Һ�����Ϊ����?
��ѧ���
| �� 1 | �� 2 | �� 3 | �� 4 | �� 5 | �� 6 | �� 7 | �� 8 |
| �� 9 | �� 10 | �� 11 | �� 12 | �� 13 | �� 14 | �� 15 | �� 16 |
�ڢ��(��ѡ���⣬��60��)
17��(8��)ʵ�������������������������������������������������������
������ʵ���������������ж�������������������������������������������
�����ӷ���ʽΪ�������������������������� ����������������������������
18��(10��)A����������B�������� ��C����������D���������� E���������� ��
19��(22��)(1)F ����������Ӧ�Ļ�ѧ����ʽ����������������������
��(2)E�����ƣ�������������
��(3)������B�ĵ���ʽΪ��������������
��(4)A�ķ����д������������� �����������������ӣ���������������� ���塣
��(5)B��C��Ӧ�Ļ�ѧ����ʽ������������������������������������
(6)F��G��Ӧ�����ӷ�Ӧ����ʽ���������������������������������� ��
���� J����L�����ӷ�Ӧ����ʽ������������������������������������ ��
��(7)H�Ĺ���ת��ΪD�Ļ�ѧ��Ӧ���̣����������������������������� ��
����H����Һת��ΪD�Ļ�ѧ��Ӧ����ʽ���������������������������� ��
20��(12��)(1)װ��B�з�����Ӧ�Ļ�ѧ����ʽ������������ ��
����(2)װ��E�е������������������������������� ��
����(3)������Һ��Fe3+�IJ���������������������
����(4)�ٲ���I��ͨ��C12�������������������� ��
�ڲ�����FeCl3ϡ��Һ�еõ�FeCl3��6H20�������Ҫ����������
������������������������������������������������������������
�������б��������������Ҫԭ����(������ӷ���ʽ��Ҫ˵��)��
����������������������������������������������������������
21��(8��)(1)���ﵽ������ʱ����������������Һ�����Ϊ���������� ml��
 ������ʱ����Һ�е�����Ϊ������������
��
������ʱ����Һ�е�����Ϊ������������
��
����(2)NaOH��Һ��Ũ��Ϊ��������������
(3)ԭ��Ʒ�������ʵ���Ϊ���������� ��
����þ�����ʵ���ΪΪ����������
��(4)�����ɵij���Ϊ1��5mʱ������NaOH��Һ�����Ϊ����?
�������¿���ѧ�ο���
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| C | B | D | B | B | A | C | B |
| 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| C | D | A | B | B | C | C | C |
17����8�֣���B����μ���A���������ɳ���������������ܽ⣬��AΪ![]() ��Һ
��Һ![]() ����
����
![]()
18����10�֣�![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]()
19����22�֣���1��F����������Ӧ�Ļ�ѧ����ʽ��![]()
��2����������3����4�����Լ����ۼ������Ǽ��ԡ� ����
��5��![]()
��6��![]()
![]() ��
��
![]()
��7��![]()
![]()
20����12�֣���1��![]() ��
��
��2����ɫ�����죬�Ҷ˹ܱ���ˮ�飨3��ȡ������Һ�����뼸����Һ���۲���Һ�Ƿ���ɫ
��4���ٽ�![]() ������
������![]() �� �ڼ���Ũ������ȴ�ᾧ������
�� �ڼ���Ũ������ȴ�ᾧ������
��![]() ��������������
��������������![]() ˮ��
ˮ��
21����8�֣���1��60![]() ��
�� ![]() ���� ��2��
���� ��2��![]()
��3��![]()
![]() ���� ��4��50
���� ��4��50![]() �� 65
�� 65![]()