第四单元 电解原理及其应用
一、基础知识填空
1.(1)原电池中较活泼的金属是_____极,较不活泼的金属(或能导电的非金属)是_______极。
(2)电解池中与外电源的正极相连的极板叫____极,与外电源的负极相连的极板叫_____极。
(3)原电池是把______能转化为________能的装置。电解池是把______能转化为________能的装置。在能量转化过程中,都发生了___ _______反应。
2.电解通电时,电子从电源的_____极沿导线流入电解池的_____极,在阴极区氧化性强的阳离子先得电子,被_________。同时,电子又从电解池的________流出,沿导线流回电源的正极,即在阳极区还原性强的阴离子(包括活性电极)先_______电子被_______。
3.当极板材料(阳极)为 Pt 或C时,称为______电极。当极板材料(阳极)为Cu等金属(除了Pt和C),还原性强,易_______电子,易被氧化称为_______电极。
阴离子放电顺序:S2- > I- > Br- >Cl- > OH- > 含氧酸根> F-
阳离子放电顺序:Ag+ > Hg 2+> Fe 3+> Cu 2+ >H+>……
4.当镀层金属作___极,含有镀层金属离子的电解质为电解液,把待镀金属制品浸入电镀液为____极时的电解即为_________。电镀时,由于两极得失电子相同,所以理论上电解液的浓度保持_________。
二、练习
高考试题:(四川.06)11.下列描述中,不符合生产实际的是 ( )
A. 电解熔融的氧化铝制取金属铝,用铁作阳极
B. 电解法精炼粗铜,用纯铜作阴极
C. 电解饱和食盐水制烧碱,用涂镍碳钢网作阴极
D. 在镀件上电镀锌,用锌作阳极
(全国I.06)09.把分别盛有熔融的氯化钾、氯化镁、氯化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比为 ( )
 A.1:2:3 B.3:2:1 C.6:3:1 D.6:3:2
A.1:2:3 B.3:2:1 C.6:3:1 D.6:3:2
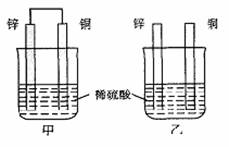
(上海.06)13.将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大 D.产生气泡的速度甲比乙慢
1.下列叙述中不正确的是(双选) ( )
A. 电解池中与电源正极相连的是电解池的阴极
B. 电解池的阳极发生氧化反应,阴极发生还原反应
C. 电解池中电子从电源的负极沿导线流入电解池的阴极
D. 电解池是把化学能转变为电能的装置
2.在原电池和电解池的电极上所发生的反应,同属氧化反应或同属还原反应的是(双选)( )
A. 原电池的正极和电解池的阳极所发生的反应
B. 原电池的正极和电解池的阴极所发生的反应
C. 原电池的负极和电解池的阳极所发生的反应
D. 原电池的负极和电解池的阴极所发生的反应
3.下列实验现象的描述不正确的是(双选) ( )
A. 把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B. 把石墨作电极电解硫酸铜溶液,阳极质量增加
C. 把铜片插入浓氯化铁溶液中,在铜片表面出现一层铁
D. 把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
4.下列关于铜电极的叙述正确的是(双选) ( )
A. 铜锌原电池中铜是正极
B. 用电解法精炼粗铜时粗铜作阴极
C. 在镀件上电镀铜时可用铜作阳极
D. 电解稀硫酸指H2、O2时铜作阳极
5.将质量分数为0.052(5.2%)的NaOH溶液1L(密度为1.6g/cm3)用铂电极电解,当溶液中NaOH的质量分数改变了0.010(1.0%)时停止电解,则此时溶液中符合的关系是 ( )
| 编号 | NaOH的质量分数 | 阳极析出物的质量/g | 阴极析出物的质量/g |
| A | 0.062(6.2%) | 19 | 152 |
| B | 0.062(6.2%) | 152 | 19 |
| C | 0.042(4.2%) | 12 | 94 |
| D | 0.042(4.2%) | 94 | 12 |
6.用惰性电极实现电解,下列说法正确的是 ( )
A. 电解稀硫酸溶液,实际上是电解水,故溶液pH不变
B. 电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小
C. 电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1:2
D. 电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:1
7.用石墨作电极,电解1mol/L下列物质的溶液,溶液的PH值保持不变的是 ( )
A.HCl B.NaOH C.Na2SO4 D.NaCl
8.图中X、Y分别是直流电源的两极,通电后发现a极板质量增加,b 极板有无色无嗅气体放出,符合这一情况的是 ( )
| 编号 | a极板 | b极板 | X电极 | Y电极 |
| A | 锌 | 石墨 | 负极 | CuSO4 |
| B | 石墨 | 石墨 | 负极 | NaOH |
| C | 银 | 铁 | 正极 | AgNO3 |
| D | 铜 | 石墨 | 负极 | CuCl2 |
9.用惰性电极电解一定浓度的下列物质的溶液,一段时间后向余下的溶液中加入适量物质(括号中列出),能使溶液与电解前相同的是 ( )
A.CuCl2(水) B.H2SO4(水) C.CuSO4(氢氧化铜) D.NaCl(盐酸)
10.电解水时需加入一些电解质以增强导电性,下列电解质中不适宜加入的是 ( )
A.KNO3 B.KCl C.H2SO4 D.KOH
11.在外界提供相同电量的条件,Cu2+或Ag+分别按Cu2++2e→Cu或Ag++e→Ag在电极上放电,若析出铜的质量为1.92g,则析出银的质量为 ( )
A.1.62g B.6.48g C.3.24g D.12.96g
12.用惰性电极电解X(NO3)n溶液,若阳极上生成560ml气体(标况),则阴极上析出金属m g,则金属X的相对原子质量为 ( )
A.mn B.m/n C.20mn D.10mn
13.将两个铂电极插入500ml CuSO4溶液中,进行电解。通电一定时间后,某一电极增重0.064g(设电解时该电极无氢气析出,且不考虑水解和溶液的体积变化),此时溶液中氢离子浓度约为( )
A.4×10-3 mol/L B.2×10-3 mol/L C.1×10-3 mol/L D.1×10-7 mol/L
14.用两支惰性电极插入500mlAgNO3溶液中,通电电解。当电解液的pH从6.0变为3.0时(设电解时阳极没有氢气放出,且电解液在电解前后体积变化可以忽略),电极上应析出银的质量是( )
A.27mg B.54mg C.108mg D.216mg
15.氢镍电池是近年开发出来的可充电电池,它可以取代会产生污染的铜镍电池。氢镍电池的总反应式是: H2 + 2 NiO(OH)2 ![]() 2Ni(OH)2
根据此反应式,判断下列叙述正确的是 ( )
2Ni(OH)2
根据此反应式,判断下列叙述正确的是 ( )
A.电池放电时,电池负极周围溶液的OHˉ不断增大
B.电池放电时,镍元素被氧化
C.电池充电时,氢元素被还原
D.电池放电时,氢气是负极
16.指出下列装置:原电池是 ,电解池是 ,电镀池是
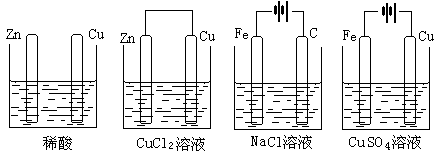
A B C D
17.从H+、Na+、Ba2+、Cu2+、Cl-、SO42-等离子中选择恰当离子组成电解质,按下列要求进行电解:
(1)以碳棒为电极,使电解质含量减少,水量不变,则选出的电解质的化学式为
(2)以碳棒为电极,使电解质溶液浓度增加,但加水后又可恢复原浓度,则选出的电解质的化学式为
(3)以碳棒为阳极,铁为阴极,使电解质和水的量都减少,则选出的电解质的化学式为
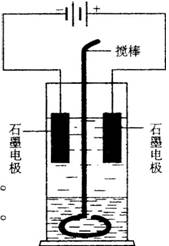 (04.全国)28.(14分)
(04.全国)28.(14分)
在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如右图。接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。根据上述实验回答:
(1)阳极上的电极反应式为_____________________。
(2)阴极上的电极反应式为_____________________。
(3)原上层液体是_____________________________。
(4)原下层液体是______________________________。
(5)搅拌后两层液体颜色发生变化的原因是________
。
(6)要检验上层液体中含有的金属离子,其方法是_____________________________,
现象是_____________________________________________________________
_____________________________________________________________________。
答案:
一、
1.(1)负 正
(2)阳 阴
(3)化学 电 电 化学 氧化还原
2.负 阴 还原 阳 失 氧化
3.惰性 失 活性
4.阳 阴 电镀 不变
二、
高考试题:
A D C
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| AD | BC | BC | AC | B | D | C | A | B | B | B | D | A | B | CD |
16.B CD D
17.(1)HCl、CuCl2 (2)Na2SO4、H2SO4 (3)NaCl、CuSO4、BaCl2
![]()
![]() 28.(1)2
28.(1)2![]() I2 (2)2
I2 (2)2![]() H2↑(3)KI(或NaI等)水溶液
H2↑(3)KI(或NaI等)水溶液
(4)CCl4(或CHCl3等)
(5)I2在CCl4中的溶解度大于在水中溶解度,所以绝大部分I2都转移到CCl4中
(6)焰色反应 透过蓝色钴玻璃观察火焰呈紫色(其它合理答案同样给分。例如,若③中答NaI水溶液,这里答火焰呈黄色。)