理科综合能力测试[化学部分](七)
第Ⅰ卷
(选择题,每小题6分,共48分)
在下列各题的四个选项中,只有一个选项是符合题目要求的。
以下数据可供解题时参考:
原子量:H 1,C 12,O 16,Cu 64
1.下列叙述正确的是
A.同主族金属的原子半径越大熔点越高
B.稀有气体原子序数越大沸点越高
C.同周期元素的原子半径越小越易失去电子
D.在晶体中只要有阳离子就一定有阴离子
2.
pH=4的FeCl3溶液和pH=10的K2CO3溶液中,水的电离度分别为![]() 和
和![]() ,则它们的大小关系是
,则它们的大小关系是
A.![]() <
<![]() B.
B.![]() >
>![]() C.
C.
![]() =
=![]() D.无法判断
D.无法判断
3.常温下,将甲酸和氢氧化钠溶液混合,所得溶液pH=7,则此溶液中
A.[HCOO— ]>[Na+] B.[HCOO— ]<[Na+]
C.[HCOO— ]=[Na+] D.无法确定[HCOO— ]与[Na+]的关系
4.某无色透明溶液中,由水电离出来的[H+]=1×10—11 mol·L—1,该溶液中一定能大量共存离子组是
A.K+、Na+、MnO4—、NO3— B.K+、Na+、Cl—、NO3—
C.NH4+、AlO2—、Na+、CH3COO— D.Fe3+、S2—、Al3+、HCO3—
5.1,2,3—三苯基环丙烷的三个苯基可以分布在环丙烷环平面的上下,因此有如下2个异构体(![]() 是苯基,环用键线表示,C、H原子都未画出)
是苯基,环用键线表示,C、H原子都未画出)
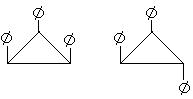
据此,可判断1,2,3,4,5—五氯环戊烷(假定五个碳原子也处于同一个平面上)的异构体数是
A.3 B.4 C.5 D.6
6.
在一定条件下,可逆反应X(g)+3Y(g)![]() 2Z(g)
达到平衡时,测得X的转化率为25%,Y的转化率为37.5%,则反应开始时,充入容器中的X与Y的物质的量之比是
2Z(g)
达到平衡时,测得X的转化率为25%,Y的转化率为37.5%,则反应开始时,充入容器中的X与Y的物质的量之比是
A.1:3 B.3:1 C.3:2 D.1:2
7.已知1个N2O3分子的质量为a g,1个N2O5分子的质量为b g。若以16O原子质量的![]() 作为相对原子质量的标准,则NO2的相对分子质量为
作为相对原子质量的标准,则NO2的相对分子质量为
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
8.将32 g CuO热到900℃,CuO部分分解为Cu2O,最后固体质量为31.2 g。则未分解的CuO与分解的CuO的物质的量之比为
A.2:1 B.1:2 C.1:3 D.3:1
第Ⅱ卷
(非选择题,共3小题,共50分)
9.(20分)醛在一定条件下可以两分子加成:
![]()
加成产物不稳定,受热即脱水而生成不饱和醛:
![]()
卤代烃在氢氧化钠醇溶液中加热可生成不饱和化合物:
CH3CH2CH2Cl+NaOH![]() CH3CH=CH2 + HCl
CH3CH=CH2 + HCl
已知物质B是一种可作为药物的芳香族化合物,请根据下图(所有无机产物已略去)中各有机物的转化关系回答问题:
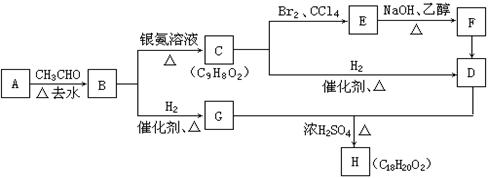
(1)(6分)写出B、F的结构简式
B:__________________________ F:_________________________
(2)(4分)图中涉及的有机反应类型有以下的(填写序号)________________
①取代反应 ②加成反应 ③氧化反应 ④还原反应
⑤消去反应 ⑥聚合反应 ⑦酯化反应 ⑧水解反应
(3)(4分)写出G与D反应生成H的化学方程式
_________________________________________________________________
(4)(4分)F若与H2发生加反应,1 mol F最多消耗的H2的物质的量为_________mol。
10.(10分)水在自然界有“自净化”功能,其净化过程是将水中的有机污染物自发地转变为简单的无机物,但需水中有一定的氧气,才能使转化过程完成:
有机物+O2→CO2+H2O
1 L水中含有的有机物转化为无机物所需要的氧气量,叫做“生化需氧量”,用BOD表示,单位为g·L—1。若水中含氧气的量比BOD少,水质就变坏、发臭,水生动植物则不能生存。
某河水中含有机物A(A的组成用C6H10O5表示,设河水的密度为1.00 g·㎝—3。)
(1)(3分)假设该河水能自动净化,其净化过程可用化学方程式表示为:
______________________________________________________________
(2)(7分)在正常情况下,氧气在水中溶解量为0.00920 g·L—1,若该河水中水生动植物能生存,则河水中含有机物A的质量分数不超过百万分之____________________。
11.(20分)自然界存在的碳酸盐类铜矿(如孔雀石、石青等)的化学组成为:
aCuCO3·bCu(OH)2(a,b为正整数,且a≤2,b≤2)
(1)将孔雀石、石青矿样分别加盐酸至完全溶解,耗用HCl物质的量与产生CO2物质的量之比:孔雀石为4︰1;石青为3︰1。则它们的化学组成为孔雀石:____________,石青:_________________。
(2)今有一份碳酸盐类铜矿样品,将其等分为A、B两份。然后,加盐酸使A样品完全溶解,产生CO2 3.36 L(标准状况);加热B样品使其完全分解,得到20 g CuO。试计算并确定该矿石的化学组成。
______________________________________________________
(3)某碳酸盐类铜矿样加酸完全溶解后,产生CO2 6.72 L(标准状况),这份矿样中CuO含量不低于_____________g。
(4)设某碳酸盐类铜矿的质量为A g,所含CuO质量为G g。加酸完全溶解后,产生CO2体积(标准状况)为V L,则含铜矿样的A、V、G之间的关系式为:
A=______________________________________。
理科综合能力测试(化学部分)参考答案及评分标准
Ⅰ卷 每小题6分,共48分
1.B 2.C 3.C 4.B 5.B 6.D 7.C 8.D
Ⅱ卷 包括3小题,共50分
9.(20分)
(1)
![]() (每空4分,共8分)
(每空4分,共8分)
(2)①②③④⑤⑦ (4分)
(3)
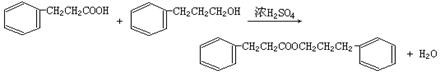 (4分)
(4分)
(4)5 (4分)
10.(10分)
(1)C6H10O5+6O2→6CO2+5H2O (3分)
(2)7.76 (7分)
11.(20分)
(1)CuCO3·Cu(OH)2;2CuCO3·Cu(OH)2 (每空3分,共6分)
(2)a︰b=3︰2,该矿样的化学组成为CuCO3·Cu(OH)2与2CuCO3·Cu(OH)2的混合物。 (4分)
(3)36 g (5分)
(4)![]() (5分)
(5分)