理科综合能力测试[化学部分](九)
第Ⅰ卷
(选择题,每小题6分,共48分)
在下列各题的四个选项中,只有一个选项是符合题目要求的。
以下数据可供解题时参考:
原子量:H 1,C 12,O 16,S 32,Ca 40,Fe 56,Cu 64
1.甲、乙是周期表中同一主族的两种元素,若甲的原子序数为x,则乙的原子序数不可能是
A.x+2 B.x+4 C.x+8 D.x+18
2.下列说法中正确的是
A.原子及其离子的核外电子层数等于该元素所在的周期数
B.稀有气体原子的最外层电子数都有是8
C.元素周期表中从ⅢB族到ⅡB族10个纵行的元素都有是金属
D.同一元素的各种同位素的物理性质、化学性质均相同
3. 某温度下,100 g饱和氯化钠溶液中含有氯化钠26.5 g。若向此溶液中添加3.5 g氯化钠和6.5 g水,则所得溶液的质量分数是
A.30% B.![]()
C.26.5%
D.![]()
4.将pH=1的盐酸平均分成2份,1份加适量水,别1份加入与该盐酸物质的量浓度相同的适量NaOH溶液后,pH都升高了1,则加入的水与NaOH溶液的体积比为
A.9 B.10 C.11 D.12
5.常温下,向20 L真空容器内通入a mol H2S气体和b mol SO2气体(a和b都是正整数,且a≤5,b≤5)。反应完全后,容器内气体可能达到的最大密度约是
A. 24.5 g・L―1 B.14.4 g・L―1
 C. 8 g・L―1
D.5.1 g・L―1
C. 8 g・L―1
D.5.1 g・L―1
6.用于制造隐形飞机的某种物质具有吸收微波的功能,其主要成分的结构如图,它属于
A.芳香族化合物 B.高分子化合物
C.无机化合物 D.有机化合物
7.用足量的CO还原32.0 g某种氧化物,将生成的气体通入足量澄清石灰水中,得到60 g沉淀,则该氧化物是
A.FeO B.Fe2O3 C.CuO D.Cu2O
8.下列反应的离子方程式书写正确的是
A.向氢氧化钠溶液中通入少量CO2 OH―+CO2=HCO3―
B.用氨水吸收少量SO2 2NH3・H2O+SO2=2NH4++SO32―+H2O
C.硝酸铝溶液中加入过量氨水 Al3++4NH3・H2O=AlO2―+4NH4++2H2O
D.向硫酸铁的酸性溶液中通入足量H2S Fe3++H2S=Fe2++S↓+2H+
第Ⅱ卷
(非选择题,共3小题,共50分)
9.(16分)人体缺碘会影响正常的生命活动,为提高人体素质,食物补碘已引起人们的重视,人从食物中摄取碘后碘便在甲状腺中积存,在甲状腺内,通过有关反应形成甲状腺素,甲状腺素的合成过程可表示为:
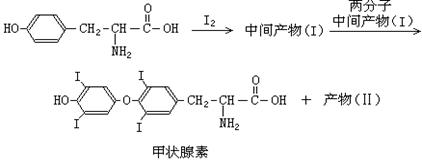
请填写下列空白:
(1)甲状腺素的分子式为__________________________。
(2)中间产物(I)的结构简式为__________________________。
(3)产物(II)的名称为_________________________________。
(4)甲状腺素在物质的分类是从不同角度考虑可以属于____________(填标号)。
A.酚 B.氨基酸 C.卤代烃 D.芳香烃
10.(16分)
①A、B、C、D四种物质均含元素X,有的还含有元素Y、Z,元素Y、X、Z的原子序数递增。
②X在A、B、C、D中都不呈现它的最高化合价。
③室温下单质A与某种常见的一元强碱溶液反应,可得到B和C。
④化合物D受热催化分解,可制得元素Y的单质。
(1)元素X是___________,Z是____________。
(2)写出③中反应的化学方程式:
______________________________________________________。
(3)写出④中反应的化学方程式:
______________________________________________________。
11.(18分)本题要求写出必要的文字说明、方程式和重要的解步聚,只写出最后答案的不得分。有数值计算的题,答案中必须明确写出数值和单位。
在一支10 mL试管中充满NO2和O2,将其倒立在盛有足量水的水槽中,若以y mL表示完全反应后试管内剩余气体的体积,x mL表示原混合气体中NO2的体积:
(1)试建立![]() 的关系式(讨论x在不同值时,反应后气体的体积y)。
的关系式(讨论x在不同值时,反应后气体的体积y)。
(2)在下图坐标中作出![]() 的曲线。
的曲线。

理科综合能力测试(化学部分)参考答案及评分标准
Ⅰ卷 每小题6分,共48分
1.B 2.C 3.C 4.C 5.B 6.D 7.B 8.B
Ⅱ卷 包括3小题,共50分
9.(16分)
(1)C15H11NO4I4 (4分)
(2)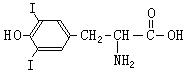 (4分)
(4分)
(3)丙氨酸(或α―氨基酸) (4分)
(4)A、B、C (4分)
10.(16分)
(1)Cl(或氯),K(或钾) (每空3分,共6分)
(2)Cl2+2KOH=KCl+KClO+H2O (5分)
(3)2KClO3
![]() 2KCl+3O2↑
(5分)
2KCl+3O2↑
(5分)
11.(18分)
解:NO2与O2体积比为4:1时恰好完全反应生成HNO3
4NO2+O2 +2H2O=4HNO3 (2分)
设NO2体积为x,讨论如下:
(1)当O2过量,0<x≤8时,用NO2的体积来计算
![]()
![]() 则
则![]() (3分)
(3分)
当NO2过量,8≤x<10 时,O2与NO2完全反应且过量的NO2又与水反应,所以
![]()
![]() (3分)
(3分)
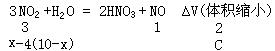
![]() (3分)
(3分)
则![]() (3分)
(3分)
(2)坐标曲线如图(4分)
