河北石家庄高三理综模拟(一)
说明:本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共300分。考试时间150分钟。
第Ⅰ卷(选择题 共132分)
本卷共22题,每题6分,共132分。在下列各题给出的四个选项中,只有一个选项是符合题意的。
可能用到的原子量:
H 1 C 12 N 14 O 16 Mg 24 Al 27 Si 28 S 32 Ca 40 Fe 56
1.下列哪组最可能是线粒体的组成元素
A.C、H、O、N、P B.C、H、O、N
C.C、H、O、S、P D.C、H、O、S
2.下图是人体糖代谢的部分过程,图解存在的错误是
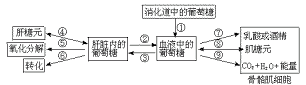
A.③④ B.⑤⑥ C.⑦⑧ D.⑧⑨
3.下图为某种生物体有性生殖过程中有关细胞的分裂图象。下列说法错误的是
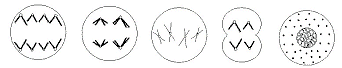
| ||||||||||
| ||||||||||
|
|
| ||||||||
①雄性动物体内,同时具有图甲~戊所示细胞的器官是睾丸而不可能是肝脏 ②基因重组的发生与图甲有关而与图丙无直接关系 ③图乙所示分裂方式,其间期突变产生的新基因传给后代的可能性要大于图丙 ④中心法则表示的生命活动主要发生在图乙和图戊
A.①② B.①③ C.②③ D.②④
4.基因A、B、C分别控制酶Ⅰ、酶Ⅱ、酶Ⅲ的产生,这三种酶共同作用可将一原本无色的物质转变为黑色素,即无色黑色素。若两亲本基因型均为AaBbCc,则子代中能正常合成黑色素个体的几率是![]()
A.1/64 B.3/64 C.9/64 D.27/64
5.在一个封闭的池塘中,水体受大量生活污水的污染,出现富营养化。其水中含氧量变化曲线可能是(纵轴表示溶解氧含量,横轴表示时间)
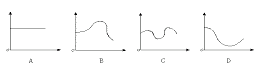
6.下列化学式既表示物质的组成,又表示物质分子式的是
A.SiO2 B.CH4O C.NH4Cl D.P
7.pH=5的硫酸稀释500倍,稀释后SO2-4与H+浓度之比最接近于
A.1∶1 B.1∶2 C.1∶10 D.10∶1
8.下列叙述正确的是
(1)离子化合物中不一定含有金属阳离子
(2)分子晶体中不一定含有共价键
(3)有机物中不一定都含有氢元素
(4)酸酐都能直接与水反应生成相应酸
(5)酸与碱混合只发生中和反应
(6)酸式盐溶于水得到的溶液都呈现酸性
A.只有(1)(2)
B.只有(1)(2)(3)
C.只有(3)(5)(6)
D.只有(1)(2)(4)(6)
9.在给定条件下,下列加点的物质在化学反应中能被完全消耗的是
A.用浓盐酸与二氧化锰共热制取氯气
B.标准状况下,将1g铝片投入20 mL 18mol·L-1的硫酸中
C.向100 mL 3mol·L-1的硝酸中加入5.6 g铁
D.在5×107 Pa、500℃和铁触媒催化的条件下,用氮气和氢气合成氨
10.右图是元素周期表前六周期的一部分,关于元素X、Y、Z的叙述正确的是
①X的气态氢化物与Y最高价氧化物对应的水化物能发生反应生成盐
 ②Y原子半径比氧原子或氯原子都大
②Y原子半径比氧原子或氯原子都大
③Z的单质常温下可与铁粉反应
④Z的原子序数比Y大19
⑤Z所在的周期中含有32种元素
A.只有②
B.只有①④
C.只有①②③④
D.①②③④⑤
11.下列关系不正确的是
A.离子半径:Cl->F+>Na+>Al3+
B.熔点:石英>食盐>钾>干冰
C.结合质子的能力:CO2-3>HCO-3>SO2-4
D.热稳定性:PH3>H2S>HBr>NH3
12.不用焰色反应,也不用其他试剂,限用化学方法区分下列溶液,可行的有
A.KNO3、K2SO4、HCl、K2CO3
B.NaNO3、KCl、HCl、KOH
C.KOH、MgSO4、KHSO4、K2CO3
D.MgCl2、BaCl2、Na2SO4、KNO3
13.某有机物的结构简式如下,关于它性质的叙述正确的是
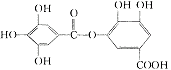
A.酸性条件下可以发生水解反应,且产物只有一种
B.1 mol该有机物与足量氢氧化钠溶液共热,最多消耗7 mol NaOH
C.1 mol该有机物最多能和含2 mol溴的溴水反应
D.该有机物与新制氢氧化铜或高锰酸钾酸性溶液都不能反应
14.为了探究金属腐蚀的条件和快慢,某课外学习小组用不同的细金属丝将三根大小相同的普通铁钉分别固定在下图所示的三个装置内,并将这些装置在相同的环境中放置相同的一段时间,下列对实验结果的描述不正确的是
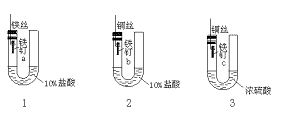
A.实验结束时,装置1左侧的液面一定会下降
B.实验结束时,装置1一定比装置2左侧的液面低
C.实验结束时,铁钉b腐蚀最严重
D.实验结束时,铁钉c几乎没有被腐蚀
15.下列说法中正确的是
A.布朗运动实验中看到的小颗粒的运动就是液体分子的无规则运动
B.只要温度相同,任何物体分子运动的平均速率都相等
C.当物体的温度升高时,分子的平均动能增大
D.当物体的机械能发生变化时,内能一定发生变化
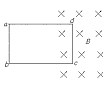 16.如图所示,矩形线圈abcd的一部分在匀强磁场内,水平磁场B的方向与线圈平面垂直,磁场的边界与ab边平行,在线圈运动的过程中bc边受到的安培力方向竖直向下,则线圈的运动情况是
16.如图所示,矩形线圈abcd的一部分在匀强磁场内,水平磁场B的方向与线圈平面垂直,磁场的边界与ab边平行,在线圈运动的过程中bc边受到的安培力方向竖直向下,则线圈的运动情况是
A.向左平动
B.向右平动
C.向上平动
D.向下平动
17.将两节相同的电池分别以串联或并联两种方式与同一个外电阻R相连接,组成闭合电路,每节电池的电动势为E、内阻为r,并且r=R。当电池串联时,电路的路端电压为U1,通过电阻的电流为I1;当电池并联时,电路的路端电压为U2,通过电阻的电流为I2,则下列关系正确的是(提示:两节相同电池并联使用时,总电动势等于每节电池的电动势,总电阻的计算与并联电阻的计算方法相同)
A.U1>U2 I1>I2
B.U1=U2 I1=I2
C.U1>U2 I1<I2
D.U1<U2 I1=I2
18.如图所示,是一列简谐横波在某时刻的波形图象。已知波沿着x轴的负方向传播, 波的频率为2.5 Hz,a为介质中某一质点,下列判断正确的是
波的频率为2.5 Hz,a为介质中某一质点,下列判断正确的是
A.经过0.1 s,a点的位移为正的最大值
B.经过0.1 s,a点移动到b点
C.经过0.2 s,a点的振动方向向上
D.经过0.2 s,a点的速度最小
19.如图所示,实线表示在竖直平面内匀强电场的电场线,电场线与水平方向成α角,水平方向的匀强磁场与电场正交,有一带电液滴沿斜向上的虚线l做直线运动,l与水平方向成β角,且α>β,则下列说法中错误的是
A.液滴一定做匀速直线运动
 B.液滴一定带正电
B.液滴一定带正电
C.电场线方向一定斜向上
D.液滴有可能做匀变速直线运动
20.如图所示,输入电压UAB=200 V,变阻器R1标有
“150 Ω、3 A”字样,负载电阻R2标有“50 Ω、2 A”字样,在电路允许的情况下,则输出电压Uab
A.最大值为200 V,最小值为0
B.最大值为100 V,最小值为0
C.最大值为200 V,最小值为75 V
D.最大值为100 V,最小值为75 V
21.如图所示,R1为定值电阻,R2为滑动变电阻器,电源E内阻不计。现有如下判断
①当R2为定值时,电压表V1的示数与电流表A的示数之比为R1
②当R2为定值时,电压表V2的示数与电流表A的示数之比为 R1
③当R2的阻值发生变化时,电压表V2示数变化的数值与电流表A示数变化的数值之比为R1
④当R2的阻值发生变化时,电压表V1示数变化的数值与电流表A示数变化的数值之比为R1
以上判断全部正确的组合是
A.①④ B.②③ C.①③④ D.②③④
22.如图甲所示,abcd为导体做成的框架,其平面与水平面成θ角。质量为m的导体棒PQ与ad、bc接触良好,回路的总电阻为R。整个装置放在垂直于框架平面的变化磁场中,磁场的磁感应强度B随时间t变化情况如图乙所示(设图甲中B的方向为正方向)。若PQ始终静止,关于PQ与框架间的摩擦力在 0~t1时间内的变化情况,有如下判断

|
|
①一直增大
②一直减小
③先减小后增大
④先增大后减小
以上对摩擦力变化情况的判断可能的是
A.①④ B.①③ C.②③ D.②④
第Ⅱ卷(非选择题 共168分)
23.(16分)某中学老师想利用烟草内某些化学物质能引起细胞的染色体变异的原理,组织课外小组同学进行实验和观察,以说明吸烟有害健康。
实验材料和用具:蚕豆干种子10粒(蚕豆染色体数为12,蚕豆根尖在常温条件下,一个细胞周期所占时间约为19.8小时),并准备了烟草浸出液(烟丝在蒸馏水中浸泡后提取)、蒸馏水、培养器、剪刀、镊子、清水、盐酸、染液、显微镜、载玻片等。请就实验课前准备和实验中的一些问题作答:
(1)第一步:种子萌发。将10粒蚕豆种子放在盛有蒸馏水的培养器中,并不使蒸馏水浸没种子。这样处理的原因是____________________________。种子萌发时吸水的主要方式是____________________________。
(2)第二步:培养生根。甲同学将上述已生根的10粒种子的根部浸泡在烟草浸出液中放在适宜条件下10小时后,切取根尖制成装片观察。
请针对该同学实验方法的不妥之处,写出你的设计思路:
①____________________________;
②____________________________。
为了得到更多的侧根,应切去主根。采取该措施的原理是_______________________。
(3)第三步:制作临时装片。乙同学的制作步骤是:取材→解离→染色→制片。请纠正该同学实验中的不正确操作步骤____________________________。
(4)预测同学们在显微镜下观察时,可能观察到的染色体变异类型有____________________________。要清晰观察染色体是否变异,最好寻找处于________期的细胞进行观察。
24.(8分)舞毒蛾的幼虫具有鲜艳的色彩和斑纹,且全身长满毒毛,如果被鸟类吞食,这些毒毛就会刺伤鸟的口腔黏膜。尝过这种苦头的鸟,再见到这种幼虫后,会迅速避开。请分析回答下列问题:
(1)从生命活动调节方式的角度来看,舞毒蛾幼虫所具有的色彩和斑纹是引起食虫鸟避开的条件刺激,而食虫鸟再次见到这种幼虫时便迅速避开的现象称为____________________________。
(2)从遗传和变异的角度来看,舞毒蛾幼虫的鲜艳色彩的斑纹是由________________________控制的,这种物质主要存在于____________________________上。
(3)从生物进化的角度来看,舞毒蛾幼虫的这种鲜艳色彩和斑纹是经过长期的____________________________形成的。这一过程是通过____________________________来实现的。
(4)从生物与环境关系的角度来看,舞毒蛾幼虫这种鲜艳的色彩和斑纹是对环境的一种____________________________。其意义是对敌害起____________________________作用,对其本身具有____________________________作用。
25.(22分)西气东输使天然气在化工生产中的用途越来越广泛。有人预计,“可燃冰”(主要成分也是甲烷)在若干年后有可能代替石油和煤成为有机化工中碳原子的主要来源。下面是天然气综合利用的一个实例:
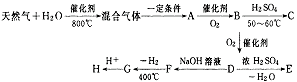
其中,F是一种有机酸的钠盐,将F与银氨溶液混合后水浴加热有银镜产生;1 mol G是2 mol F脱去1 mol氢气的缩合产物;一个C分子是由三个B分子通过加成反应生成的六元环状分子;E是常见的有毒气体。
(1)物质A的官能团是________基,这种官能团的电子式是________________。
(2)写出下列物质的结构简式
C____________________________G____________________________。
(3)写出D→F的离子方程式____________________________。
(4)写出H与足量的A发生反应的化学方程式
____________________________。
配制一定物质的量浓度的溶液是中学化学的基础实验,下面两题是实验过程中的一些问题:
26.(6分)为配制氢氧化钠溶液,需要先称量小烧杯的质量(称量结果是31.2 g)。实验中与天平配套的砝码规格如下表,请用“↑”表示向托盘上添加砝码,用“↓”表示又从托盘上取下该砝码,把称量过程中各个砝码的最合理的使用情况填在下表中的空格内
| 砝码的规格(g) | 50 | 20 | 20 | 10 | 5 |
| 使用的顺序 (用1、2、3……表示) | |||||
| 砝码的添加和取下情况 (用↑、↓表示) |
27.(14分)若配制500 mL 0.20 mol·L-1)的稀硫酸:
(1)需要使用质量分数0.98的硫酸(密度为1.84 g·mL-1)________mL。
(2)下面是某学生的操作过程:
a.检查容量瓶是否漏水 b.用100 mL的量筒量取浓硫酸 c.将浓硫酸倒入另一个盛有适量蒸馏水的量筒中稀释,并冷却到常温 d.用玻璃棒引流,将稀释后的硫酸倒入500 mL的容量瓶 e.轻轻摇动容量瓶,使瓶内液体混合均匀,再向容量瓶中加水至离刻度线1~2 cm f.用胶头滴管加水至凹液面底部与刻度线相切,摇匀 g.在容量瓶上贴上标签待用。
按照通常的配制要求,指出其中缺少或错误的操作,并补充或改正(有几项填几项,若空格不够可以补加)
①_____________ ②_____________
③_____________ ④_____________
⑤_____________ ⑥_____________
(3)任何实验都有误差,在你改正后的操作中,产生误差的原因还有
____________________________。
(4)本实验最浪费时间的步骤是将稀释后的硫酸冷却到室温,为了节约时间,简便易行的加快稀硫酸冷却的方法是
____________________________。
28.(17分)风力发电作为一种无污染、低成本的电力产业,发展前景广阔。我国风力资源丰富,到2000年底,我国风力发电机的总装机容量已达264万千瓦。风力发电的原理是利用风推动叶轮转动,将风的动能转化为叶轮的动能,再将叶轮的动能转化为电能。
(1)设空气的密度为ρ,叶轮每个车叶的长度均为L,正对叶轮的水平风速为v,整个发电机的效率为η,那么每台发电机发出的电功率P=________。
(2)我国研制Wd—646型风力发电机,每个车叶的长度L=22 m,当风速达到v=15 m/s时,其输出电功率可达P=600 kW。求该风力发电机将风的动能转化为电能的总效率η.(空气密度为ρ=1.29 kg/m3)
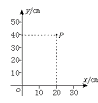 29.(17分)如图所示,在x>0的区域内存在着垂直于xOy平面的匀强磁场B,磁场的左边界为x=0,一个带电量为q=+1.0×10-17
C、质量为m=2.0×10-25
kg的粒子,沿着x轴的正方向从坐标原点O射入磁场,恰好经过磁场中的P点,P点的坐标如图所示。已知粒子的动能为Ek=1.0×10-13 J(不计粒子重力)。
29.(17分)如图所示,在x>0的区域内存在着垂直于xOy平面的匀强磁场B,磁场的左边界为x=0,一个带电量为q=+1.0×10-17
C、质量为m=2.0×10-25
kg的粒子,沿着x轴的正方向从坐标原点O射入磁场,恰好经过磁场中的P点,P点的坐标如图所示。已知粒子的动能为Ek=1.0×10-13 J(不计粒子重力)。
(1)在磁场中画出粒子的运动轨迹并标出磁场方向。
(2)求出匀强磁场的磁感应强度B。
(3)求出粒子在磁场中从O点运动到P点的时间t。
30.(12分)
Ⅰ.(6分)下图是几种与生物生命活动相关的能量的关系图解。请据图回答问题:
(1)图中A、F代表的生理过程依次为________和________。前者进行的场所是_____________。
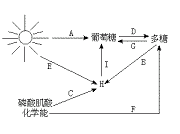
(2)图中H代表的物质是________。B代表的生理过程是_____________。
(3)从代谢类型来看,进行A或F生理过程的生物叫做________生物。
Ⅱ.(6分)上图中过程G也可以在实验室中用试管实验来完成。若在某试管中已放有0.5g淀粉,请你接着设计下面的实验以完成“淀粉→葡萄糖”的转化,并检验反应是否进行完全,完成下表:
| 转化实验所用试 剂及操作 | 反应的化学方程式 | 检验反应已完全 的试剂及现象 |
31.(35分)
Ⅰ.(17分)常用的电压表和电流表都是由小量程的电流表G(表头)改装而成。常用的表头主要由永磁铁和放入永磁铁磁场中的可转动的线圈组成。当线圈中有电流通过时,线圈在磁场力的作用下带着指针一起偏转。电流越大,指针偏转的角度越大,且指针偏转的角度与电流成正比,由指针在标有电流值的刻度盘上所指的位置,就可以读出通过表头的电流值。由欧姆定律可知,通过表头的电流跟加在表头两端的电压成正比。如果在刻度盘上标出电压值,由指针所指的位置就可以读出加在表头两端的电压值。
若已知某电流表G的内电阻Rg=100 Ω,满偏电流Ig=50 μA,现要求将该表头按如图甲所示的电路改装成一个量程I=100 mA、量程U=10 V的多用电表。
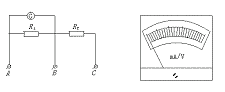
|
(1)当多用电表作为电流表使用时,应接________接线柱(填“A”“B”或“C”)。
当多用电表作为电压表使用时,应接________接线柱(填“A”“B”或“C”)。
(2)请你在图乙表盘上标出改装后多用电表6个长刻度线分别代表的值,并写出每一个小格所代表的值____________________________。
(3)电阻R1=________,R2=________。
Ⅱ.(18分)A、B、C、D、E、F是由短周期元素组成的六种微粒,每个微粒中都有10个电子。其中有两种是分子,四种是离子。已知A、E是由非金属元素构成的阳离子,这六种微粒有如下的相互关系:
a.A、B两种离子在加热条件下可以生成C、D两种分子
b.C是常温下呈气态的分子,遇到HCl会产生白烟
c.1 mol B离子与1 mol E离子相互作用可生成2 mol D分子
d.含有F微粒的溶液遇到B离子会产生白色沉淀W,B离子过量时W又溶解得到无色透明溶液。在此无色溶液中加入E时,又产生白色沉淀W,E过量时,W又转化为F。
(1)微粒A的电子式是________,微粒E的化学式是________,微粒C的空间构型是________。
(2)写出下列反应的离子方程式
A与B:____________________________。
F水解:____________________________。
F与过量的C的水溶液:____________________________。
(3)由物质的量相等的A离子和Cl-以及D分子组成的混合物呈________(填“酸”“碱”或“中”)性,其原因用离子方程式可表示为_____________。
(4)除了HCl外,请写出一种检验C的方法_____________。
32.(21分)如图甲所示是一种获得高能粒子的装置,环形区域内存在垂直于纸面向外、大小可以调节的匀强磁场。质量为m、电荷为+q的粒子在环中做半径为R的匀速圆周运动。图中A、B为两块中心开有小孔的极板(极板间距离远小于R),原来电势都为零,每当粒子飞经A板时,A板的电势升高为+U,B板的电势仍为零。粒子在两板间的电场中得到加速。每当粒子离开B板时,A板的电势又降为零。粒子在电场一次次的加速下动能不断增大,而绕行半径不变。设t=0时粒子在A板小孔处,由静止开始在电场力作用下加速并开始绕行,则
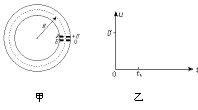
(1)粒子绕行n圈回到A板时的动能En=________。
(2)为使粒子始终保持在半径为R的圆轨道上运动,磁感应强度必须周期性递增,则粒子绕行第n圈时,所加磁场的磁感应强度Bn=________。
(3)求出粒子绕行前n圈所需的总时间tn。
(4)在乙图中画出A板的电势u与时间t的关系图象(图中t1是粒子第一次回到A板的时刻,要求定性画出从t=0起到粒子第四次离开B板为止的图象)。
高三理综模拟(一)答案
1.A 2.C 3.D 4.D 5.B 6.B 7.C 8.B 9.C 10.C 11.D 12.C 13.A 14.B 15.C 16.A 17.B 18.A 19.D 20.D 21.C 22.B
23.(16分,每空2分)
(1)种子萌发时需要充足的空气(氧气) 吸胀吸水 (2)①将蚕豆随机分为两组,每组5粒,分别放在盛有等量蒸馏水和烟草浸出液的培养器中②应培养19.8小时以上 打破顶端优势 (3)解离后应用清水充分漂洗根尖后再染色 (4)染色体结构变异和染色体数目变异 (有丝分裂)中
24.(8分,每空1分)
(1)条件反射 (2)基因(DNA) 染色体 (3)自然选择 生存斗争 (4)适应 预先示警 自我保护
![]() 25.(22分)
25.(22分)
(1)(6分)羟
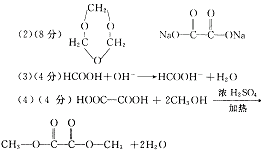
26.(6分)
| 砝码的规格(g) | 50 | 20 | 20 | 10 | 5 |
| 使用的顺序 (用1、2、3……表示) | 1 | 2 | 3 | 4 | 5 |
| 砝码的添加和取下情况 (用↑、↓表示) | ↑↓ | ↑ | ↑↓ | ↑ | ↑↓ |
| 砝码的规格(g) | 50 | 20 | 20 | 10 | 5 |
| 使用的顺序 (用1、2、3……表示) | 1 | 2 | 3 | 4 | |
| 砝码的添加和取下情况 (用↑、↓表示) | ↑ | ↑↓ | ↑ | ↑↓ |
27.(14分)
(1)(2分)5.4
(2)(每空2分)
①缺少洗涤烧杯和玻璃棒的操作
②量筒的规格错,应该用10 mL的量筒量取浓硫酸(或回答“用移液管、滴定管量取浓硫酸”)
③不应该在量筒中稀释浓硫酸,应该用烧杯
④不应该用容量瓶保存溶液,应该用细口瓶
(3)(2分)量筒的精确度不够高(或读数误差、溶质仍有少量残留在烧杯内、室温未必是20℃等)
(4)(2分)充分搅拌(冷水浴冷却盛有稀硫酸的烧杯、加冰块等即可)。
28.(17分)解:
(1)![]() πρηL2v3
(8分)
πρηL2v3
(8分)
(2)由(1)的结果可知
该风力发电机将风的动能转化为电能的效率
η=![]() (5分)
(5分)
=![]() (2分)
(2分)
=18%(2分)
 29.(17分)
29.(17分)
解:(1)如图所示(4分)
(2)由几何关系求出粒子在磁场中做匀速圆周运动的半径
r2=202+(40-r)2 (3分)
又因qvB=mv2/r (1分)
而Ek=![]() mv2
(1分)
mv2
(1分)
联立以上各式并代入数据得
B=![]() =8.0×10-2 T
(2分)
=8.0×10-2 T
(2分)
(3)由图可知 sinθ=15/25=3/5
故θ=37°(用反三角函数表示也可)(2分)
粒子在磁场中做匀速圆周运动,到P点时转动的圆心角为
φ=θ+90°=127° (1分)
粒子从O点运动到P点所用时间为(粒子运动周期T=![]() )
)
t=![]() T=
T=![]() ×
×![]() (2分)
(2分)
代入数据求出 t=5.54×10-7 s(1分)
(用反三角函数形式表达正确的也同样给分)
30.(12分)
Ⅰ.(6分)(每空1分)(1)光合作用 化能合成作用
叶绿体 (2)ATP(三磷酸腺苷) 呼吸作用 (3)自养型
Ⅱ.(6分)
| 转化实验所用试 剂及操作 | 反应的化学方程式 | 检验反应已完全 的试剂及现象 | ||
| 向该试管中加入稀 硫酸并加热一段时 间 | (C6H10O5)n+nH2O
| 碘水 溶液不变蓝色 |
31.(35分)
Ⅰ.(17分)
(1)A、B(3分) A、C(3分) (2)刻度标示略(3分) 4 mA(1分) 0.4 V(1分) (3)0.05 Ω(3分) 99.95 Ω(100 Ω,3分)
Ⅱ.(每空2分,共18分)
(1)(6分)
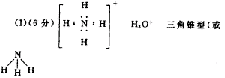
|
(2)(6分)NH+4+OH- ![]() NH3·H2O或NH+4+OH-
NH3·H2O或NH+4+OH- NH3↑+H2O
Al3++3H2O![]() Al(OH)3+3H+
Al(OH)3+3H+
Al3++3NH3·H2O Al(OH)3↓+3NH+4
(3)(4分)酸 NH+4+H2O![]() NH3·H2O+H+
NH3·H2O+H+
(4)(2分)C能使湿润的蓝色石蕊试纸变红
32.(21分)
解:(1)粒子每经过A、B两极板一次增加的动能为qU,所以粒子绕行n圈回到A板时的动能En=nqU. (4分)
(2)设粒子绕行n圈后的速度为vn,则有
nqU=![]() mvn2
①
mvn2
①
洛伦兹力充当向心力,有qvB=![]() ②
②
由以上两式得Bn=![]()
![]() ③(6分)
③(6分)
(3)设粒子绕行第一圈,第二圈……第n圈的周期分别为T1、T2、…Tn,则
T1=![]() ,T2=
,T2=![]() ,……Tn=
,……Tn=![]() ④(2分)
④(2分)
粒子绕行前n圈所用总时间tn=T1+T2+…+Tn ⑤(2分)
由③④⑤式得tn=πR![]() (1+
(1+![]() +
+![]() +…+
+…+![]() )
(3分)
)
(3分)
(4)如图所示

(4分)