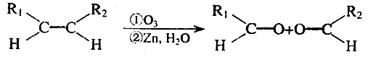������������5�¿��Ծ�
���Ծ���Ϊ�ڢ����ѡ���⣩�͵ڢ������ѡ���⣩�����֡���150�֣�����ʱ��120���ӡ�
��I����ѡ��������36�֣�
�������ݿɹ���ʱ�ο�
���ԭ��������H
һ��ѡ�������������13С�⣬ÿС��6�֣�ÿ��ֻ��һ��ѡ�������ĿҪ��
1����̬������ָ�����������������ذ�ij�����������������Ϣ�ͷ��ܵĵ�������Ⱥ����
���ֲ������ȶ���չ���������磬�Ͼ�����ԭ����ī���磬���ǰ����顢Խ�Ͻ�����
�����ϣ����ɴ���չ�����������ݵȵأ����ӳ�Ƭ����Ϊ���صġ����ݡ����Ͼ������ġ����֡�ʹ��Щ����������������������������������������
A�����ֶ��������ӡ��������������� B����̬ϵͳ��Ӫ���ṹ���ڸ���
C��ԭ�����ֵ������ܵ���в�������� D���Ŵ�����������
2�����������ػ���ı�������У�ϸ���ڰ��淢���ı仯�����������ͼ�е�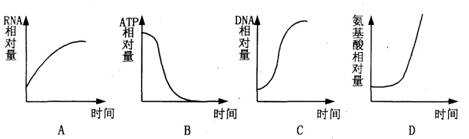
3������������������ɣ�ʹ���Ǹ��õ��о����������Ϊ������������йص������д������ ������ ��
A�������ϳ��ö����ڵ�ϸ����Ϊ����
B�������ȶ��ں��ʵ�����Ӫ�����ʣ���������ߴ�л����IJ���
C�����������ӳ����������ڣ��Ӷ���߲���
D�������ڵ�ϸ����л��Ծ�����������
4����������Ԥ����Ⱦ����������������ӵĵ���������һDNA���磬�������ɲ�ԭ���е�һ�α��ԭ�Ļ����Ƴɣ���λ������IJ�����������������߷�Ӧ�����¹���DNA����������в���ȷ���ǣ�
�� A��DNA���絼��������ܹ���������������
�� B�����������DNA����������ֱ�Ӳ������壬����������
C��DNA����Ľ��ֿ��ԴﵽԤ���ض������Ⱦ��Ŀ��
�� D��DNA������ֺ�������������Ŀ������ɽ�ϸ���ϳɵ�
5����Դ�ĺ���ʹ����ʹ��������ֲ�Ӱ����Դ�ij־����á���Ȼ��Ⱥ�����ʡ�S�������ߡ�����������Ⱥ�����ֵK��200��N��ʾ��Ⱥ����ˮƽ�������±��жϣ�������IJ����У�ʲô������Ⱥˮƽ���ܱ������IJ�����
| �����ϵĵ� | ��Ⱥ��С | (K��N)��K | ��Ⱥ�������� |
| Sl | 20 | 0��90 | 18 |
| S2 | 50 | 0��75 | 38 |
| S3 | 100 | 0��50 | 50 |
| S4 | 150 | 0��25 | 38 |
| S5 | 180 | 0��10 | 18 |
A��N��0��1Kʱ
B��N��0��5Kʱ
C��N��0��9Kʱ
D��N��Kʱ
6����NA��ʾ�����ӵ�������ֵ������˵����ȷ���ǣ������� ������������
�� A������ͭ��������������
�� B��ͨ��״���£���0.5mol HI�����0.5mol������Ϻ�����ķ�����ΪNA
C��
D��
7���������ؿ�����֧�������������Է�Ӧ,��ṹ��ʽ���¡����й����������ص�������ȷ���ǣ��� ��
����A�������ʵķ���ʽΪC9H16NO3
|
����C��1mol��������NaOH��Һ��Ӧ����������2mol NaOH
����D����������Ũ��ˮ���ܷ���ȡ����Ӧ�����ܷ����ӳɷ�Ӧ
8��������������ȷ���ǣ�������
������ ��п��ϡ���ᷴӦ����ȡ������������������ͭ��Һ�ܼӿ췴Ӧ����
������ �ڶƲ������������п�������������������������������ױ���ʴ
������ �۵��ʱ��Ӧ�Ѵ��Ƽ����ڵ��۵�����
������ ���õ�ⷨ������ͭʱ����ͭ����������ͭ������
������ �ݸ���������ʴʱ��������ӦʽΪ2H2O+O2��4e��=4OH��
������ A���٢ڢܡ������������� B���٢ۢܡ���������������C���٢ۢܢݡ�����������D���ڢܢ�
9����֪��Ӧ����Cl2+2KBr==2KCl+Br2������KClO3+6HCl==3Cl2��+KCl+3H2O��
��2KBrO3+Cl2==Br2+2KClO3������˵����ȷ���ǣ�������
������ A������������Ӧ���е������ɣ����Զ������û���Ӧ
������ B����Ӧ����1mol Cl2��Ӧʱ���������õ��ӵ����ʵ���Ϊ5mol
������ C����Ӧ����3mol Cl2���ɣ���ʽת�Ƶ��ӵ����ʵ���Ϊ6
10���ҹ�֧�֡����İ��ˡ���һ����Ҫ�����ǣ���������˶�Ա�����˷ܼ����˷ܼ��Ľṹ��ʽ��ͼ��ʾ���йظ����ʵ�˵����ȷ����
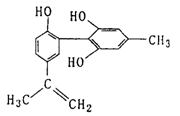 �� A����FeCl3��Һ����ɫ����Ϊ�������뱽������ͬϵ��
�� A����FeCl3��Һ����ɫ����Ϊ�������뱽������ͬϵ��
��
�� B������KMnO4(H��)��Һ���۲���ɫ��ȥ����֤����
���д���̼̼˫��
�� C��1mol�����ʷֱ���Ũ��ˮ��H2��Ӧʱ�������
Br2��H2�ֱ�Ϊ4mol��7mol
�� D���������ܷ���������Ӧ
11��
A��C(s)��![]() O2(g)
O2(g) ![]() CO(g)������H����393��
CO(g)������H����393��
����B��2H2 (g)��O2 (g) ![]() 2H2O(g)������H����571��6kJ��mol
2H2O(g)������H����571��6kJ��mol
����C��CH4(g)��2O2 (g) ![]() CO2 (g)��2H2O(g)������H����890��3kJ��mol
CO2 (g)��2H2O(g)������H����890��3kJ��mol
����D��![]() C6H12O6(s)��3O2
(g)
C6H12O6(s)��3O2
(g) ![]() 3CO2 (g)��3H2O(l)������H����1400kJ��mol
3CO2 (g)��3H2O(l)������H����1400kJ��mol
12. �����й�������ȷ���ǣ�������
����A. ![]() �Ĵ�������
�Ĵ�������![]()
B. 1mol�����Ƿ����к���![]()
C. ���![]() ������ת��
������ת��
D. һ�������½�2mol ![]() ��1mol
��1mol ![]() ��ϳ�ַ�Ӧ����
��ϳ�ַ�Ӧ����![]() ������ת��
������ת��
13. ��������ʵ�ֱ�ó��Ľ�����ȷ���ǣ�������
����A. ����������Ӧ�����Ȼ�����˵��������������ǿ
B. ����������̼������Һ��Ӧ����̼�����ƣ�˵�����ӵ����Ա�̼��ǿ
C. �ס������ֽ����õ������Ӳ���ϡ�����У�������ָʾ��Ϊ������˵�����Dz����ý���
D. ����![]() ��Һ��ͨ�����
��Һ��ͨ�����![]() ������
������![]() ���壬˵��
���壬˵��![]() ���ܽ��С��
���ܽ��С��![]()
����ѡ���⣨�������8С�⡣ÿС��������ĸ�ѡ���У��е�ֻ��һ��ѡ����ȷ���е��ж��ѡ����ȷ��ȫ��ѡ�Եĵ�6�֣�ѡ�Ե���ȫ�ĵ�3�֣���ѡ���ĵ�0�֣�
14���������ͬ������ʱ���Ƚ����Ƿ���������Բ�����Ȼ���죬ʹ������Բ������У�
����������Բ������е�Զ�ص�ʱ�ٴα�죬ʹ���ǽ���ͬ��Բ�����������ͬ��Բ��������Բ����Ƚϣ�����˵����ȷ���ǡ�����������������������������������������������������
������ A���ٶȱ�С�����ڱ䳤�����ٶȱ�С����������
������ B���ٶȱ�����ڱ�̣����ٶȱ����������
������ C���ٶȱ�С�����ڱ䳤�����ٶȱ�С�����ܼ�С
������ D���ٶȱ�����ڱ�̣����ٶȱ�����ܼ�С
|
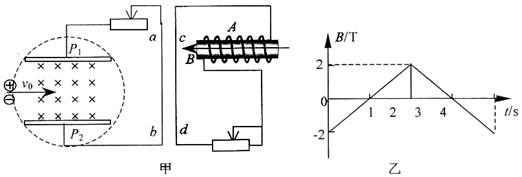
������ A��0~1s��ab��cd�������ų⡡���������� B��1~2s��ab��cd����������
������ C��2~3s��ab��cd���������������������� D��3~4s��ab��cd�������ų�
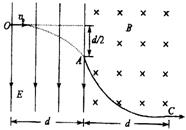
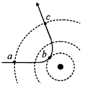 16�����ݦ�����ɢ��ʵ�飬¬ɪ�������ԭ�ӵĺ�ʽ�ṹģ�͡�ͼ�����߱�ʾԭ�Ӻ����γɵĵ糡�ĵ����ߣ�ʵ�߱�ʾһ�������ӵ��˶��켣���ڦ����Ӵ�a�˶���b�����˶���c�Ĺ����У�����˵����ȷ����(�� )
16�����ݦ�����ɢ��ʵ�飬¬ɪ�������ԭ�ӵĺ�ʽ�ṹģ�͡�ͼ�����߱�ʾԭ�Ӻ����γɵĵ糡�ĵ����ߣ�ʵ�߱�ʾһ�������ӵ��˶��켣���ڦ����Ӵ�a�˶���b�����˶���c�Ĺ����У�����˵����ȷ����(�� )
(A)�����������С������������������ (B)�������ȼ�С��������
(C)�糡�����������������������ܹ������㡡(D)���ٶ��ȱ�С������
17����ͼ����x����������һ�м�г�Შ��ijʱ�̵�ͼ����֪�ò��IJ���Ϊ
A������0.1s���ʵ�a���ʵ�b��λ��
B������0.2s���ʵ�a�Ķ��ܿ�ʼ�������ܿ�ʼ��С
C������0.02s���ʵ�a���ٶ�����ٶȷ�����ͬ
 D���ò�����һ��Ƶ��Ϊ10Hz�IJ�������������
D���ò�����һ��Ƶ��Ϊ10Hz�IJ�������������
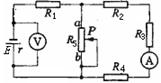
18����ͼ��ʾ��������ΪM������A��B��ֹ�ڹ⻬ˮƽ�����ϲ�������һ�𣨲�ճ������A��ab�������ķ�֮һ�⻬Բ����bc�����Ǵֲڵ�ˮƽ�档��������ΪmС���C������Ϊ�ʵ㣩��a�㾲ֹ�ͷţ����ոպ��ܵ���c�������A�ϻ��¡�������˵������ȷ���ǣ�������
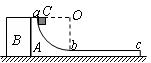 A��С���C��b��ʱ��A���ٶ����
A��С���C��b��ʱ��A���ٶ����
B��С���C��c��ʱ��A���ٶ����
C��С���C��b��ʱ��C���ٶ����
D��С���C��c��ʱ��A�����ʴ���B������
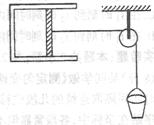 19����ͼ��ʾ�������������õ��������û������һ�������Ŀ��������̶�����������¶Ⱥ㶨��һ��ϸ����������ڻ����ϣ���һ�˿�������ֺ�������һ��СͰ�ϣ���ʼʱ������ֹ�����ڲ�����СͰ������ϸɳ��ʹ�������������ƶ�������ʼ��δ���������ף�������������Ӽ�����ã����ڻ����ƶ������У�����˵����ȷ���ǣ����� ��
19����ͼ��ʾ�������������õ��������û������һ�������Ŀ��������̶�����������¶Ⱥ㶨��һ��ϸ����������ڻ����ϣ���һ�˿�������ֺ�������һ��СͰ�ϣ���ʼʱ������ֹ�����ڲ�����СͰ������ϸɳ��ʹ�������������ƶ�������ʼ��δ���������ף�������������Ӽ�����ã����ڻ����ƶ������У�����˵����ȷ���ǣ����� ��
A������������ķ���ƽ�����ܱ�С��B�������������ѹǿ��С
C����������������ų���������D������������������������
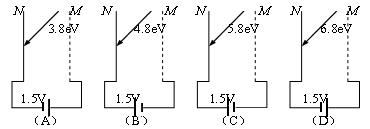
20����ͼ��ʾ��NΪ�ٰ壬MΪ�����������Ƿֱ����ص���������������صĵ綯�ƺͼ�������ͼ�б������֪�����ٵ��ݳ���Ϊ4.5eV���ֱַ��ò�ͬ�����Ĺ��������ٰ壨�����ӵ�������ͼ�ϱ��������ô���и�ͼ�У�����ӿ��ܴﵽ���������ǣ�������
21����ͼ��ʾ��ƽ�н���������ˮƽ�������Ϊ����������費�ƣ�����ֵΪR�Ķ�ֵ����
��������ǿ�ų���ֱ��������ƽ�棬�Ÿ�ǿ��ΪB����һ����Ϊm��Ϊl�ĵ������ab
λ�û�ƽ��б��Ĵ�СΪv�ij��������˶�����Զ����a /b /��λ�ã����еľ���Ϊs�������
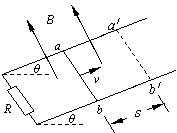 �ĵ���ҲΪR���뵼��֮��Ķ�Ħ������Ϊ����������
�ĵ���ҲΪR���뵼��֮��Ķ�Ħ������Ϊ����������
A���ϻ������е�����ܵ����������ΪB
B���ϻ������а�����������Ħ�����������Ե���������ܹ�Ϊmv2/2��
C���ϻ������е�����������������Ϊmv2/2��mgs (sin������cos��)��
D���ϻ������е������ʧ�Ļ�е��Ϊmv2/2��mgs sin����
�ڢ������ѡ���⣬��174�֣�
22��ʵ���⣨18�֣�
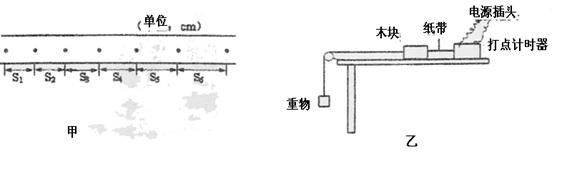
�� ����8�֣���̽�����ٶ����������������������Ĺ�ϵʵ���У�ʵ��װ����ͼ����ʾ��һľ�����ˮƽ�⻬��ľ���ϣ����˩��һ�����쳤��ϸ���ߣ�����̶���ľ���Ե�Ļ�����һ�������������������Ϊm��ľ���Ҳ��봩������ʱ����ֽ��������������ǣ���£�ľ����ľ���������ȼ����˶���ͼ�����˴���ʱ����ֽ���ϴ����һЩ�����ĵ㣬����֮��ľ���ֱ�ΪS1��S2��S3��S4��S5��S6������ʱ�����ý���������ΪT�����ݸ�����������
�� ��1��ľ����ٶȵı���ʽ��a=���������������������������������� ��
�� ��2��ϸ�߶�ľ�������ı���ʽ��T=���������������������������������� ��
|
�� ����10�֣�����һ������Rx��ֵ��ԼΪ70![]() ���������������ģ�
���������������ģ�
| |
B����ѹ����0��3V��15V ����ֱ���
�� 3k![]() ��15k
��15k![]() ��
��
C����Դ��1.5V�ɵ��2 �ڣ�
D������������R1��0��10![]() ��
��
E������������R2��0��1k![]() ��
��
F���������������
�� ��1�����������������ĺ�ʵ��Ҫ��
�ڷ����л���ʵ���·ͼ
|
�� ��2��ʵ���е�ѹ��ѡ���������������� ���̣�����������ѡ���������������� ��
�� ��3�����ݵ�·ͼ��ѡ����������Ӻ������ʵ����·ͼ��
23����16�֣���ij����͵�����ܶ���ͬ�������������渽����һ����Ϊ
�� ��1���������뾶�����İ뾶֮��Ϊ���٣�
24����18�֣�ij�й涨����������һ����·����ʻ�ٶȲ��ó���
�� ��1�������жϴ��������Ƿ�Υ���涨������ʻ���ٶ�ɲ�������ȼ����˶�������ʱ��ȡg =
�� ��2�����������װ���ַ�����װ�ã������ɲ��ʱ�ɻ�ñȳ��ֱ���ʱ������ƶ������Ӷ�ʹɲ���������С������Сɲ���������DZ��⽻ͨ�¹ʵ�����Ч;����ɲ��������������ij��ٶȡ��ƶ����й��⣬�����뿼�Ǽ�ʻԱ�ķ�Ӧʱ�䣨˾���ӷ������������������ƶ�����ʱ�䣩������������װ���ַ�����װ�ú�ɲ��ʱ���ƶ����Ƕ�ֵf����ʻԱ�ķ�Ӧʱ��Ϊt0������������Ϊm����ʻ�ٶ�Ϊv0������ͨ������ɲ�����벢˵�����ٹ�·���Ͻ����١����غ;ƺ��ʻ��ԭ��
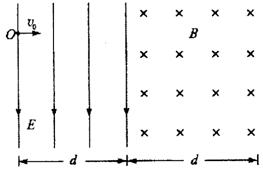
25����20�֣���ͼ��ʾ����ǿ�糡�������ǿ�ų������ǽ��ڵ��ҿ�����Ⱦ�Ϊd���糡������ֽƽ���ڣ����ų�����ֱֽ�����һ���������Ӵ�O�����ٶ�v0�ش�ֱ�糡�������糡���ڵ糡���������·���ƫת����A���뿪�糡����ų����뿪�糡ʱ���������ڵ糡�����λ��Ϊ�糡���ȵ�һ�룬�����Ӵ�C�㣨A��C����ͼ��δ����������ų�ʱ�ٶȷ��������糡O��ʱ���ٶȷ���һ�£������������������ƣ���
|
�� ��2���糡ǿ��E�ʹŸ�Ӧǿ��B�ı�ֵ![]() ��
��
�� ��3�������ڵ硢�ų��е��˶�����ʱ�䡣
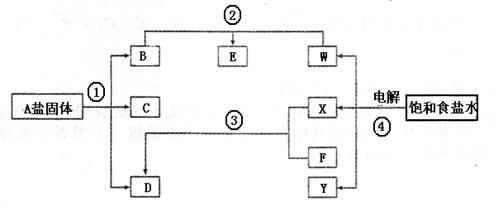
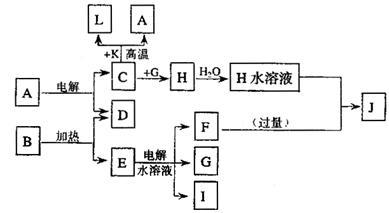
26����16�֣����ַǽ���Ԫ��X��Y��λ�ڶ����ڵ��������ڡ������塣��֪��Ԫ������������ˮ�����Ϊǿ�ᡣ������ͼת����ϵ����Ӧ���������ֲ�������ȥ�����ش����⣺
|
�� ��1����A��B��C��D��Ϊ��XԪ�صĻ������A��һ��������ֻ����10�����ӣ���A���ӵĽṹʽΪ�������������� ����Ӧ�١��ڡ����ǹ�ҵ���������������� ���ѧʽ���Ļ���ԭ�������з�Ӧ�ٵĻ�ѧ����ʽΪ
�������������������������������������������������������������������������� ��
��Ӧ�ܵ����ӷ���ʽΪ���������������������������������������������� ��
��
��2����A��B��C��D��Ϊ��YԪ�صĻ������A��Ħ������Ϊ
|
��
��1����PtΪ�缫���κͷ�̪�ı���ʳ��ˮʱ�������ĵ缫��ӦʽΪ���������� ������������Һ����ɫ��Ϊ��ɫ��ԭ���������������������� ��������
�� ��2��д��A��X�Ļ�ѧʽ��A������������������ ��X������������������ ��
�� ��3��д����Ӧ�ڵĻ�ѧ����ʽ������������������ ��
�� ��4��д����Ӧ�۵������������������������� ��
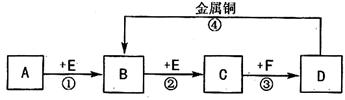
28����12�֣�A~J�ֱ������ѧ��ѧ�г�����һ�ֵ��ʻ����ת����ϵ��ͼ��
|
������
��֪C��D��G��IΪ������Ԫ���γɵĵ��ʣ�D��G��I������Ϊ��̬���γ�D��Ԫ�ص�ԭ�������������Ǵ�����3����B����ɫ��Ӧ�г���ɫ������ɫ�ܲ�������
������ ��ش�
�� ��1��I��G��ȼ��ʱ������Ϊ���������������������������������� ��
�� ��2��L��ĿǰӦ����㷺�Ľ�������̼����������L��������д�����Eˮ��Һ�Ļ�ѧ����ʽ�������������������������������������������� ��
�� ��3����֪KΪ����ɫ��ĩ��д��C��K��Ӧ�Ļ�ѧ����ʽ�������������������� ��
�������������÷�Ӧ�IJ���Ϊ�������������� ��������������������������
�� ��4��J��H��Ӧ�����ӷ���ʽΪ�������������������������������������� ����������ת����ϵ��ÿһ����Ӧ��Ϊǡ�÷�Ӧ���Ҳ�����C+K��A+L�ı仯ʱ��Ϊ�����յõ�J����A��B�����ʵ���֮��Ϊ������������ ��
|
29��(14��)Cu��Fe�Ͻ����ڳ�ʱ�����ڿ����б��������һ������Ĥ(�ɷ�ΪFe![]() O
O![]() �� CuO)���ֽ�������ʵ�飨��������������ڱ�״���²��)��
�� CuO)���ֽ�������ʵ�飨��������������ڱ�״���²��)��
�ٽ��˺Ͻ�5��![]() SO
SO![]() �����������������ռ�����������ΪVmL�����˵���ɫ��ҺA������Cu
�����������������ռ�����������ΪVmL�����˵���ɫ��ҺA������Cu![]() �������������� B��
�������������� B��
������BͶ�뵽һ��Ũ�ȵ�HNO![]() �У���ȫ�ܽ⣮��NO��NO���ģ�̨����896mL��
�У���ȫ�ܽ⣮��NO��NO���ģ�̨����896mL��
���������˻��������ܶ�Ϊ1
�۽���������Һ����dͬ�F����i��q HN![]() ,����ǡ����ȫ����ˮ��
,����ǡ����ȫ����ˮ��
��1������ʱ��Ӧ�õ��IJ���������_______________________________
��2��A�е���������______________������B�к�______________________
��3������ʴǰ�ĺϽ���Fe�����ʵ���Ϊ_________mo1��Cu�����ʵ���Ϊ________mo1
��4��V����ֵΪ__________
30��(20��)�������й������³´�л���������⡣
I���������������� �����ͼ��ʾ����ǿ�ȵı仯��ijֲ�������ʵĹ�ϵ����ͼ��ʾ�¶ȱ仯��ij��ֲ���������ʵĹ�ϵ����ͼ��ʾɭ��Ҷ���ָ���������úͺ������õĹ�ϵ(Ҷ���ָ����ָ��λ���������ֲ��Ҷ�������������ֵԽ��ʾֲ��ҶƬ�����̶�Խ��)����ش�
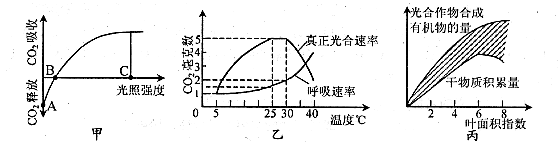
����(1)����ͼ�����߱�ʾij��Ҷ����(����ֲ��)�Ĺ�����ʣ���Ļ������(����ֲ��)�Ĺ����������ʱ���൱��ͼ��C���λ���ƶ�����Ӧ���������������� �����ٶ��¶����ǿ�ȵ���ǿ�������ߣ���ͼ��B��C��ĺ���ǿ�ȴ�С�Ĺ�ϵӦ��Ϊ���������������������� ��
����(2)����ͼ������֪����ֲ������������̬��������ʱ�����������Ҫ�ﵽ�����¶�Ҫ��Ӧ���������������������������� ������
����(3)�����ϴ�����ֲ�߲�ʱ��Ϊ��֤�нϸߵIJ���������Ĺ���ǿ��Ӧ���������൱�ڼ�ͼ�е���һ��?������������ ������������������������������
����(4)�ڶ�ɭ����Դ�������У�һ��Ҫ��Ҷ���ָ��Ϊ6������Ϊ8ʱ������ľ�IJɷ��ȽϺ��㣬���Ҫ˵��ԭ��
����II���������˶�ʱ���ļ���ATP��Ҫ����������10������������ATP��Ҫ���������ӵ�t00�����ϡ���ش�
����(1)�˶��еļ���ϸ������Ҫ��ATP��Ҫ��ͨ�������������������� �ڵ������������������ġ�����������������������������������ͨ�������������� ���̽��в��䡣��һ�����в����ı�ͪ������ �������� �ڱ���ԭ������������ �ġ�
����(2)�������Ĺ�Ӧ�dz���ģ�ϸ�����������в����ı�ͪ��Ҳ�������������� ø�Ĵ��£����ɱ����ᡣ
����(3)�������������ĵ��������������������������� ��
������д������������һϵ������ת�ƹ����У�ATP����Ĺؼ����ã�
����������ɫֲ��Ĺ�������У����������������������������������� ��
�������������ڵ�ϸ�������У����������������������� ����������������
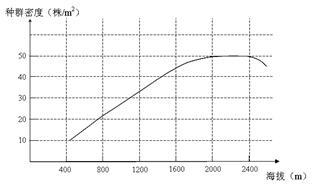 31.��22�֣��Ͼ�����ԭ���������ޣ����ҹ�Σ�������������֡���ѧ�Ҷ��Ͼ���������Ⱥ�ܶȽ����˵��飬�о����������뺣�εĹ�ϵ���������ͼ��ʾ��
31.��22�֣��Ͼ�����ԭ���������ޣ����ҹ�Σ�������������֡���ѧ�Ҷ��Ͼ���������Ⱥ�ܶȽ����˵��飬�о����������뺣�εĹ�ϵ���������ͼ��ʾ��
��1����ֲ����Ⱥ�ܶȽ���ȡ������ʱ����������������������ͼ�������������Ͼ����������������___________��Ӱ���Ͼ������ֲ�����Ҫ������������______________��
��2���Ͼ�������һ�������������ܼ���Ƭ���Ծ��˵ķ�ֳ�����ų�ijЩֲ���������������̬ϵͳ�ĵֿ����ȶ����������������� ��
��3���о������Ͼ������ķ���ʱ���֣�����ʵӬ�ɽ��ܾ��Ѳ����Ͼ��������ڣ������Ͼ��������������˷�������������֮����������� ��ϵ�����ŵ���_________________�� ���⣬2,4-D�ȳ��ݼ����Ͼ�����Ҳ��һ���Ŀ������ã�ԭ������������������ ��
| |
| |
��4����ѧ�����о��Ͼ�����ʱ����������һ�ִ�������ֲ�����ƻ�ɫ�Ļ���λ�ڳ�Ⱦɫ���ϣ��Һ컨��A������a��Ϊ���ԣ������Ҷ�εĻ���λ��XȾɫ���ϣ��ҿ�Ҷ��B������Ҷ��b��Ϊ���ԡ�
��Ҫ����һ���ӽ�ʵ�飬��֤��ֲ��Ҷ�ε��Ŵ����ڰ����Ŵ�����Ӧѡ���ױ���Ҷ���������ǣ������������� ��ĸ������������ ��
��ѡ�����Ҷ�ͺ컨��Ҷ���ױ������ӽ���F1�ı����ͼ��������±���
| F1�ı����ͼ����� | ���� | ���� | ||
| �컨��Ҷ��1/4�� | ����Ҷ��1/4�� | �컨��Ҷ��1/4�� | ����Ҷ��1/4�� | |
�����Ŵ�ͼ���ʾ���ӽ����̡�
5�¸������۲ο���
һ�������������� ѡ����
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| �� | C | A | C | B | B | D | C | B | D | C | D |
| ��� | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | |
| �� | B | A | A | BC | C | BC | AC | BD | D | CD |
������ѡ����
22��ʵ���⣨18�֣�
����8�֣�
��
��1��![]() ��4�֣���������ʾ3�֣�
��4�֣���������ʾ3�֣�
��
��2��![]() ��4�֣�
��4�֣�
[˵��������1���м��ٶȲ�������ʾ������2�������ˣ�1���Ľ������2�����۷�]
����10�֣�
�� ��1��ͼ��3�֣�
�� ��2��0 �C 3V��2�֣��� R1��2�֣�
�� ��3��3��
|
23����16�֣�
�⣺��С�� ��
��
��ã�![]() ��
��
�Ե����������壬��![]() ��
��
����������������
![]() ��
��
![]() ��
��
��ã�![]() ��
��
����������Ӧ�У�![]() ��
��
����![]() ��
��
���ֱ����٢ۢ�ʽÿʽ3�֣���ʽ4�֣��ڢܢ�ʽÿʽ1�֣��ܼ�16�֡�
24����18�֣�
�� ��1�����ֱ����������������ȼ����˶������ٶȴ�СΪ
��������![]() �������������������������������������������������������� ��3�֣�
�������������������������������������������������������� ��3�֣�
��������������ɲ��ʱ�ٶ�Ϊv0�������˶�ѧ��ʽ��
��������![]() �������������������������������������������������������������������� ��3�֣�
�������������������������������������������������������������������� ��3�֣�
����������![]() ������������������������������2�֣�
������������������������������2�֣�
��������������������Ϊ
�� ��2�����Ǽ�ʻԱ�ķ�Ӧʱ��t0���ƶ���f���������ʻԱ���������Ӧ������ɲ��ֱ��ͣ�µĹ����У�������ʻ�ľ���LΪ
��������![]() �������������������������������������� ��5�֣�
�������������������������������������� ��5�֣�
������������ʽ���Կ���������v0������m�ƺ��ʻ��Ӧʱ��t0������������ɲ��������������ɽ�ͨ�¹ʡ�
25���⣺��1�������ڵ糡��ƫת���ڴ�ֱ�糡����![]() ��ƽ�е糡����
��ƽ�е糡����![]()
����![]() ��
��![]() ��
�� ![]() ����
���� ![]()
���������ڴų���������Բ���˶����ʴ����ų��ٶ�![]()
�� ��2���ڵ糡���˶�ʱ��![]() ���� ��
���� �� ![]()
|
�����˶�����ı�45�㣬�˶��뾶![]()
������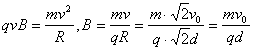 ����
����
��
![]()
�� ��3�������ڴų����˶�ʱ��
����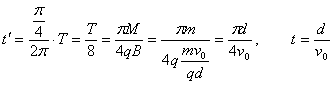
�˶���ʱ�� t��=![]()
26����16�֣�
|
����������
 |
�������� 4NH3+5O2������ 4NO+6H2O��3�֣�
 ��������
3Cu+8H++2NO3��=3Cu2++2NO��+4H2O��3�֣�
��������
3Cu+8H++2NO3��=3Cu2++2NO��+4H2O��3�֣�
�� ��2��H2SO4��1�֣���4FeS2+11O2������ 2Fe2O3+8SO2��3�֣�
�����������������ȣ�2�֣����������ڵڢ��壨2�֣�
27����12�֣�
�� ��1���� C12��
![]() ��ΪH2O���� H++OH-����2H++2e-
��ΪH2O���� H++OH-����2H++2e-����H2��ʹC��OH-����������
�� ��2��NH4HCO3[��NH4��2CO3]��H2
�� ��3��NaOH+CO2 �� NaHCO3������������Ҳ�ɣ�
�� ��4�����¡���ѹ��������ÿ��2�֣���12�֣�
|
|
�� ��3��2Al+Fe2O3������Al2O3+3Fe����Al��Fe2O3������м�KClO3O��ĩ������þ������ȼþ��
�� ��4��Al3++3AlO![]() +6H2O=4Al(OH)3����1:8
+6H2O=4Al(OH)3����1:8
29����14�֣�
��1��©�������������ձ���3�֣�
��2��Fe2+�� H+��������2�֣�Cu��2�֣�
��3��0.04mol��0.05mol ��4�֣�
��4��448��3�֣�

31.��20��
��1�������� ����
��2���½�
��3����������
���г�Ч������������Ⱦ���ص㣬�ܱ�����������ԣ��������һ��ɵ÷֣�
��Ũ�ȵ�2,4-D�����Ͼ���������������2,4-D��ֲ�����������þ��������ԣ�
��4�������� ��Ҷ����ĸ���� ��Ҷ
�����Ŵ�ͼ�⣺
 |
���ֱ�����1������2������3��ÿ��2�֣���14�֣�
��4����8�֡�ǰ����ÿ��1�֣��Ŵ�ͼ��6�֣������ױ������ͱ�������д��ȷ2�֣�ÿ���ױ�1�֣����Ŵ�ͼ����ط��ţ�P��F1 �� ����дΪ�ױ� �Ӵ� ����д��ȷ1�֣��Ӵ�������ȫ����д��ȷ1�֣�������ȫ����д��ȷ1�֣���ֵ��ȷ1�֡�