�߿�������ѧ��������Ծ�
�������ۺϣ�
�����ߣ���־������ë���С�������
������֪��
����1��ȫ�����Ծ����Ծ���ʹ��������Խ��������������Ͻ���
2���Ծ��� 9 ҳ����31С�⡣����300�֣�����ʱ��150���ӡ�
3���뽫�����ڴ����������Ӧλ���ϣ�д���Ծ�����Ч��
4�����øֱʻ�Բ��ʽ���������֤����ֱ���д�ڴ����������Ӧλ���ϡ�
5�������������ԭ��������H��1 O��16��Zn:65
�Ծ���
����2BǦ�ʽ�������ϵ���֤�ź�ѧ����������Ӧ�����Ż�Ϳ�ڣ�Ȼ��ʼ���⡣
һ��ѡ����(��13С�⣬��78�֡�ÿС��ֻ��һ�����������ѡ���ѡ����ѡ��������)
1�������ǵȹ������������˴��ģ�������У���ŷ�����ķ�ţ���Ϳ�����һ�������������Ե�����ʳƷ������ó�ֻš����й��������е�����ѧ��˵������������
A������ֻ��������ϸ����Ŀ�ԭ��������������ϸ���ڵĿ�ԭ
����B����Һ���߶Բ�ԭ��ͨ��ѪҺѭ����ɢ�����������
����C�������ͨ��ЧӦTϸ��������ϸ������-2�ֿ���ԭ��
����D��ЧӦTϸ���ܼ����ϸ���е���ø����ͷ��ܰ�����
2��ũ��ԱΪȷ�����߲˴�����CO2Ũ�ȵı仯������ڴ����ڰ�װ��CO2���������ٶ�6ʱ��18ʱ�ֱ�Ϊ�ճ�������ʱ�䣬Ԥ��һ���ڴ�����CO2Ũ�ȵı仯�����
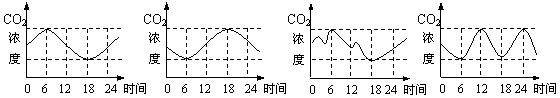 |
A������������������ B������������������ C���������������� D
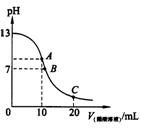
3�����û����ֶΣ��ѳɹ��������������������صĽ�ĸ����ij��ҩ������þ�����������о�����һ�̶��ݻ��ķ����������ý�ĸ�����±��Ƕ�ʱȡ���ⶨ��������pH���������������/mL�����õĽ����
| ��Ʒ���� | a | b | c | d | e | f | g | H |
| �������� | 32 | 56 | 127 | 234 | 762 | 819 | 821 | 824 |
| pH | 6.0 | 4.7 | 5.9 | 4.9 | 5.7 | 5.3 | 5.1 | 5.6 |
��������ȡ��ʱ������Ա�Ĵ��ģ����˱��ȡ����ʱ�䡣����Ըñ�������������ȷ����
A�� d��ʱ���������е��������ľ���
B�����Ҫ��������������c��ʱ��ѡȡ����
C��g��ʱ�ڴμ���л���������൱�Ļ���
D��������ȡ�����ʱ�䣬�����������������
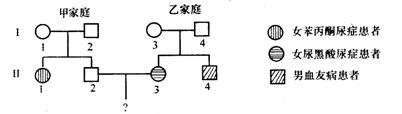
4���ֲ�������ù��һ����������ֳ������ͨ���ɵ������˿�ӽ��ɶ�������ӡ����ӽ���һ�μ������Ѻ��ٽ���һ����˿���ѣ������γ�8�����ӡ���֪���Ӵ��ͣ�R����С�ͣ�r��Ϊ���ԣ���ɫ��T����ɫ��t��Ϊ���ԣ���ͼ��ʾij�����γ����ӵĹ��̣�
 |
���и�ѡ������������
A��a��c�Ļ���������ͬ�ġ�����������B�����ӵĻ�����ΪRrtt��
����C��b�Ļ�������RT������������������ D��d���ܷ����˻���ͻ��
5��ޱ�ʾ�ԭ�����С������ޣ����������ҹ���������ϲ�⡢������Ԯ�����Ϲ�ľ����ľ����Ѹ���γ����긲��֮�ƣ�����ȵ��������⣬�����ǵ�ֲ��ͻ�����ȱ���������ή��ޱ�ʾ����ҹ��Ѿ�����˴�Ŀ���ĵ�������Σ�����Դ�˵������ȷ����
A�������������ֿ����������������
B��Ӧ�öž��������ֵ�����
C��ޱ�ʾ��뱻�串�ǵ���ɫֲ���Ĺ�ϵ�Ǿ���
D��ޱ�ʾշ��ĵ�ԭ��������ԭ���غ�������ͻ��Ľ��
6. ����������2007�ꡰ���ᡱ����Ҫ���⣬���������ǹ�������κ���������˵����ȷ���ǡ���������
A������ʹ�ú���ϴ�Ӽ��������ɫ��Ⱦ
����B������ʹ�÷��ȴ����Ŀ����Ϊ�˼�������
����C���������ɵ���ˮ�������Դ����������ᾭ�÷�չ������
����D����ȼ�ϵ��������ʹ�ã�������Ч���ٳ��п�����Ⱦ��
7�������и������ӵ�������ȷ����(��)
����A��![]() ��
��![]() ��
��![]() ��
��![]() ����ˮ��Һ�д�������
����ˮ��Һ�д�������
����B�� ![]() ��
��![]() ��
��![]() ��
��![]() ���ڼ�����Һ�д�������
���ڼ�����Һ�д�������
����C��![]() ��
��![]() ��
��![]() ��
��![]() �ܴ�����������Һ�Ժ�ɫ
�ܴ�����������Һ�Ժ�ɫ
 ����D��
����D��![]() ��
��![]() ��I-��
��I-��![]() ����������Һ�д�������
����������Һ�д�������
8��2006��ŵ������ѧ������������ѧ��Roger��D��Kormberg������ʾ������������ڵ�ϸ��������û����ڴ洢����Ϣ���������ʡ����й��ڵ����ʵ�˵������ȷ����
A�������ʾ�Ϊ��Ȼ�л��߷��ӻ����û�е����ʾ�û������
B�������ʾ�������ˮ�����ܸ�Ũ�������ñ��
C��HCHO��Һ��(NH4)2SO4��Һ����ʹ�����ʱ���
D�����Բ��ö���������������ķ��������ᴿ������
9��14C��̼��һ��ͬλ��ԭ�ӡ���N0Ϊ�����ӵ�����ֵ������˵������
����ȷ���ǡ�����������
A��1/8 mol 14CH4��������������ΪN0
B��7 g 14Cԭ���γɵ�ʯī��ȫȼ�����ɶ�����̼ʱ��ת�Ƶĵ�����Ϊ2N0
C�����³�ѹ�£�22.4 L��14C�Ķ�����̼�з���������N0
D�����³�ѹ�£�17 g������14CH3������������Ϊ9N0
10��1g ��������������ȫȼ��������̬ˮʱ���ų�����120.9kJ��������˵����ȷ���ǡ����� ��������
������ A����Ӧ���Ȼ�ѧ����ʽ��2H2(g)+O2(g)=2H2O(g)����H=+483.6kJ��mol��1
������ B��������ȼ����Ϊ241.8 kJ��mol��1
������ C��1molH2O(1)����������1molH2O(g)������
������ D��2molH2��1molO2�������ܺʹ���2molH2O(g)������
11�����Ե�ؾ��������ŵ��������ص㣬����õ��㷺Ӧ�á�п���̼��Ե��������������ҺΪ���Һ������ܷ�ӦʽΪ��Zn��s��+2MnO2��s��+H2O��l����Zn(OH)2
(s)+Mn2O3��s������˵��������ǡ�����������������������
������ A����ع���ʱ��пʧȥ����
������ B����������ĵ缫��ӦʽΪ��2MnO2��s��+H2O��l��+2e��=Mn2O3��s��+2OH����aq��
������ C����ع���ʱ������������ͨ�����·����
������ D�����·��ÿͨ��0.2mol���ӣ�п�����������ϼ�С6.5g
12����һ�ݻ��㶨�ܱ������У������ʵ�����A��B�������·�Ӧ��A(g)+2B(g)![]() 2C(g)��һ��ʱ���Ӧ�ﵽƽ�⣬��ͬ�¶������û������ѹǿ��ԭ����4/5������ʱA��ת�����ǡ�����������������������������������������������������
(�� )
2C(g)��һ��ʱ���Ӧ�ﵽƽ�⣬��ͬ�¶������û������ѹǿ��ԭ����4/5������ʱA��ת�����ǡ�����������������������������������������������������
(�� )
A��40%������ ��B��50%��������C��60%��������D��70%
|
������A����A�㣺![]()
������B����B�㣺![]()
������C����C�㣺![]()
������D����C�㣺![]()
����ѡ���⣨��8С�⣬��48������ÿС��������ĸ�ѡ���У��е�С��ֻ��һ��ѡ����ȷ���е�С���ж��ѡ����ȷ��ȫ��ѡ�Եĵ�6�֣�ѡ�Ե���ȫ�ĵ�3�֣���ѡ����ѡ�ĵ�0�֣�
14��һȺ���ڻ�̬����ԭ������������Eo�Ĺ��Ӻ��ͷų����������Ĺ��ӣ�������һ�ֹ��ӵ�����ΪE1��������˵����ȷ���ǡ���������
����A��E1һ��������Eo�������������� B��E1һ����С��Eo��
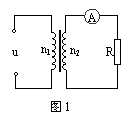 C��E1һ��С��Eo ���������������� D��E1һ������Eo
C��E1һ��С��Eo ���������������� D��E1һ������Eo
15����ͼ1��ʾ�������ѹ��ԭ��Ȧ���뽻���ѹ![]() ������Ȧ����һ����������ֵΪ100���ĸ��ص���R����õ�������ʾ��Ϊ0.10A���ɴ˿�֪�ñ�ѹ����ԭ������Ȧ��������Ϊ����
��
������Ȧ����һ����������ֵΪ100���ĸ��ص���R����õ�������ʾ��Ϊ0.10A���ɴ˿�֪�ñ�ѹ����ԭ������Ȧ��������Ϊ����
��
������ A��141��1���� B��14.1��1�������� C��100��1������ D��10��1
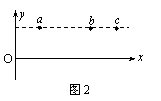 16����ͼ2��ʾ��a��b��c��ʾijʱ��һ��г�Შ�IJ���ͼ����һ��ƽ����x���ֱ���ཻ�������ʵ㣬�����������ʵ���˶����������˵����ȷ���� (��)
16����ͼ2��ʾ��a��b��c��ʾijʱ��һ��г�Შ�IJ���ͼ����һ��ƽ����x���ֱ���ཻ�������ʵ㣬�����������ʵ���˶����������˵����ȷ���� (��)
A����ʱ���������ʵ�һ��������ͬ�ļ��ٶ�
B����ʱ���������ʵ�һ��������ͬ���ٶ�
C������ʱ���������ʵ������ƽ��λ�õ�λ�ƶ���ͬ
D����������ʱ�䣬�������ʵ�ͨ����·�̶���ͬ
17������������A��B��A��B֮�������ò��ƣ������Ǹ���һ�ſ������������ǣ������������ǵ�������ȣ��ɴ˿�֪��������
������ A������A��B�����������ٶ�֮�ȵ������ǵİ뾶֮��
������ B���������ǵ����ٶ�һ�����
������ C������A��B������һ�����
D������A��B���ܶȲ�һ�����
18��һ������������(���������������ܲ���)����ƽ��״̬�����跨ʹ���¶Ƚ���ͬʱѹǿ���ﵽƽ��״̬������״̬���Ϊ״̬��Ĺ����С� ������ ��
A�� ������ӵ�ƽ�����ܱض���С��
��B����λʱ����������Ӷ����ڵ�λ�������ײ��������
����C����������ܿ��ܲ��䡡��������������
D������ض��ų�����
 19����ͼ3��ʾ����������ȫ��ͬ������ƽ�еIJ��������һ�ȱ������Σ��м��ǿ��������к����������һϸ������ƽ�еױ�BC��AB�����룬��AC����������AC������Ĺ���������
19����ͼ3��ʾ����������ȫ��ͬ������ƽ�еIJ��������һ�ȱ������Σ��м��ǿ��������к����������һϸ������ƽ�еױ�BC��AB�����룬��AC����������AC������Ĺ���������
����A���ֳ�����������Ϊ��⣬����Ϊ����
����B���ֳ�����������Ϊ���⣬����Ϊ���
����C����ȻΪһ��������ױ�BCƽ��
����D����ȻΪһ��������ױ�BCƫ��
20��K �C����˥�䷽��Ϊ��K�C���� �C+��o������K�C���Ӻ��� �C���Ӵ����Ļ�Ԫ��ɣ���o���Ӳ����硣��ͼ4��ʾ��һ��K�C�����ش�ֱ�ڴų��ķ���������ǿ�ų��У���켣ΪԲ����ͼ4�����ߣ������ڴų��з���˥�䣬���� �C���Ӻ���o�����˶��켣�����������ͼ�еģ��� ��
 |
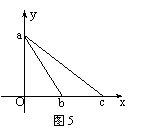 21����ͼ5��ʾ����xOy����ϵ�н�һ������y����a������x��b��ʱ����˷��糡������W������һ���Ӵ�a������x����c��ʱ��������ܼ�СW����ô���ڴ˿ռ���ڵľ��糡�����ǣ�������
21����ͼ5��ʾ����xOy����ϵ�н�һ������y����a������x��b��ʱ����˷��糡������W������һ���Ӵ�a������x����c��ʱ��������ܼ�СW����ô���ڴ˿ռ���ڵľ��糡�����ǣ�������
A���糡ǿ�ȷ�����x�Ḻ�����ǿ�糡
B������y���ϵ�һ�������γɵĵ糡
C������y���ϵ�һ�Ե������ֵ����γɵĵ糡
D������һ�Ե���ͬ�ֵ����γɵĵ糡
�Ծ���
22��(17��)
�ţ�5�֣��漰��ʵ����������˵��������������ȷ�ģ�����������
��A�����ò��ͷ�뷨�ⶨ���������ʡ���ʵ���У����ⲣ��ש�����治һ��Ҫ��ƽ��
��B��������Ĥ�������ֱ������ʵ���У���������ϡ����Һ����ҪĿ����Ϊ�˼�������ĺ���
��C������֤��ײ�ж����غ㡱��ʵ���У��������ײС�����������Ҫ������������
��D�����о�ƽ���˶�����ʵ���У����Լ�¼С��ƽ���˶��켣��ľ��ֻҪ��ֱ�̶�����
�ƣ�12�֣������������ģ�
������A1������0.2A������Լ0.5������������ ������A2������0.02A������Լ1������
��ѹ��V1������3V������Լ3k�������������� ��ѹ��V2������100V������ܴ�
����������R��0��10������������������������ ������Ro��0��9999.9����0.1A
��������E���綯��E=6V������r=0.1���������������S���������ɡ�
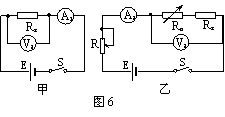 Ϊ��ȷ�زⶨһ����ֵRxԼΪ1.2���ĵ���˿����ֵ�����мס�����λͬѧ�ֱ��������ͼ6�ס��Ҷ�����·ͼ������Rx�����ס�������·��ƾ��в�����֮������ָ�����ڵ����⣨��ͼ������ָ��һ�����⣩��
Ϊ��ȷ�زⶨһ����ֵRxԼΪ1.2���ĵ���˿����ֵ�����мס�����λͬѧ�ֱ��������ͼ6�ס��Ҷ�����·ͼ������Rx�����ס�������·��ƾ��в�����֮������ָ�����ڵ����⣨��ͼ������ָ��һ�����⣩��
��ͼ������֮���������� ����������
��ͼ������֮���������� ����������
�������������ѡ��������ģ����һ��������ĵ�·ͼ�����ڴ�����Ϲ涨�����߷����ڣ�ͼ�б��������ѡ�����ĵķ��ţ���
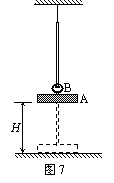 23����16�֣���ͼ7��ʾ������A��װ�г�0.5m��ֱ���ˣ�������Ϊ1kg����ϸ�����ң�����������ˮƽ����H=0.2m��������������Ϊ0.2kg��С��B������˼���Ħ�����軷�����Ի���ʱĦ������Сʼ�ղ��䣬���ӵ�����
23����16�֣���ͼ7��ʾ������A��װ�г�0.5m��ֱ���ˣ�������Ϊ1kg����ϸ�����ң�����������ˮƽ����H=0.2m��������������Ϊ0.2kg��С��B������˼���Ħ�����軷�����Ի���ʱĦ������Сʼ�ղ��䣬���ӵ�����![]() m/s�ij��ٶ��ظ������˶������ǡ�ܵ���˵Ķ��ˣ�ȡg=10m/s2������
m/s�ij��ٶ��ظ������˶������ǡ�ܵ���˵Ķ��ˣ�ȡg=10m/s2������
�Ż��ظ��ϻ������еļ��ٶȴ�С��
���ڻ��ϻ������У�ϸ�߶Ը˵�������С��
����С���ڸ˶���ʱϸ��ͻȻ�ϵ���������������������ճ�Ϻ�ֹ���������̸�û�лζ������߶Ϻʱ�价��һ�������������
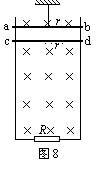 24����19�֣���ͼ8��ʾ���㹻���������⻬�̶��������0.5m��ֱ���ã�������費�ƣ��¶�������ֵΪ1���ĵ���R�����촦�ڴŸ�Ӧǿ��Ϊ0.8T����ǿ�ų�B�У��ų�����ֱ�ڵ���ƽ���������������Ϊ0.04kg�������Ϊ0.5����ˮƽ������ab��cd���뵼��Ӵ����ã�������ab��һ��ϸ�����ң�ϸ���������ܵ��������Ϊ0.64N������cd���Ӿ�ֹ��ʼ���䣬��1s��ϸ���պñ����ϣ�gȡ10m/s2����
24����19�֣���ͼ8��ʾ���㹻���������⻬�̶��������0.5m��ֱ���ã�������費�ƣ��¶�������ֵΪ1���ĵ���R�����촦�ڴŸ�Ӧǿ��Ϊ0.8T����ǿ�ų�B�У��ų�����ֱ�ڵ���ƽ���������������Ϊ0.04kg�������Ϊ0.5����ˮƽ������ab��cd���뵼��Ӵ����ã�������ab��һ��ϸ�����ң�ϸ���������ܵ��������Ϊ0.64N������cd���Ӿ�ֹ��ʼ���䣬��1s��ϸ���պñ����ϣ�gȡ10m/s2����
��ϸ�߸ձ�����ʱ��������·���ĵ��ܵ繦��P��
�ƴ�cd����ʼ���䵽ϸ�߸պñ����ϵĹ����У�ͨ��cd���ĵ����q��
 25����20�֣���ͼ9��ʾ������P�̶����㹻�ߵ�ˮƽ�����ϣ�С���A��B��С�ɺ��ԣ����Ƿֱ����+QA��+QB�ĵ�����������ֱ�ΪmA��mB.������ɾ�Ե���ᵯ��������һ�����쳤������������֣�һ����B���ӣ���һ������һ����С��.����װ�ô��ڳ�ǿΪE������ˮƽ�������ǿ�糡��. A��B��ʼʱ��ֹ����֪���ɵľ���ϵ��Ϊk������һ��Ħ����A��B��Ŀ�������A��B������������ֲ��䣬B�����������֡�
25����20�֣���ͼ9��ʾ������P�̶����㹻�ߵ�ˮƽ�����ϣ�С���A��B��С�ɺ��ԣ����Ƿֱ����+QA��+QB�ĵ�����������ֱ�ΪmA��mB.������ɾ�Ե���ᵯ��������һ�����쳤������������֣�һ����B���ӣ���һ������һ����С��.����װ�ô��ڳ�ǿΪE������ˮƽ�������ǿ�糡��. A��B��ʼʱ��ֹ����֪���ɵľ���ϵ��Ϊk������һ��Ħ����A��B��Ŀ�������A��B������������ֲ��䣬B�����������֡�
������С���Ϲ�һ����ΪM�����C���ɾ�ֹ�ͷţ���ʹ���A�Ե���P��ѹ��ǡΪ�㣬�������뿪P�������C�½��������룻
����C��������Ϊ2M����A���뿪����Pʱ��B���ٶȶ��
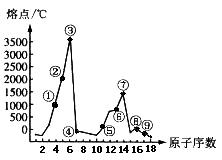 26����15�֣���ͼ�Dz��ֶ�����Ԫ�صĵ����۵�ı仯ͼ�����ݴ�ͼ����д���пո�
26����15�֣���ͼ�Dz��ֶ�����Ԫ�صĵ����۵�ı仯ͼ�����ݴ�ͼ����д���пո�
��1���ۺ�Ԫ����Ԫ�����ڱ��е�λ����___��__________��
�䡡���ʵ�һ��ͬ���������ܵ��磬��ͬ������������ƽ�
__________��____��
��2���ݡ�������Ԫ���γɵ�����������Ӧ��ˮ����֮����
����Ӧ�����ӷ���ʽΪ____��__________��
��3���ߺ�Ԫ�ص�ԭ�ӽṹ��ͼΪ____��_______��
��4���ڡ�����Ԫ���γɵĻ������侧�������ֽṹ������һ��
�ṹ����ʯ���ƣ��ýṹ�ľ�����_____��______���壬��ʹ���ۻ������ƻ���������Ϊ______________��_____��
(5) д���ݺ͢��γɳ���������ĵ���ʽ_____��__________
27��(14��)A��H�Ǵ��������Һ�е����ʣ�����A���ճ���������õĽ������ʡ�����֮�������¹�ϵ��(���ֲ���ͷ�Ӧ������)
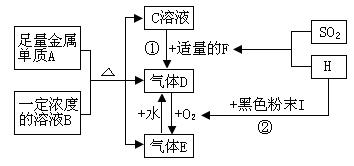
����������Ϣ���ش��������⣺
(1)д���������ʵĻ�ѧʽB���� ��������E���������� ��
(2) H�� SO2����ǿ��F���˷�Ӧ����������______��___________________________.
(3)д���ٵ����ӷ���ʽ������������������ ������������������������������ ��
(4)д���ڵĻ�ѧ����ʽ�������������� �� ����������������������������������
(5) C��Һ�е���NaOH��Һ�к��������� ���������������������������������� ��
28��(16��)�����ʾ����ij�л�����A��һ��������ת��ΪH��N�Ĺ�ϵ������N�Ǹ߷��ӡ���֪��
����![]()
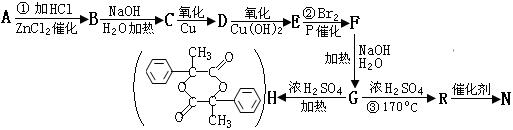
�ش��������⣺
(1)д����Ӧ���ͣ��������� ������ �������� ������������ ��
(2)д���л���Ľṹ��ʽ��F�������������� ��B������ ������������
(3)д�����л�ѧ����ʽ��
D��E���������������������������� ������������������������������ ��
R��N������������������������������ ������������������������������ ��
(4)FҲ���Ծ�һ����Ӧ����R���䷴Ӧ�����ǣ����� �������������������������� ��
(5) E��ͬ���칹���ж��֣��������ڱ��Ķ�ȡ����Ҽ�����������Ӧ����FeCl3��Һ���ܳ���ɫ��ͬ���칹����6�֣���д����������һ�ֵĽṹ��ʽ������������������ ��
29����15�֣�ij�о���ѧϰС����̽��ͭ��п��Ũ����ķ�Ӧʱ�����������ʵ�鷽����
ʵ����Ʒ����пƷ��37%Ũ���ᡢͭƬ������ˮ���Ȼ�ͭ��Һ��
��ͬѧ����пƬ����Ũ�����У���Ӧ���ʽϿ�
��ͬѧ���������н�����Ƭ���е�ʵ�飬����ʵ����̼�¼�����������н�����
|
|
�������������뽻�����ϻش��������⣺
�� ��1���ҷ�Ӧ�������Աȼ죬ԭ�������������� ���������� ��������������
�� ��2������ͬѧʵ��(2)�в���������ȼ����ʵ����������ͬѧ���������ƶϣ�
�ٱ�ͬѧ���������������ܽ���ˮ��Һ�е������ڼ���ʱ�ݳ�����Ϊ����������ˮ�������룺��ͭ������Ũ�����ڼ��������¼�����Ӧ������ɫ��Һ��������
����Ϊ��ͬѧ�ķ���������Ƿ������(���������)��������������
�ڶ�ͬѧ���룺ͭƬ�п��ܺ���п�����ʡ�Ϊ����֤�Ƿ�������������ʵ�鷽����
| ��ͬѧ���� | �����֤���� | Ԥ�������� |
| ����ΪͭƬ�п��ܺ���п������ | �� | �� |
��3�� ��ͬѧʵ��(3)�еİ�ɫ�����Ǻ����ͬѧ��������������CuCl2����ΪCuCl2��Һ����ɫ����ɫ��Ҳ���������Ȼ�п����Ϊϡ�ͺ���ҺŨ�ȸ�С�����������������á����Ͽ�Ƭ���еĢ٢ڴ��룺��ɫ���������ɵ��Ȼ���ͭ����������±��е���֤������֤�������IJ�������ȷ�ġ��������д��ʵ����������ۡ�
| ��ͬѧ���� | ��ͬѧ��֤���� | ��ʵ����������� |
| ��ɫ�������Ȼ���ͭ | �Ѱ�ɫ��������ϡ�����У���ͨ������ | �� |
��4������������Ͽ�Ƭ�е���Ϣ���������һ��ʵ�鷽������֤��ͬѧ�IJ��롣
| ��ͬѧ���� | �����֤���� | Ԥ������������ |
| ��ɫ�������Ȼ���ͭ | �� | �� |
30����22�֣���ͼ�������ڱ����������Ұ���Ĵ�л;��������ͼ�⡣ͼ���еĢ١��ڡ���
�����ֱ����һ��ø����������ش�
 |
�� ��1������Դ�������࣬�����ڻ����е��Ұ���������������
�� ��2����ø������n��������ͨ���������γɵ�������������ɣ�����ϸ������ı�������Ƚϣ�ø�ٻ���ı������IJ�֮ͬ������������ø���ڳ���ˮ��Ĺ����У�����Ҫ��������ˮ���ӡ�
�� ��3�������Ŵ�ϵ��ͼ�У���1��ȱ��ø�ٶ����б���ͪ��֢����3��ȱ��ø�ڶ������������֢����4���һ���Ѫ�Ѳ���������������״�ĵ�λ����ֱ���A��a��B��b��H��h��ʾ����ͥ���Ҽ�ͥ�������жԷ���ͥ�����ֵ��²�����
|
����
���Ҽ�ͥ�У��������֢���Ŵ���ʽ�����������жϵ���������������
�������ۺϿ�������������״���Ŵ���I3����Ļ���������������
�����ۢ�3�Ѿ��������У�Ԥ�����������ӻ����ĸ���Ϊ��������
31��( 20 ��)�������ҹ���ֲ��һ����Ҫ����ʳ������и߸ѺͰ�������Ʒ�֡���֪����Ũ�ȵij�ù���ܴٽ������쳤�����������ִٽ����ö�ͬ��ֲ��߸�Ʒ�ֺͰ���Ʒ�ֵ�Ч���Ƿ�����?�����һ��Сʵ�����̽����
�����þߣ����������Ĵ��ָ߸����ʹ��ְ��������������ɣ����ƺõ���ȫ����Һ������Ũ�ȵij�ù����Һ������ƿ�ȱ�����Ʒ��(��ù�ص�ʹ�÷�������Ҫ��)
ʵ�鲽�裺
��һ������������ʵ��
A�飺��ȫ����Һ+�߸��������硡 ��
B�飺��ȫ����Һ+������������
���������� C�飺__������������
���������� D�飺__������
�ڶ�����__������
����������¼���������ѵĸ߶ȡ�
Ԥ�����ͽ��ۣ�
��__������
����������������
����������