2003年MAM高考化学仿真试题(五)答案
一、1.C 2.C 3.B 4.C 5.D 6.B 7.A 8.D
二、9.CD 10.D 11.A 12.BC 13.AC 14.D 15.A 16.AC 17.AC 18.AD
|
三、19.(10分)(1)CO2+C====2CO(2分)
(2)CO 澄清石灰水变浑浊(4分,每空2分)
(3)H2 氧化铜与碳粉混合物(4分,每空2分)
20.(12分)(1)C(2分)
(2)A(2分)
(3)检查装置气密性 本反应为放热反应(4分)
(4)将系统内空气排尽 c(4分,每空2分)
四、21.(12分)(1)KMnO4 Cl2(4分,每空2分)
(2)KMnO4和O2 Cl(4分,每空2分)
(3)Cl2+K2MnO4====2KCl+MnO2+O2↑(4分)
22.(10分)(1)3 逆(3分) 1<c≤4(3分)
(2)降温;温度降低,平衡向吸热方向移动。(4分,每空2分)
五、23.(8分)(1)H2SO3(或SO2+H2O)(2分)
(2)Na2SO3、H2O;(2分)
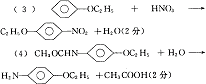
24.(10分)(1)A和B C和F D和E(6分,每空2分)
(2)醇和醚(2分)
(3)都有18O标记;因为反应中间体在消去一分子H2O时,有两种可能,而乙氧基
(―OC2H5)是保留的。(2分)
六、25.(3分)7∶2
26.(11分)(1)讨论:
剩余固体 a的取值 n的取值
Na2CO3 0.15 n=2∶3(2分)
Na2CO3和NaOH 0.03≤a<0.15 ![]() <n≤2(2分)
<n≤2(2分)
Na2CO3・NaOH和Na2O2 a<0.03 n=2(2分)
(2)①当剩余固体全为Na2CO3时,应产生气体0.06 mol,不符题意。(1分)
②当剩余固体为Na2CO3和NaOH时,其中Na2CO3为:![]() =0.025 mol,NaOH为0.12-2×0.025=0.07 mol,固体质量为0.025×106+0.07×40=5.45
g(2分)
=0.025 mol,NaOH为0.12-2×0.025=0.07 mol,固体质量为0.025×106+0.07×40=5.45
g(2分)
③当剩余固体为三者混合物时,产生0.025 mol气体为CO2和O2混合气体,可通过列方程组求得,剩余固体质量为5 g。(2分)